Chapitre 1 : Définition et base de la réglementation
Qu'est-ce que la recherche clinique ?
Source : Loi n° 88-1138, dite loi Huriet-Sérusclat qui régit les recherches biomédicales en France adaptée à la directive européenne n° 2001/20/CE du 4 avril 2001
En pratique, application en France depuis le 27 août 2006, du nouveau dispositif législatif et réglementaire, encadrant les recherches biomédicales, instauré par la loi de santé publique du 9 août 2004.
On entend par recherche clinique une étude menée sur l'être humain dans le domaine de la santé.
Une Recherche Biomédicale se définit comme "une recherche organisée et pratiquée sur l'être humain en vue du développement des connaissances biologiques et médicales".
Cette recherche est utile car elle permet le progrès en matière de soins.
Très encadrée, elle respecte un protocole d'étude précis et n'est réalisée qu'à certaines conditions :
- avoir pour but d'augmenter les connaissances médicales,
- être menée par des personnes compétentes
- prendre toutes les mesures pour protéger les personnes qui se prêtent à la recherche,
- le responsable de cette recherche ("le promoteur") doit obtenir les autorisations réglementaires et avoir fait toutes les démarches légales et éthiques nécessaires.
Quand on parle de recherche clinique on pense généralement à l'essai de nouveaux médicaments : meilleure efficacité, meilleure tolérance, moindre toxicité, moindre coût ... Elle ne se limite pas à cela, surtout dans les centres hospitalo-universitaires où se côtoient plusieurs types de recherches interventionnelles et observationnelles.
Le cadre réglementaire
1 - Les recherches interventionnelles
Les recherches biomédicales sont définies comme "les recherches organisées et pratiquées sur l'être humain en vue du développement des connaissances biologiques et médicales". Ce type de recherches est autorisé en France, sous réserve du respect notamment des dispositions des articles L.1121-1 et suivants du Code de la santé publique.
1.1 - Les recherches biomédicales portant sur un médicament sont entendues comme tout essai clinique d'un ou plusieurs médicaments visant à déterminer ou à confirmer leurs effets cliniques, pharmacologiques et les autres effets pharmacodynamiques ou à mettre en évidence tout effet indésirable, ou à en étudier l'absorption, la distribution, le métabolisme et l'élimination, dans le but de s'assurer de leur innocuité ou de leur efficacité. (Article R1121-Décret n°2006-477 du 26 avril 2006 - art. 1 JORF 27 avril 2006).
1.2 - Les recherches biomédicales portant sur un dispositif médical sont entendues comme tout essai clinique ou investigation clinique d'un ou plusieurs dispositifs médicaux visant à déterminer ou à confirmer leurs performances ou à mettre en évidence leurs effets indésirables et à évaluer si ceux-ci constituent des risques au regard des performances assignées au dispositif. (Article R1121-Décret n°2006-477 du 26 avril 2006 - art. 1 JORF 27 avril 2006).
1.3 - Les autres catégories de recherches biomédicales mentionnées au premier alinéa de l'article L. 1121-1 font l'objet, en tant que de besoin, d'une définition par arrêté du ministre chargé de la santé, pris sur proposition du directeur général de l'Agence française de sécurité sanitaire des produits de santé pour les produits relevant de sa compétence. (Article R1121-Décret n°2006-477 du 26 avril 2006 - art. 1 JORF 27 avril 2006). Soit dans la pratique, les recherches biomédicales hors produits de santé sont l'évaluation des actes, combinaisons d'actes ou stratégies médicales de prévention, de diagnostic ou de traitement qui ne sont pas de pratique courante.
1.4 - Les recherches biomédicales portant sur les soins courants sont les recherches autres que celles portant sur les médicaments, lorsque tous les actes sont pratiqués et les produits utilisés de manière habituelle mais que des modalités particulières de surveillance sont prévues par un protocole,…
Ce sont les recherches dont l'objectif est d'évaluer des actes, combinaisons d'actes ou stratégies médicales de prévention, de diagnostic ou de traitement qui sont de pratique courante, c'est-à-dire faisant l'objet d'un consensus professionnel, dans le respect de leurs indications.
En sont exclues :
- les recherches qui portent sur des techniques ou des stratégies innovantes, ou considérées comme obsolètes….
- les recherches qui portent sur l’évaluation d’une combinaison innovante d’actes ou de produits, même si chacun d’eux pris isolément est d’utilisation courante….
- les recherches qui portent sur une comparaison de stratégies médicales, lorsque l’une de ces stratégies peut être considérée supérieure à l’autre en termes de sécurité et d’efficacité.
Les modalités particulières de surveillance mises en œuvre dans ces recherches ne comportent que des risques et des contraintes négligeables pour la personne qui se prête à la recherche. L'information de cette dernière fait l'objet d'un document écrit soumis préalablement au comité de protection des personnes intéressé. (Article R1121-3 Décret n°2006-477 du 26 avril 2006 - art. 1 JORF 27 avril 2006).
2 - Les recherches non interventionnelles ou observationnelles
Les recherches définies au 1° de l'article L. 1121-1 appelées "recherches non interventionnelles" sont des recherches pour lesquelles la stratégie médicale destinée à une personne qui se prête à la recherche n'est pas fixée à l'avance par un protocole et relève de la pratique courante.
Les recherches non interventionnelles portant sur des produits mentionnés à l'article L. 5311-1 sont entendues comme toute recherche dans le cadre de laquelle le ou les produits sont prescrits ou utilisés de manière habituelle. Elles se conforment :
- Pour les recherches portant sur les médicaments, à l'autorisation de mise sur le marché mentionnée à l'article L. 5121-8 ;
- Pour les recherches portant sur les dispositifs médicaux, à la notice d'instruction, ou pour les recherches portant sur les dispositifs médicaux de diagnostic in vitro, à la notice d'utilisation ;
- Pour les recherches portant sur les produits sanguins labiles, à la décision mentionnée au 1° de l'article L. 1221-8 ;
- Pour les recherches portant sur les tissus issus du corps humain et sur les préparations de thérapie cellulaire, à l'autorisation mentionnée à l'article L. 1243-5 ;
- Pour les recherches portant sur les produits cosmétiques ou les produits de tatouage, à toute étude menée chez des volontaires sains, à l'aide de méthodes d'investigations à risque négligeable, sur des produits dont la sécurité d'emploi est établie, lorsqu'ils sont appliqués dans des conditions normales d'emploi ou selon des méthodes reproduisant ces conditions.
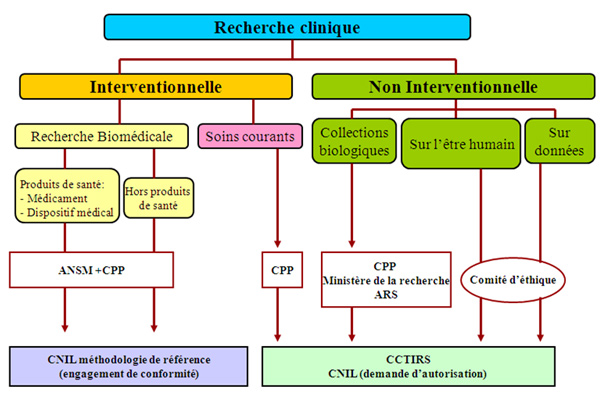
ANSM : Agence Nationale de Sécurité du Médicament
CPP : Comité de Protection des Personnes (donne une autorisation, le comité d’éthique, structure différente, ne délivre pas d’autorisation mais un avis consultatif).
CNIL : Commission nationale de l'informatique et des libertés
CCTIRS : Comité consultatif sur le traitement de l'information en matière de recherche dans le domaine de la santé
ARS : Agence Régionale de la Santé
Evolution de la réglementation pour 2013-2014
Source : Loi n° 2012-300 du 5 mars 2012 relative aux recherches impliquant la personne humaine (décrets d’application à paraître).
Après une première adoption au parlement en janvier 2009, la loi dite « Jardé », encadrant les recherches sur la personne humaine, a finalement été promulguée en mars 2012. Ce long parcours, qui n’est cependant pas totalement terminé dans la mesure où restent en attente les décrets et arrêtés qui en permettront l’application. Elle permet cependant une évolution notable de la législation en matière de recherche clinique notamment par l’intégration plus claire des recherches non interventionnelles et par la définition de compétences élargies des Comités de Protection des Personnes (CPP).
Cette loi encadrant les recherches sur la personne humaine s’inscrit dans la suite et l’esprit des lois antérieures. Parmi les principales nouveautés, la loi Jardé étend le cadre juridique à l’ensemble des recherches menées sur la personne humaine en définissant 3 catégories tenant compte des risques encourus par les sujets.
Quelques-uns des principaux changements :
- Trois catégories de recherche bien distinctes et une réglementation adaptée aux recherches interventionnelles à risques et contraintes minimes.
- Tableau comparatif entre la législation en vigueur au 7 décembre 2012 et la future loi Jardé :
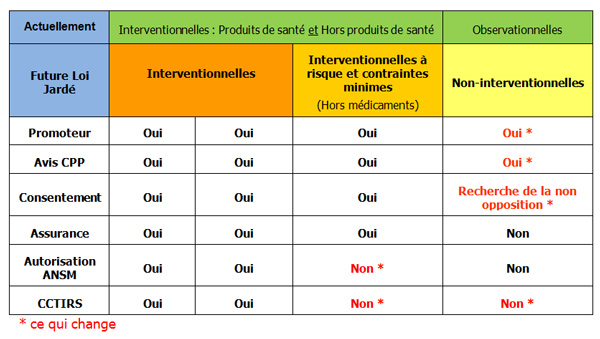
- Avant de réaliser une recherche impliquant la personne humaine, le promoteur doit soumettre le projet à l’avis d’un comité de protection des personnes désigné de manière aléatoire par la commission nationale.
- Pour les recherches non interventionnelles les participants recevront une information préalable avec la possibilité de s'opposer à la recherche. Ces recherches seront aussi soumises à l'autorisation des CPP.
- Pour les Recherches Interventionnelles à Contraintes Minimes et non interventionnelles: rédaction de nouvelles Bonnes Pratiques Cliniques, répertoire des recherches rendu public.
- En cas de doute sur la qualification d’une Recherche au regard des trois catégories: le CPP saisit pour avis l’Agence Nationale de Sécurité du Médicament (ANSM).
- La loi définit "les Recherches Interventionnelles à finalité non commerciale", dans le cadre desquelles l'assurance maladie prend en charge les produits de santé utilisés conformément à leur autorisation de mise sur le marché (AMM) ou, par dérogation, hors AMM.
- Un investigateur risque 3 ans d’emprisonnement et 45 000 € d’amende pour une recherche non interventionnelle pratiquée alors que la personne s’y est opposée.
Lexique
Source : Direction Générale de la Santé.
Approche fondée sur le risque (Risk-based approach)
Méthode générale de gestion des recherches biomédicales en quatre étapes : 1) Identification, analyse et hiérarchisation des risques ; 2) Mise en place de mesures d'atténuation (prévention, réduction, ou élimination) des risques ; 3) Conduite de la recherche et évaluation continue des risques; 4) Mise à jour des mesures d'atténuation des risques.
Assurance de la qualité
Ensemble des activités préétablies et systématiques mises en œuvre pour s'assurer que la recherche est réalisée et que les données sont générées, recueillies par écrit, documentées, enregistrées et rapportées conformément aux bonnes pratiques cliniques et aux dispositions législatives et réglementaires en vigueur.
Attaché de recherche clinique, moniteur ou assistant
Personne mandatée par le promoteur, chargée d'assurer pour ce dernier le suivi de la recherche biomédicale et le contrôle de sa qualité (mise en place sur site des essais cliniques, réalisation du suivi et du contrôle de la qualité scientifique, technique et réglementaire des projets de recherche clinique ).
Audit d'une recherche biomédicale
Examen indépendant et méthodique des activités et des documents relatifs à la recherche, en vue de déterminer si les activités liées à la mise en place et au suivi de cette recherche ont été réalisées, et si les données ont été recueillies, analysées et rapportées dans le respect du protocole, des procédures opératoires standardisées préétablies, des bonnes pratiques cliniques et des dispositions législatives et réglementaires en vigueur.
Biostatisticien
Personne diplômée en statistique ou bio-statistique qui conçoit les méthodologies statistiques et réalise les analyses statistiques des données des études de recherche préclinique et clinique.
Cahier d'observation
Document, quelque soit son support (par exemple : support papier, optique, magnétique ou électronique), destiné à recueillir par écrit toutes les informations requises par le protocole concernant chaque personne qui se prête à la recherche, et qui doivent être transmises au promoteur.
Cahier d'observation électronique (eCRF- Electronic Case Report Form)
1) Cahier d'observation électronique permettant le recueil, le contrôle et l'exploitation des données d'une étude clinique sur chaque sujet de recherche. 2) CRF dans lequel les données et leurs commentaires, notes et signatures sont reliés électroniquement.
Centre de recherche clinique
Infrastructure consacré à la recherche clinique à but non lucratif, financée par l’état, et placée aux niveau des hôpitaux, équipée de lits et de personnel. C’est une plateforme de services méthodologiques et techniques à disposition des équipes de soins engagées dans un projet de recherche.
Centre de traitement de données (Data Center)
Centre qui joue un rôle-clé dans la conception et l’analyse des projets d’essais cliniques, la gestion des données de chaque malade, et le stockage et le partage des données. Il regroupe plusieurs types de compétences : méthodologistes, statisticiens, bio-informaticiens, data
managers, ARC (assistant de recherche clinique) et TEC (technicien en recherche clinique).
Chef de projet
Personne qui gère un portefeuille de projets en recherche clinique (dont l'établissement est promoteur) sur les aspects réglementaires, financiers, logistiques, administratifs, organisationnels et humains.
Conservation
Désigne ici tout procédé qui permet d’assurer la pérennité de l’échantillon.
Coordinateur d’étude clinique
Personne qui guide les investigateurs dans les démarches réglementaires et dans la mise en place des études.
Economiste de la santé
Personne qui recueille, analyse et évalue l'information médico-économique nécessaire aux décideurs hospitaliers en lien avec les cliniciens dans le domaine des technologies de santé et des programmes de santé publique, afin d'optimiser les prises de décision. Ce métier se situe à l'interface entre le domaine de l'économie et de la médecine
Recherche biomédicale
Le Code français de la santé publique définit la recherche biomédicale comme une "recherche organisée et pratiquée sur l'être humain en vue du développement des connaissances biologiques ou médicales". Ce type de recherche est autorisé en France, sous réserve du respect notamment des dispositions des articles L.1121-1 et suivants du Code de la santé publique.
Essai clinique ou recherche biomédicale portant sur un médicament
Conformément au premier alinéa de l'article R. 1121-1 du code de la santé publique, une recherche biomédicale portant sur un médicament est entendue comme tout essai clinique (réalisé sur l'être humain) d'un ou plusieurs médicaments visant à déterminer ou à confirmer leurs effets cliniques, pharmacologiques et les autres effets pharmacodynamiques ou à mettre en évidence tout effet
indésirable, ou à en étudier l'absorption, la distribution, le métabolisme et l'élimination, dans le but de s'assurer de leur innocuité ou de leur efficacité.
Gestionnaire des données (Data Manager)
Personne qui traite les données des études cliniques. Elle est responsable du contrôle de la cohérence et de la qualité des données cliniques.
Gestion électronique des documents - GED (Document management system)
Procédé informatisé visant à organiser et gérer des informations et des documents électroniques au sein d'une organisation.
Gestion des requêtes (Query Management)
Processus d'examen en continu des données, des divergences, de la production et de la résolution des erreurs et des incohérences qui se posent dans la saisie et la transcription des données des essais cliniques.
Groupe coopérateur
Ensemble de médecins des hôpitaux de type CHU ou non qui travaillent ensemble sur la même maladie de manière à appliquer des protocoles et essayer de faire avancer la science ou le traitement sur telle ou telle maladie. Par définition, un groupe coopérateur est multicentrique, c’est à dire au minimum va s’adresser à plusieurs types de structures hospitalières, des centres anti-cancéreux, des hôpitaux régionaux et dans différentes parties de la France.
Investigateur
Selon la loi Huriet, l’investigateur d’un essai clinique est forcément un médecin qui dirige et surveille la réalisation de la recherche biomédicale (article L1121-3 du Code de la Santé publique). Ce médecin doit justifier d’une expérience appropriée. "Dans les sciences du comportement humain, une personne qualifiée conjointement avec l'investigateur peut exercer la direction de la recherche. Les recherches biomédicales concernant le domaine de l'odontologie ne peuvent être effectuées que sous la direction et la surveillance d'un chirurgien-dentiste et d'un médecin justifiant d'une expérience appropriée".
Logiciel de gestion de projets (Project management software)
Terme qui regroupe les différents et nombreux types de logiciels, y compris ceux de la planification, d'allocation des ressources, ou logiciels de collaboration, de communication et des systèmes de documentation, qui sont utilisés pour faire face à la complexité des grands projets.
Logiciel libre (Open source software)
Logiciel dont l'utilisation, l'étude, la modification et la duplication en vue de sa diffusion sont permises, techniquement et légalement afin de garantir certaines libertés induites, dont le contrôle du programme et la possibilité de partage entre utilisateurs.
Méthodologiste
Personne le plus souvent l‘épidémiologiste, le pharmacologue ou le biostatisticien qui aide à la conception des projets, et supervise le déroulement des études à toute les étapes. Méthodologiste assure aussi la rédaction des protocoles en maîtrisant les divers schémas d'études, le calcul de la taille d’échantillon, le plan et le rapport d’étude, l’analyse statistique, la programmation et rédaction de publications, etc.
Monitorage
Fait d'exercer au cours d'une recherche biomédicale une activité de contrôle de qualité auprès des sites investigateurs. Ces activités peuvent s'exercer sur site, ou à distance (depuis l'unité d'essai clinique), ou de façon combinée.
Outil de monitorage
Tout dispositif, modèle de document, procédure, ou circuit, qui permet la réalisation d'une tâche de monitorage. Les outils de monitorage sont utilisés sur site ou à distance, ou de façon combinée. Les outils de monitorage fondés sur le risque sont ceux permettant l'implémentation de l'approche fondée sur le risque : outils de monitorage à distance, ou permettant de réduire le recours au monitorage sur site.
Préparation
Désigne ici toutes les actions menées sur les échantillons biologiques qui permettront de le rendre utilisable pour la recherche.
Procédures opératoires standardisées (POS)
Instructions détaillées, écrites, préétablies visant à uniformiser la manière d'effectuer une activité.
Promoteur
Selon la loi Huriet-Sérusclat (CSP, art. L1121-1, révisée le 9 août 2004) le promoteur est "la personne physique ou morale qui prend l'initiative d'une recherche biomédicale sur l'être humain, qui en assure la gestion et vérifie que le financement de la recherche est prévu".
En pratique, le promoteur doit choisir l'investigateur, recruter des ARC contrôleurs de qualité, soumettre le protocole de la recherche à l'avis du CPP et à l'autorisation de l'autorité compétente, contracter une assurance couvrant les conséquences éventuelles de cette recherche, et déclarer au Ministère ou à l'ANSM les éventuels événements indésirables survenus au cours de la recherche. De plus, il est habituel que le promoteur prenne en charge les coûts de la recherche mais ce n'est pas obligatoire puisqu'un tiers peut financer la recherche sans se porter obligatoirement promoteur. A la fin de la recherche, le promoteur avise l'autorité compétente et le CPP que la recherche est terminée ou indique les raisons qui motivent l'arrêt de la recherche lorsqu'il est anticipé.
Risque
La combinaison de la probabilité de la survenue d'un dommage et de la gravité de ce dommage (ISO/IEC Guide 51). Dans les recherches biomédicales, les risques peuvent concerner le participant, le site investigateur, l'unité d'essai clinique, le promoteur, la population générale.
Saisie de données à distance (Remote Data Entry)
Processus de collecte de données dans les essais cliniques au format électronique sur les sites d'essai, en utilisant le cahier d'observation électronique (eCRF).
Saisie électronique des données (Electronic Data Capture)
Système informatisé conçu pour la collecte des données d’essais clinique au format électronique. Toutes les données doivent être tractables, elles doivent être archivées dans leur totalité pendant au moins trois ans et leur consultation doit être relativement aisée.
Système de gestion de base de données (SGBD)
Collection de logiciels permettant de créer, de gérer et d’interroger efficacement une base de données indépendamment du domaine d’application tout en garantissant la qualité, la pérennité et la confidentialité des informations.
Système de gestion des essais cliniques (Clinical Trial Management System)
Système utilisé pour gérer la planification, la préparation, la performance et le rapport des essais cliniques, mettant l'accent sur la conservation des informations de contact mises à jour pour les participants et les délais de suivi.
Technicien d’étude clinique
Exerçant à l’hôpital, le technicien d’études cliniques (TEC) réalise la saisie des données cliniques recueillies auprès des patients, afin de mettre en place le déroulé de l’étude de recherche. Dans ce cadre, il gère ces données et traite les informations qu’il peut en tirer, les analyse, les diffuse au médecin investigateur de l’équipe de recherche, les suit puis les classe.
Unité d’essai clinique
Unité qui assure la coordination méthodologique et l'analyse des données des essais cliniques. Elle fournit l’aide à la conception de l'étude, l‘organisation, la logistique, la sélection des centres, la gestion des données, le suivi, l'analyse des données et le reporting.
Validation du système informatique (Computer System Validation)
Processus documenté qui sert à assurer qu'un système informatique exécute exactement pour quoi il est conçu d'une manière cohérente et reproductible.
Valorisation
Valorisation hospitalière consiste à transférer les résultats obtenus par les équipes de recherche clinique vers les acteurs susceptibles de les développer, de les transformer en produits et activités au bénéfice des patients, du système de soins et de la population.
C’est aussi une démarche de protection des inventeurs, ainsi que des hôpitaux qui assurent la promotion ou la validation clinique de ces inventions, avant la publication des résultats. La valorisation vise le monde socio-économique, dans un but d’associer les établissements de santé au développement économique de leur territoire, grâce à des partenariats industriels. La valorisation de la recherche permet que les résultats tangibles, scientifiques ou commerciaux de la recherche clinique puissent bénéficier en retour aussi bien aux inventeurs qu’à leurs « hôpitaux – employeurs ».
Chapitre 2 : Principales structures impliquées dans la recherche clinique hospitalière
DÉLÉGATION RECHERCHE CLINIQUE ET INNOVATION (DRCI)
La DRCI est consultée sur la politique de la recherche et a un rôle d’animation scientifique, d’incitation et de soutien auprès des équipes hospitalières pour l’émergence des projets de recherche clinique et biomédicale, et la mise en œuvre des innovations.
Missions
Les missions de la DRCI sont reprécisées dans la CIRCULAIRE N° DGOS/PF4/2011/329 du 29 JUILLET 2011 relative à l’organisation de la recherche clinique et de l’innovation et au renforcement des structures de recherche clinique.
La DRCI est chargé des trois missions essentielles, en matière d'appui à la recherche clinique, que sont:
1. la promotion : organisation, administration, gestion, contrôle, appui technico-réglementaire de la recherche cliniques
Les DRCI s’appuient sur des structures opérationnelles comme la Cellule Promotion de la Recherche Clinique dont les missions sont les suivantes :
- coordination de la conception d'un projet de recherche clinique dans le cadre d'une réponse à un appel d'offre suivie d'une demande de promotion CHU ou bien d'une demande de promotion CHU sans réponse à un appel d'offre ;
- coordination et gestion de projets financés par les Attachés de Recherche Clinique (ARC) : création des documents de l'étude (CRF, plaquettes, fiche d'inclusion, procédures, ...) / visites de mise en place (MEP), monitoring, clôture / assistance pour les amendements / gestion de l'archivage / correspondances centres (courriers, contacts téléphoniques, réunions, lettres d'informations,...) ;
- gestion des inclusions par randomisation ;
- suivi des inclusions, suivi des rapport de monitoring, suivi des rapports de MEP et de clôture ;
- affaires réglementaires : constitution et suivi du dossier réglementaire pour les demandes d'autorisations à l'autorité compétente, au CPP et à la CNIL, veille réglementaire, formation sur la législation encadrant les recherches menées sur la personne ;
- vigilance des essais cliniques : déclaration des EIG et de leur suivi dans les délais imposés, rédaction de rapports annuel de sécurité, mise à disposition exigible par l'ANSM du recueil des EI/EIG à tout moment de l'étude ;
- coordination des fins d'essai : déclaration de fin d'essai et coordination de l'écriture du rapport final pour l'ANSM ;
- gestion des bases de données d'études cliniques : création de bases de données, saisie informatique, gestion et édition des queries ;
- rédaction et mise en place de procédure opératoire standard, de documents opérationnels, de mode opératoire, de fiches techniques contribuant à la qualité de la recherche clinique ;
- missions d'aide à l'investigation : aide au screening des patients, aide au remplissage des CRFs , aide à la gestion des rendez-vous patients ;
- coordination des études non promues par le CH référent.
2. l'aide méthodologique, la gestion de données et la bio statistique
Aide rédactionnelle, méthodologie des essais cliniques, conception des essais cliniques, organisation de la chaine de traitement des données (gestion de bases de données, traitement des données, statistiques),
Les DRCI s’appuient sur des Unités de Méthodologie comme l’Unité de Biostatistique et de Recherche Clinique dont les missions sont les suivantes :
- soutien méthodologique et statistique dans la cadre de la rédaction de projets de recherche (Projets Hospitaliers de Recherche Clinique, Projets industriels, STIC, Appels d’Offre Interne, INCa...),
- formation des médecins et des personnels soignants à la méthodologie de la recherche clinique,
- analyse statistique des données et interprétation des résultats,
- expertises méthodologiques en recherche clinique et épidémiologique,
- rédaction d'articles scientifiques,
- enseignements universitaires et hospitaliers de la biostatistique et de la méthodologie des essais cliniques et accueil des étudiants et de stagiaires.
3. l'aide à l'acquisition des données
Plateformes d'investigation et de recherche clinique, d'aide aux cliniciens et d'interface avec les patients et les volontaires sains (inclusion, organisation du recueil des données patient, cliniques, biologiques, imagerie, etc.).
Les DRCI s’appuient sur des Centre de Recherche Clinique (CRC) dont les missions sont les suivantes :
- Participer au développement de technologies et de molécules innovantes en réalisant tous travaux de recherche, et en élaborant des projets et des études cliniques pour le développement de produits de santé dont les applications peuvent être :
- médicales,
- pharmaceutiques,
- et concerner les protocoles de radiodiagnostic.
Ces travaux seront indépendamment d'origine académique, universitaire ou industrielle.
Les études cliniques peuvent porter sur :
- le développement de produits de santé,
- la recherche fondamentale,
- les études cliniques de phase 1, 2, 3 ou 4 sur des volontaires sains et des patients,
- des études pharmaco-épidémiologiques.
- La réalisation d'études de 1ère administration à l'Homme (volontaire sain ou patient volontaire), est encadrée par une réglementation très complexe, qui vise à assurer la sécurité maximale des volontaires se prêtant à la recherche, et à évaluer avec rigueur extrême la tolérance de ces produits.
De telles recherches ne peuvent en effet être effectuées que dans des centres spécialisés, ce que permet le CRC avec des équipes pluri-disciplinaires dans un cadre hospitalo-universitaire permettant l'accès à un plateau technique et de soins d'urgence et de réanimation.
Le CRC répond à des normes de confidentialité pour garantir aux industriels développant des molécules innovantes que le résultats des essais restent une propriété industrielle ultra-confidentielle.
Enfin la DRCI a un rôle d'animation scientifique, d'incitation et de soutien auprès des équipes hospitalières pour l'émergence des projets de recherche clinique et biomédicale, et la mise en œuvre des innovations.
Elle aide à la mise en forme des dossiers candidats et les classe dans les réponses aux appels d'offre.
Elle veille à la qualité de la mise en œuvre et au suivi réglementaire et scientifique des projets retenus et promus par le CHU. Elle organise la diffusion des appels à projets. Enfin, elle organise et valide l'évaluation médico-économique de l'innovation ou d’activités nouvelles.
COMITÉ DE PROTECTION DES PERSONNES (CPP)
Le comité évalue les projets de recherche clinique au regard de la balance bénéfices/risques et de la protection des personnes susceptibles de participer à des recherches menées sur la personne humaine avant d’autoriser leurs mises en oeuvre.
Rôle
Avant d’autoriser la mise en œuvre des projets de recherche clinique, le comité évalue le projet au regard de la protection des personnes susceptibles de participer, de la pertinence de l’objectif de la recherche, de la balance bénéfices/risques.
Les missions des Comités de Protection des Personnes sont définies par le Code de la Santé Publique :
Nouvelle partie législative :
Première partie, Livre 1, Titre 2 : "Recherches biomédicales"
Nouvelle partie réglementaire :
Première partie, Livre 1, Titre II, Chapitre III : "Comités de protection des personnes et autorité compétente"
Recherches soumises au CPP pour examen et avis
- RBM portant sur un médicament à usage humain ;
- RBM ne portant pas sur un produit mentionné à l’article L.5311-1 du CSP (ex : essais nutritionnels, études physiologiques...) ;
- RBM en soins courants (assurance de l’établissement, pas de consentement mais document d’information paraphé et signé) ;
- RBM de dispositifs médicaux, dispositifs médicaux in vitro ;
- Constitution d’une collection d’échantillons biologiques, en cas d’utilisation d’éléments et de produits du corps humain à des fins scientifiques ;
- RBM portant sur des produits cosmétiques et de tatouage ;
- Etudes observationnelles.
Sont également soumises pour examen et avis toutes modifications substantielles en cours d’essai ne remettant pas en cause l’objectif principal. Elles portent le plus souvent sur le déroulement scientifique de l’essai, les modifications de la lettre d’information avec recueil d’un nouveau consentement, la prolongation d’étude, l’ouverture ou fermeture de centre(s).
Le comité veille à ce que :
- la personne qui se prête à la recherche ne soit exposée à aucun risque important et s’il existe des risques, que ceux-ci soient nettement inférieurs au bénéfice espéré,
- la personne susceptible de participer à un essai soit parfaitement et honnêtement informée de l’objectif de l’essai, de son déroulement, des servitudes qui en découlent, des bénéfices attendus et surtout de tous les risques possibles,
- la rédaction de cette information, pour être bien comprise, soit rédigée en termes simples et accessibles aux personnes n’ayant pas de connaissances médicales,
- le délai de réflexion soit respecté permettant, si la personne le souhaite, de soumettre le projet à son médecin de famille.
Autres missions
Le CSP prévoit également que le Comité de Protection des Personnes soit informé :
- de la première inclusion dans l’essai notifiant le début de l’essai,
- du rapport annuel de sécurité (recherche sur médicament à usage humain),
- du rapport final notifiant la fin de l’essai.
Composition
Membres du comité :
Les membres du CPP sont répartis en 2 collèges. Chaque catégorie est composée pour moitié de membres titulaires et suppléants.
Collège 1 scientifique
- 8 médecins qualifiés en recherche biomédicale
- 2 médecins généralistes
- 2 pharmacien(ne)s hospitaliers
- 2 infirmier(e)s
Collège 2 société civile
- 2 personnes qualifiées en éthique
- 2 psychologues
- 2 travailleurs sociaux
- 4 juristes
- 4 représentants des usagers de la santé
Fonctionnement
Durée du mandat :
Les membres composant le comité sont nommés, à titre bénévole, par le Préfet de Région, après appel à candidatures auprès des instances concernées (CHU, ARS, rectorat...), pour une durée de trois ans, mandat renouvelable une seule fois pour une durée identique de trois ans.
Réunions :
Pour chaque dossier, deux rapports sont établis, l’un par un membre du collège scientifique, l’autre par un membre de la société civile sur désignation du président en fonction de leur compétence scientifique (collège 1) ou sociale (collège 2).
Les rapports écrits sont présentés oralement lors des séances plénières et non publiques et servent de base aux délibérations sur lesquelles le nom des rapporteurs demeure confidentiel. Le dossier est discuté par l’assemblée et soumis au vote.
Le comité peut émettre un :
- avis favorable : si le CPP a donné son avis favorable et l’AFSSAPS son autorisation, l’essai peut débuter,
- avis réservé : demande de complément d’informations. Un délai de 3 mois est accordé au promoteur pour apporter une réponse. A la réception du complément d’informations, le comité délibère et donne un avis définitif après avis des deux rapporteurs,
- avis défavorable : cet avis peut faire l’objet d’un recours sur la base des articles L.1123-6-al.2 et R.1123-7 du Code de la Santé Publique.
Après avis, les dossiers sont archivés avec le dossier du protocole de recherche.
Les membres du comité s’engagent à n’avoir aucun conflit d’intérêt.
recours à des experts :
Si le projet d’essai prévoit d’inclure des mineurs, le comité se voit dans l’obligation de s’adjoindre les compétences d’un pédiatre (voix non délibérative).
Le comité fait également appel aux compétences d’un expert pour examiner le projet de recherche qui lui a été confié s’il ne compte pas parmi ses propres membres un médecin ou un pharmacien suffisamment qualifié dans la discipline présentée (voix non délibérative).
Si le projet inclut des analyses génétiques, le comité s’assure que celles-ci portent bien sur la pathologie étudiée dans le protocole.
Si le projet prévoit une collection d’échantillons biologiques, le comité vérifie si les autorités sanitaires ont été informées.
L’investigateur peut, soit à la demande du comité, soit à sa propre demande, exposer lui-même son projet.
COMITÉ DE LA RECHERCHE EN MATIÈRE BIOMÉDICALE ET DE SANTÉ PUBLIQUE (CRBSP)
Source : Décret no 2006-1355 du 7 novembre 2006 relatif au comité de la recherche en matière
biomédicale et de santé publique et modifiant le code de la santé publique.
Dans chaque CHU, le CRBSP veille à la coordination des activités de recherche exercées par les établissements et organismes qui les composent ou leur sont associés.
Composition
Le Comité de la recherche en matière biomédicale et de santé publique comprend 12 membres qualifiés dans le domaine de la recherche désignés comme suit :
- 4 représentants du CH référent, désignés conjointement par le Directeur Général et le Président de la Commission Médicale d’Etablissement après avis du Directoire et de la Commission médicale d’Etablissement,
- 4 représentants de l’Université, désignés conjointement par son Président et les Directeurs des unités de formation et de recherche en médecine, pharmacie et odontologie (si applicable),
- 4 représentants des organismes de recherche associés aux missions du CHU dans le cadre des conventions de partenariat pour les missions de recherche, soit l’INSERM, le CNRS et le CEA, désignés par le Président de l’INSERM après consultation de leurs Directeurs respectifs.
Missions
Le Comité de la Recherche en matière Biomédicale et de Santé Publique est une structure de réflexion stratégique sur la recherche et qui en coordonne les activités entre les structures partenaires.
Il est consulté sur les projets concernant :
- les modifications et le renouvellement de la convention qui institue la collaboration hospitalo-universitaire,
- les conventions d’association relatives au partenariat pour les missions de recherche,
- la politique de recherche, telle qu’elle résulte du projet d’établissement du CHU ainsi que des établissements de santé associés aux missions du CHU dans le cadre des conventions de collaboration hospitalo-universitaire,
- le volet relatif à l’enseignement, à la recherche et à l’innovation du contrat pluriannuel d’objectifs et de moyens des CHU et de chacun des établissements de santé dans le cadre des conventions de collaboration hospitalo-universitaire,
- les dispositions relatives à la recherche biomédicale et en santé publique du contrat d’établissement pluriannuel des établissements publics à caractère scientifique, culturel et professionnel,
- le projet de recherche des pôles d’activité des établissements publics,
- la participation du CHU aux structures de coopération.
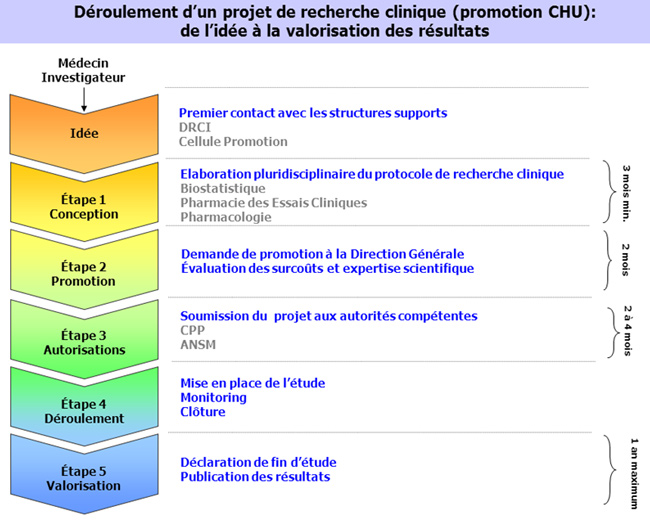
Chapitre 3 : Vie d’un projet de recherche
LA VIE D'UN PROJET DE RECHERCHE