Objectifs pédagogiques
- Connaître l'épidémiologie des méningites et encéphalites chez l'adulte et l'enfant.
- Diagnostiquer un purpura fulminans (cf item 332), une méningite, une méningoencéphalite.
- Connaître les principaux agents infectieux responsables de méningites, de ménin-goencéphalites, d'abcès cérébraux.
- Connaître la conduite à tenir dont le traitement en urgence face à un purpura fulminans, une suspicion de méningite ou de méningoencéphalite, au domicile, au cabinet médical et aux urgences hospitalières.
- Hiérarchiser les examens complémentaires en cas de suspicion de méningite, de méningoencéphalite.
- Interpréter le résultat d'un examen du liquide céphalorachidien.
- Connaître le traitement de première intention d'une méningite communautaire présumée bactérienne.
- Connaître les recommandations de la prophylaxie des infections à méningocoque dans l'entourage d'un cas de méningite à méningocoque.
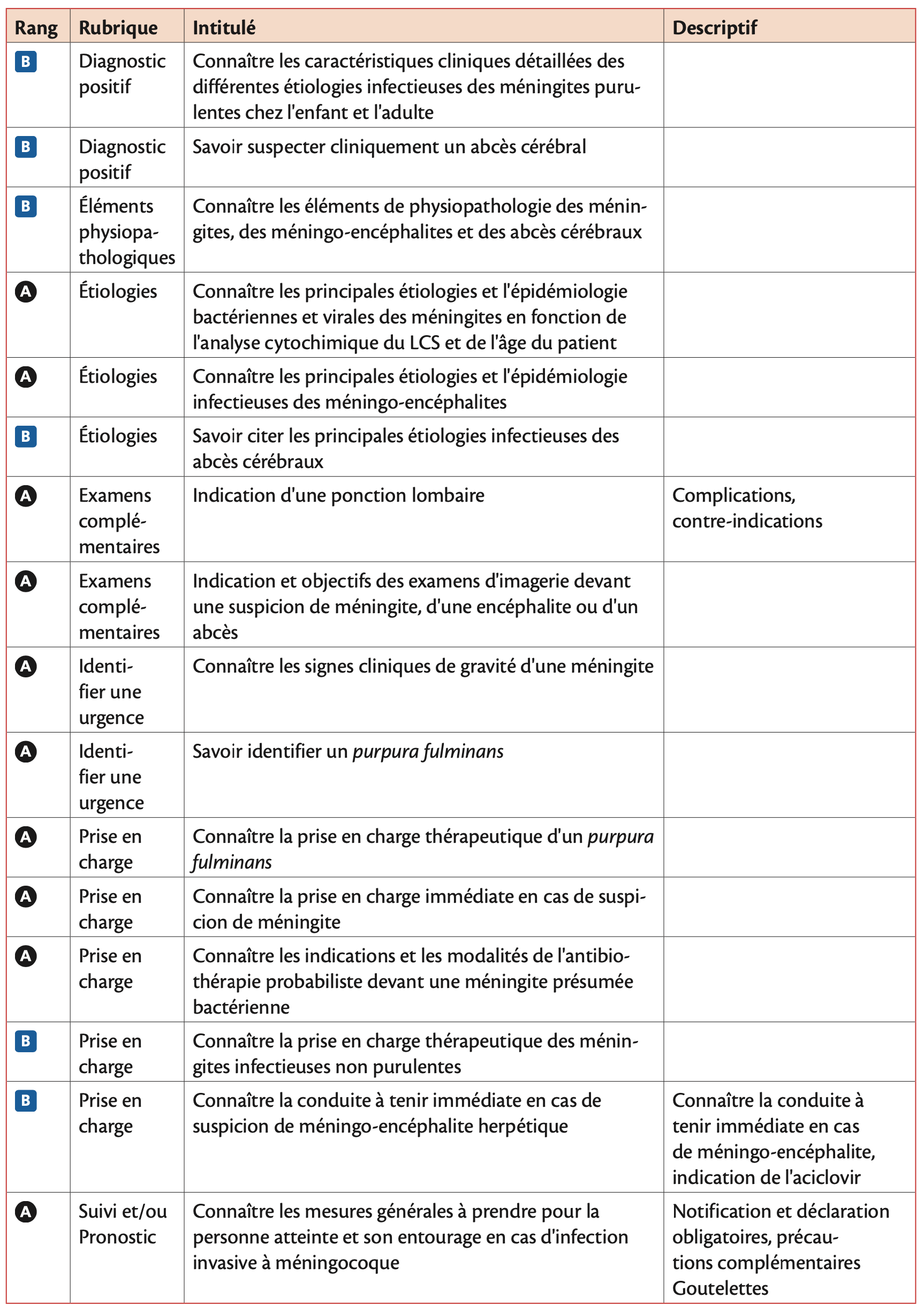
Hiérarchisation des connaissances

I. Pour comprendre
 Les méninges sont constituées de trois membranes enveloppant l'encéphale et la moelle spinale, qui sont, de dehors en dedans :
Les méninges sont constituées de trois membranes enveloppant l'encéphale et la moelle spinale, qui sont, de dehors en dedans :
- la dure-mère : couche superficielle résistante accolée à l'os ;
- l'arachnoïde : couche moyenne;
- la pie-mère : couche interne recouvrant directement le cerveau.
- La dure-mère constitue la pachyméninge; l'arachnoïde et la pie-mère forment la leptoméninge.
- L'espace sous-arachnoïdien (situé entre l'arachnoïde et la pie-mère) contient le liquide cérébrospinal (LCS).
 Le terme de méningite désigne l'inflammation des enveloppes méningées. En cas d'atteinte associée du parenchyme cérébral, on parle de méningo-encéphalite.
Le terme de méningite désigne l'inflammation des enveloppes méningées. En cas d'atteinte associée du parenchyme cérébral, on parle de méningo-encéphalite. La majorité des méningites et méningo-encéphalites aiguës sont infectieuses par contamination du LCS par un agent infectieux (le plus souvent une bactérie ou un virus). La contamination peut se faire par voie hématogène (le plus fréquemment), par contiguïté à partir des cavités ORL, ou plus rarement par inoculation directe (traumatisme, chirurgie). L'atteinte encéphalique résulte d'une multiplication de l'agent pathogène ou plus souvent d'une réaction inflammatoire.
La majorité des méningites et méningo-encéphalites aiguës sont infectieuses par contamination du LCS par un agent infectieux (le plus souvent une bactérie ou un virus). La contamination peut se faire par voie hématogène (le plus fréquemment), par contiguïté à partir des cavités ORL, ou plus rarement par inoculation directe (traumatisme, chirurgie). L'atteinte encéphalique résulte d'une multiplication de l'agent pathogène ou plus souvent d'une réaction inflammatoire.- Les abcès cérébraux sont rares (incidence de 1/100000/an). Il sont constitués d'une cavité purulente au sein du parenchyme cérébral entourée d'une importante zone d'œdème, réalisant un processus expansif. Il existe une phase d'encéphalite pré-suppurative caractérisée par un centre nécrotique avec réaction inflammatoire et présence de germe, entouré d'un œdème, suivie du stade d'abcès avec formation d'une capsule de gliose.
- Les localisations préférentielles par ordre de fréquence sont le lobe frontal (un tiers des cas), le lobe temporal (un quart des cas), et le lobe pariétal (un cinquième des cas).
- La porte d'entrée se fait le plus souvent à partir d'un foyer de contiguïté (infection ORL, ostéite crânienne, thrombose veineuse cérébrale, rarement méningite purulente), par voie hématogène (à partir d'un foyer dentaire, pulmonaire ou cardiaque), ou plus rarement dans les suites d'un traumatisme crânien avec brèche méningée ou d'une neurochirurgie.
II. Symptomatologie clinique
A. Syndrome méningé
 Un syndrome méningé est défini comme une symptomatologie en rapport avec une irritation des enveloppes méningées (arachnoïde et pie-mère), quelle qu'en soit l'origine. Il se caractérise par l'association inconstante de la triade céphalées, vomissements et raideur méningée.
Un syndrome méningé est défini comme une symptomatologie en rapport avec une irritation des enveloppes méningées (arachnoïde et pie-mère), quelle qu'en soit l'origine. Il se caractérise par l'association inconstante de la triade céphalées, vomissements et raideur méningée.
1. Céphalées
- Quasi constantes et précoces.
- Intenses, diffuses, continues avec paroxysmes possibles, mal soulagées par les antalgiques habituels.
- Exagérées par différents stimuli : mouvements de la tête, examen physique du patient, exposition à la lumière (photophobie) ou au bruit (phonophobie).
2. Vomissements
- Inconstants mais en général précoces.
- Spontanés, en jet, survenant sans effort.
- Pouvant être favorisés par les changements de position.
3. Raideur méningée
- Secondaire à une contracture des muscles paravertébraux en rapport avec la douleur provoquée par une irritation des méninges.
- Peut conduire à une attitude particulière du patient «en chien de fusil» : couché sur le côté, dos tourné à la lumière, tête en hyperextension vers l'arrière, membres semi-fléchis.
- Touche particulièrement la nuque :
- la flexion de la tête par l'examinateur entraîne une résistance invincible et douloureuse de la nuque;
- les manœuvres de rotation et de latéralité de la tête sont conservées mais augmentent la céphalée.
- Peut être mise en évidence à l'examen du patient couché sur le dos par :
- le signe de Brudzinski : flexion involontaire des membres inférieurs (cuisses sur le bassin et jambes sur les cuisses) à la flexion forcée antérieure de la nuque ;
- le signe de Kernig : impossibilité de s'asseoir sans fléchir les genoux et résistance douloureuse à l'extension complète de la jambe lorsque la cuisse est fléchie.
4. Autres signes accompagnateurs possibles
- Hyperesthésie cutanée diffuse.
- Réflexes tendineux vifs.

B. Syndrome encéphalitique
Il correspond aux manifestations cliniques en lien avec l'inflammation de l'encéphale et peut être présent de manière isolée (encéphalite) ou, le plus souvent, associé au syndrome méningé (méningo-encéphalite). Il peut comporter :
- troubles de la conscience de degré variable (de la simple somnolence au coma profond) ;
- syndrome confusionnel et troubles comportementaux;
- signes de focalisation : déficit moteur (mono- ou hémiplégie), paralysie d'un ou plusieurs nerfs crâniens, aphasie, mouvements anormaux (tremblement, myoclonies) ;
- crises épileptiques focales (sans ou avec troubles de la conscience) et généralisées, pouvant aller jusqu'à l'état de mal;
- troubles neurovégétatifs : irrégularité du pouls, de la pression artérielle et de la température, en faveur d'une souffrance du tronc cérébral.

C. Syndrome infectieux
Il associe de façon variable :
- fièvre, dont l'intensité varie en fonction du germe responsable, parfois associée à des frissons, sueurs et myalgies;
- signes d'une infection associée : pneumopathie, foyer ORL (otite, sinusite, mastoïdite, rhinopharyngite, angine), infection urinaire, atteinte digestive (diarrhées), éruption cutanée, atteinte cardiaque (endocardite, myocardite);
- un purpura vasculaire doit faire évoquer une méningite à méningocoque et représente une urgence vitale. Le tableau gravissime de purpura fulminans lié à une septicémie à méningocoque associe un purpura extensif ulcéro-nécrotique (purpura vasculaire dont les éléments s'étendent rapidement avec au moins un élément nécrotique ou ecchymotique supérieur à 3 mm de diamètre), un choc septique, une coagulation intravasculaire disséminée, et des hémorragies viscérales (par exemple, surrénalienne).
D. Signes cliniques de gravité
L'identification des critères cliniques de gravité est impérative.

E. Suspecter cliniquement un abcès cérébral
 Un abcès cérébral doit être suspecté devant un tableau subaigu s'installant sur 1 à 2 semaines associant à divers degrés un syndrome d'hypertension intracrânienne, une atteinte neurologique focale dépendant de la localisation, de la taille et du nombre de lésions (hémiparésie, troubles sensitifs, aphasie, hémianopsie latérale homonyme, troubles neurocognitifs en particulier sous-cortico-frontaux), et des crises épileptiques focales ou généralisées. La fièvre est inconstante (50 % des cas), de même que l'altération de l'état général.
Un abcès cérébral doit être suspecté devant un tableau subaigu s'installant sur 1 à 2 semaines associant à divers degrés un syndrome d'hypertension intracrânienne, une atteinte neurologique focale dépendant de la localisation, de la taille et du nombre de lésions (hémiparésie, troubles sensitifs, aphasie, hémianopsie latérale homonyme, troubles neurocognitifs en particulier sous-cortico-frontaux), et des crises épileptiques focales ou généralisées. La fièvre est inconstante (50 % des cas), de même que l'altération de l'état général.
Parfois le tableau clinique est plus progressif, réalisant une syndrome tumoral isolé évoluant en tache d'huile, ou au contraire d'installation brutale.
F. Particularités sémiologiques des méningites et méningo- encéphalites infectieuses chez le nourrisson et le sujet âgé
1. Chez le nourrisson
 Tableau diagnostique clinique plus difficile. Il doit être évoqué devant un enfant geignard, présentant des cris à la mobilisation (hyperesthésie cutanée), des modifications du comportement, une somnolence inhabituelle entrecoupée de périodes d'agitation, un refus répété du biberon, des convulsions fébriles même brèves et apparemment isolées. Une hypotonie axiale remplace souvent la raideur de nuque. Une tension anormale de la fontanelle peut être retrouvée.
Tableau diagnostique clinique plus difficile. Il doit être évoqué devant un enfant geignard, présentant des cris à la mobilisation (hyperesthésie cutanée), des modifications du comportement, une somnolence inhabituelle entrecoupée de périodes d'agitation, un refus répété du biberon, des convulsions fébriles même brèves et apparemment isolées. Une hypotonie axiale remplace souvent la raideur de nuque. Une tension anormale de la fontanelle peut être retrouvée.
2. Chez le sujet âgé
Les signes cliniques peuvent être plus frustes, avec un syndrome infectieux souvent au second plan. Les troubles du comportement et signes focaux peuvent dominer le tableau.

III. Examens complémentaires
A. Ponction lombaire
La ponction lombaire (PL) est l'examen clé permettant d'affirmer le diagnostic de méningite.
1. Conditions de réalisation
La PL doit être réalisée en urgence avant instauration d'une antibiothérapie dans la très grande majorité des cas.
- Certaines situations imposent la réalisation préalable d'une imagerie cérébrale en extrême urgence de façon à ne pas retarder la PL :
- signes de focalisation neurologique ou d'hypertension intracrânienne ;
- troubles de la conscience avec un score de Glasgow ≤ 11 ;
- crises épileptiques focales ou généralisées après l'âge de 5 ans ;
- crises épileptiques hémicorporelles avant l'âge de 5 ans.
- La réalisation de la ponction lombaire doit être précédée d'un bilan biologique :
- bilan d'hémostase : contre-indication habituelle en cas de TP < 50 % ou TCA ratio > 1,5 ;
- numération plaquettaire : contre-indication habituelle en cas de plaquettes < 50000/mm3.
- L'antibiothérapie probabiliste doit être commencée avant réalisation de la PL dans les cas suivants :
- purpura fulminans (le traitement doit être instauré au domicile du patient) ;
- prise en charge hospitalière ne pouvant pas être réalisée dans les 60 minutes, notamment si la réalisation d'une imagerie risque de retarder la mise en place d'une antibiothérapie.
Contre-indication à la ponction lombaire
- Anomalie de l'hémostase (spontanée ou induite par anticoagulants) ou thrombopénie. Attention aux anticoagulants oraux directs pour lesquels certains tests d'hémostase peuvent être pris à défaut.
- Signes cliniques d'engagement cérébral (mydriase unilatérale, hoquet, mouvements d'en- roulement, troubles ventilatoires) ou radiologiques, effet de masse à l'imagerie cérébrale notamment en cas d'abcès volumineux.
- Instabilité hémodynamique.
2. Technique et analyses
La PL est réalisée en conditions d'asepsie stricte à l'aide d'une aiguille au niveau du cul-de-sac lombaire au niveau de l'espace intervertébral L4-L5 ou de l'espace immédiatement sus ou sous-jacent, le malade étant en position assise, courbé en avant, ou bien couché sur le côté. Il faut privilégier l'usage d'aiguille atraumatique, afin de réduire le risque de syndrome post-PL. L'examen du liquide cérébrospinal (LCS) doit comporter :
- une inspection de l'aspect macroscopique du LCS (l'aspect normal est «eau de roche»);
- une analyse cytologique (globules rouges et blancs avec identification des polynucléaires neutrophiles et des lymphocytes);
- une analyse biochimique (protéinorachie, glycorachie, chlorurorachie, lactates) ;
- une analyse microbiologique (bactériologique) comportant un examen direct avec coloration de Gram, mise en culture et antibiogramme systématique en cas de culture positive ;
- des tubes supplémentaires doivent être prélevés pour analyses complémentaires guidées selon le contexte clinique : PCR dans le cadre d'une méningite ou méningo-encéphalite virale (herpès virus, VZV, entérovirus) ou bactérienne (méningocoque, pneumocoque, tuberculose), PCR universelle, antigènes solubles pneumococciques.
3. Limites et complications de la ponction lombaire
a. Limites
- Difficultés techniques pour réaliser la PL (scoliose, calcification du ligament inter-épineux, agitation du patient).
- PL blanche : absence d'écoulement du LCS lié à une déshydratation sévère ou une compression médullaire sus-jacente.
- PL traumatique avec LCS hémorragique.
b. Complications
- Décharge électrique dans un membre par contact avec une racine nerveuse.
- Hématome épidural rachidien avec risque de compression.
Syndrome post-PL
- Hypotension du LCS par écoulement lié à une brèche méningée.
- Se caractérise par une céphalée typiquement orthostatique (apparition dans les secondes ou minutes suivant la mise en position debout, amélioration significative voire disparition en position allongée), parfois associée à d'autres signes (vision floue, acouphènes non pulsatiles à type de sifflements, baisse d'acuité auditive, distorsion sonore, nausées et vomissements).
- Le diagnostic d'hypotension du LCS est clinique.
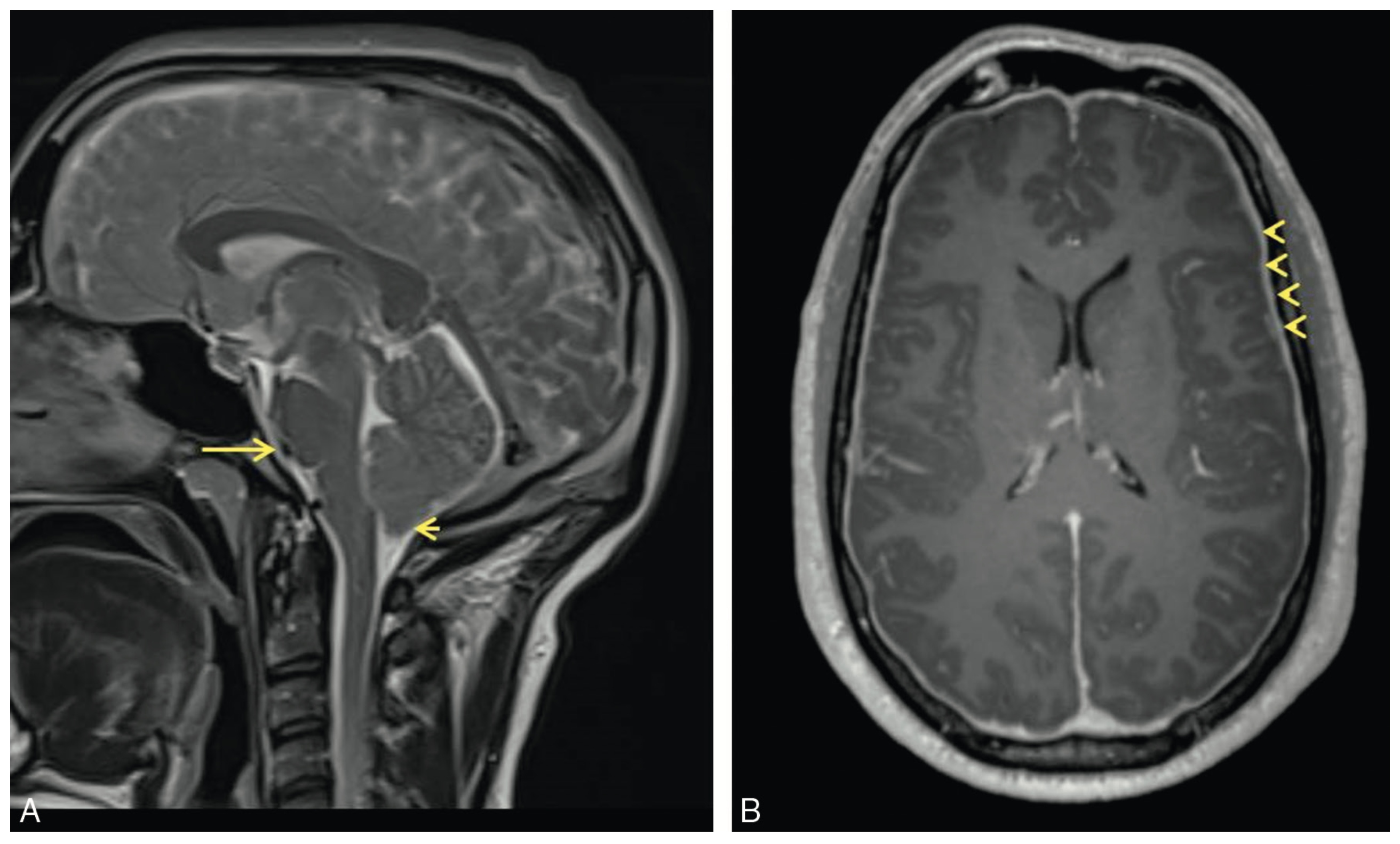
- L'IRM peut montrer des anomalies morphologiques en rapport avec le déplacement cranio-caudal de l'encéphale (aspect de ptose amygdalienne cérébelleuse, effacement des citernes prépontiques et chiasmatiques) et une prise de contraste diffuse et régulière des pachyméninges (figure 23.1).
- Le syndrome post-PL peut nécessiter la réalisation d'un blood patch épidural (injection de sang autologue dans l'espace épidural).
- Une hypotension du LCS prolongée non traitée peut se compliquer d'hématomes sous duraux bilatéraux et de thrombose veineuse cérébrale.
B. Imagerie cérébrale
Une imagerie cérébrale doit être réalisée :
- soit dans l'optique d'éliminer une contre-indication à la PL dans les situations décrites ci-dessus ;
- soit à visée étiologique en cas de signes encéphalitiques : dans ce cas, l'IRM cérébrale sans et avec injection de gadolinium doit être privilégiée du fait de sa meilleure sensibilité.
Fig. 23.1.  Patient présentant un syndrome post-PL avec hypotension du LCS.
Patient présentant un syndrome post-PL avec hypotension du LCS.
IRM cérébrale. A. Séquence T2 (coupe sagittale). B. Séquence T1 avec gadolinium (coupe axiale).
Effacement de la citerne prépontique (flèche longue), discrète ptose de l'amygdale cérébelleuse (flèche courte), prise de contraste diffuse et régulière des pachyméninges (têtes de flèches). (Source : CEN, 2021.)
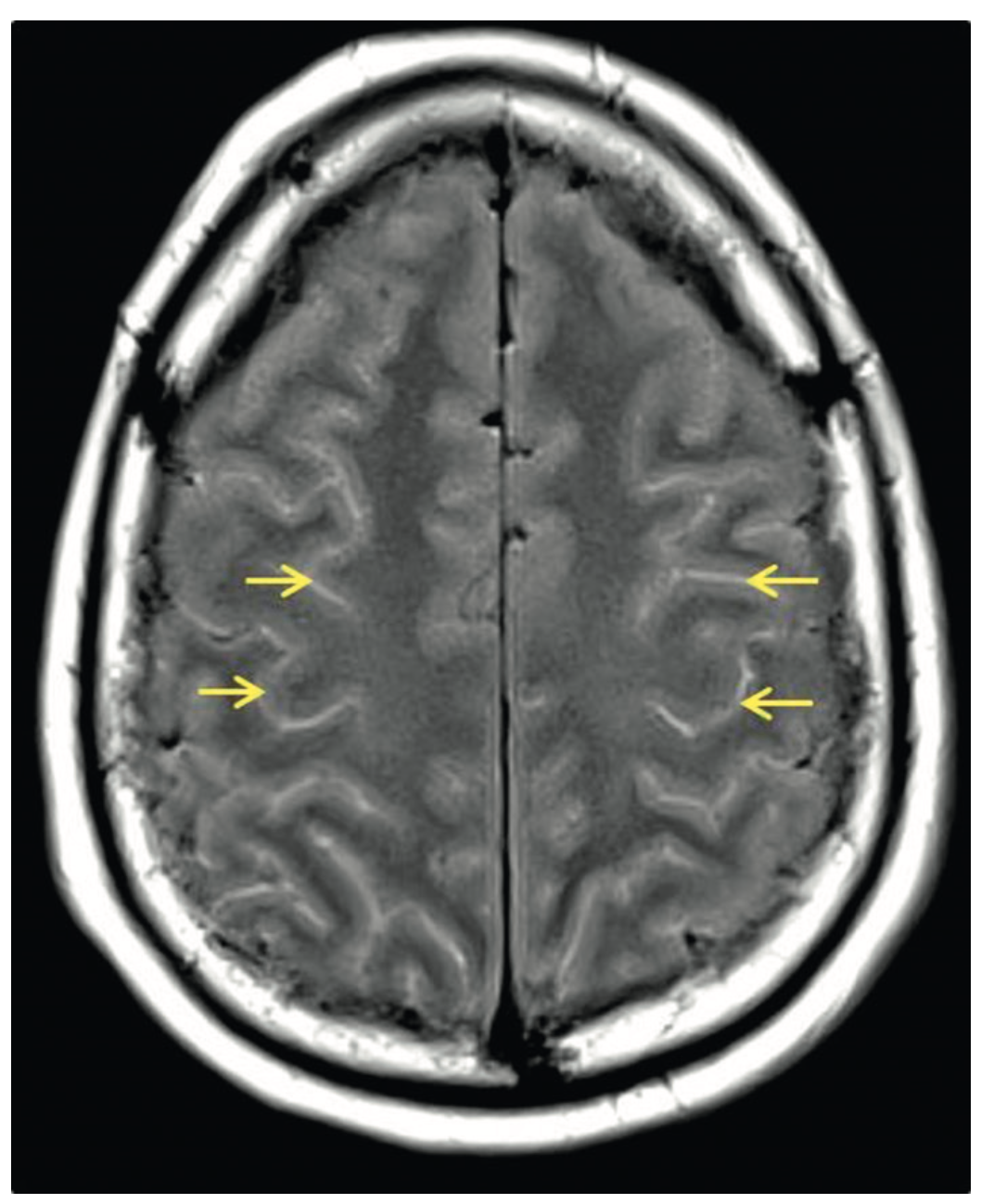
Elle peut montrer des lésions parenchymateuses en hypersignal T2 et T2-FLAIR, touchant volontiers les régions temporales et frontales, avec prise de contraste. Une méningite peut être visible sous forme d'hypersignaux diffus en séquences FLAIR au sein des sillons corticaux (figure 23.2) avec prise de contraste des leptoméninges en séquence T1 gadolinium. D'autres lésions peuvent être retrouvées en fonction du micro-organisme en cause. Néanmoins, une IRM normale n'élimine pas le diagnostic d'encéphalite ou de méningite. À défaut d'IRM, un scanner cérébral sans et avec injection de produit de contraste iodé doit être pratiqué.
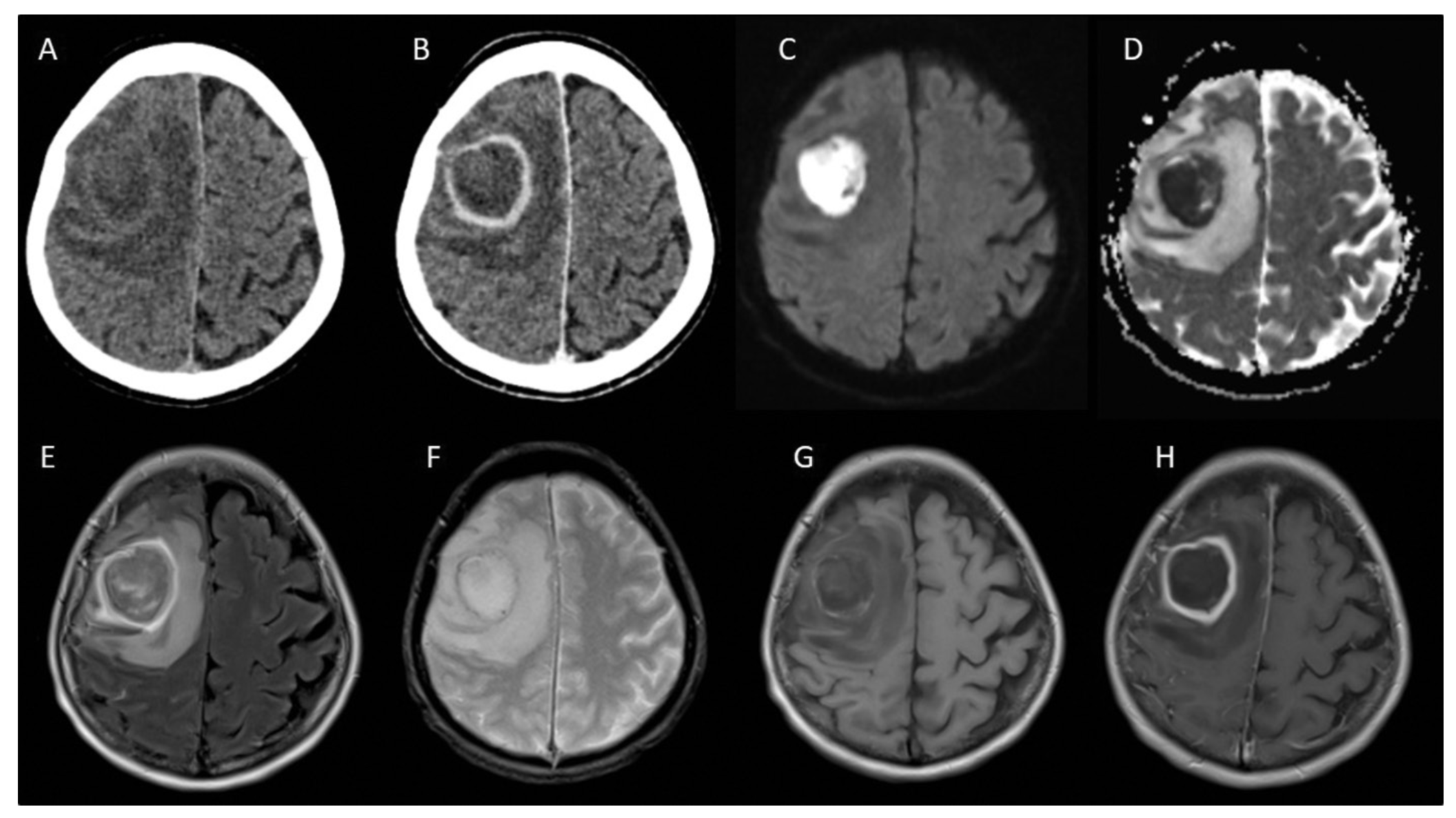
- À la recherche d'un abcès cérébral en cas de situation clinique évocatrice : le scanner cérébral avec injection de produit de contraste révèle une image en cocarde au stade d'abcès encapsulé (hypodensité arrondie entourée d'une prise de contraste annulaire avec œdème péri-lésionnel et effet de masse). En IRM la lésion comporte un centre en hyposignal en séquence T1, hypersignal en séquences T2, FLAIR et diffusion (avec coefficient apparent de diffusion [ADC] abaissé, en faveur d'une nécrose), entouré d'une capsule hyperintense en T2 et iso - ou hypo-intense en T1 prenant le contraste de façon marquée après injection de gadolinium (figure 23.3). Il existe un œdème prononcé sous forme d'hypersignal T2 et FLAIR autour de la lésion.
Fig. 23.2.  IRM cérébrale en séquence FLAIR montrant des hypersignaux diffus des sillons corticaux (flèches) chez un patient présentant une méningite à pneumocoque.
IRM cérébrale en séquence FLAIR montrant des hypersignaux diffus des sillons corticaux (flèches) chez un patient présentant une méningite à pneumocoque.
(Source : CEN, 2021.)
Fig. 23.3.  Scanner cérébral sans (A) et avec (B) injection de produit de contraste et IRM cérébrale en séquences diffusion (C), cartographie ADC (D), FLAIR (E), T2 écho de gradient (G) et T1 avec gadolinium (H), révélant un abcès cérébral frontal droit.
Scanner cérébral sans (A) et avec (B) injection de produit de contraste et IRM cérébrale en séquences diffusion (C), cartographie ADC (D), FLAIR (E), T2 écho de gradient (G) et T1 avec gadolinium (H), révélant un abcès cérébral frontal droit.
(Source : CEN, 2021.)

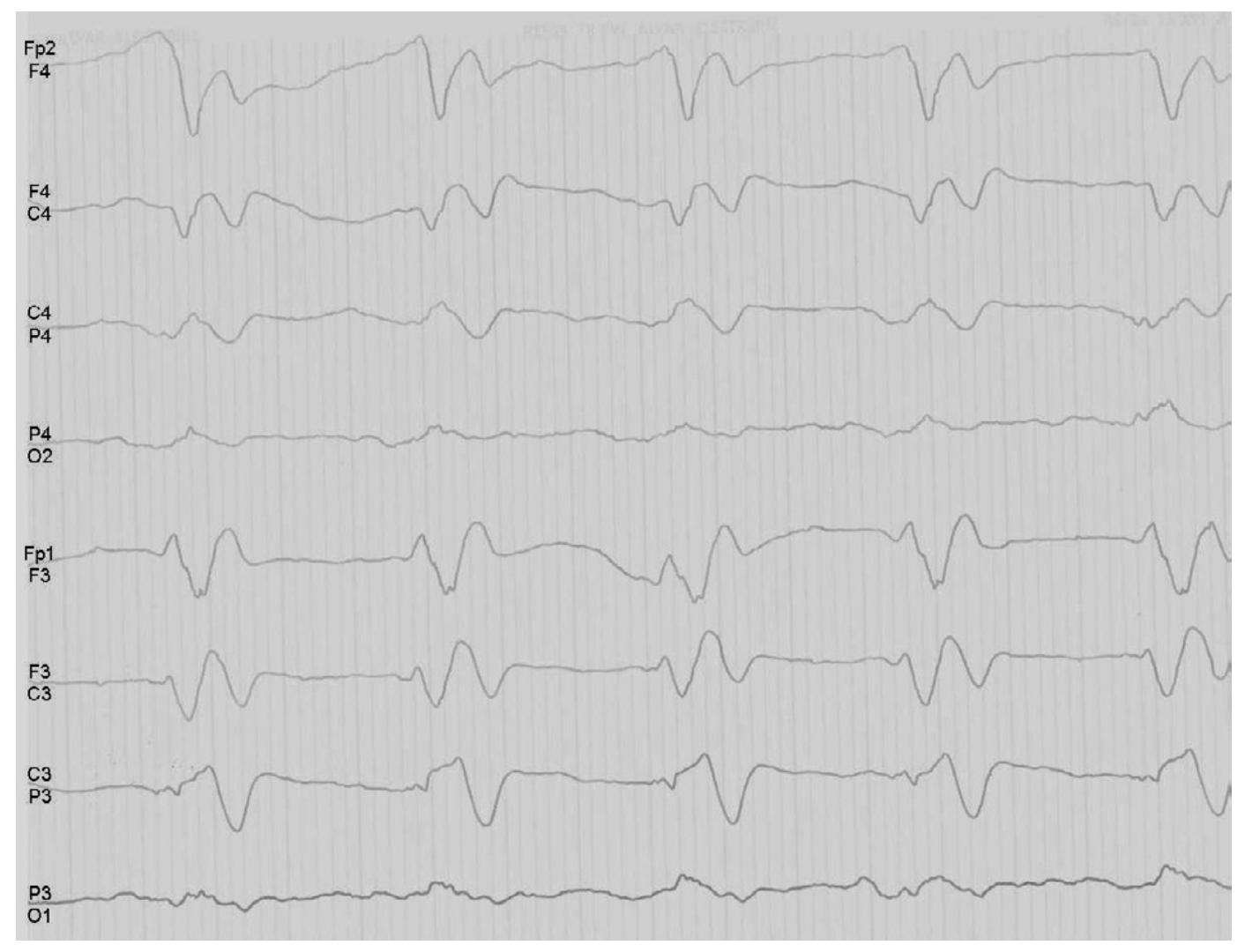
Fig. 23.4.  Électroencéphalogramme montrant un tracé lent avec ondes lentes périodiques diffuses en faveur d'une encéphalite.
Électroencéphalogramme montrant un tracé lent avec ondes lentes périodiques diffuses en faveur d'une encéphalite.
(Source : CEN, 2021.)
IV. Diagnostic étiologique
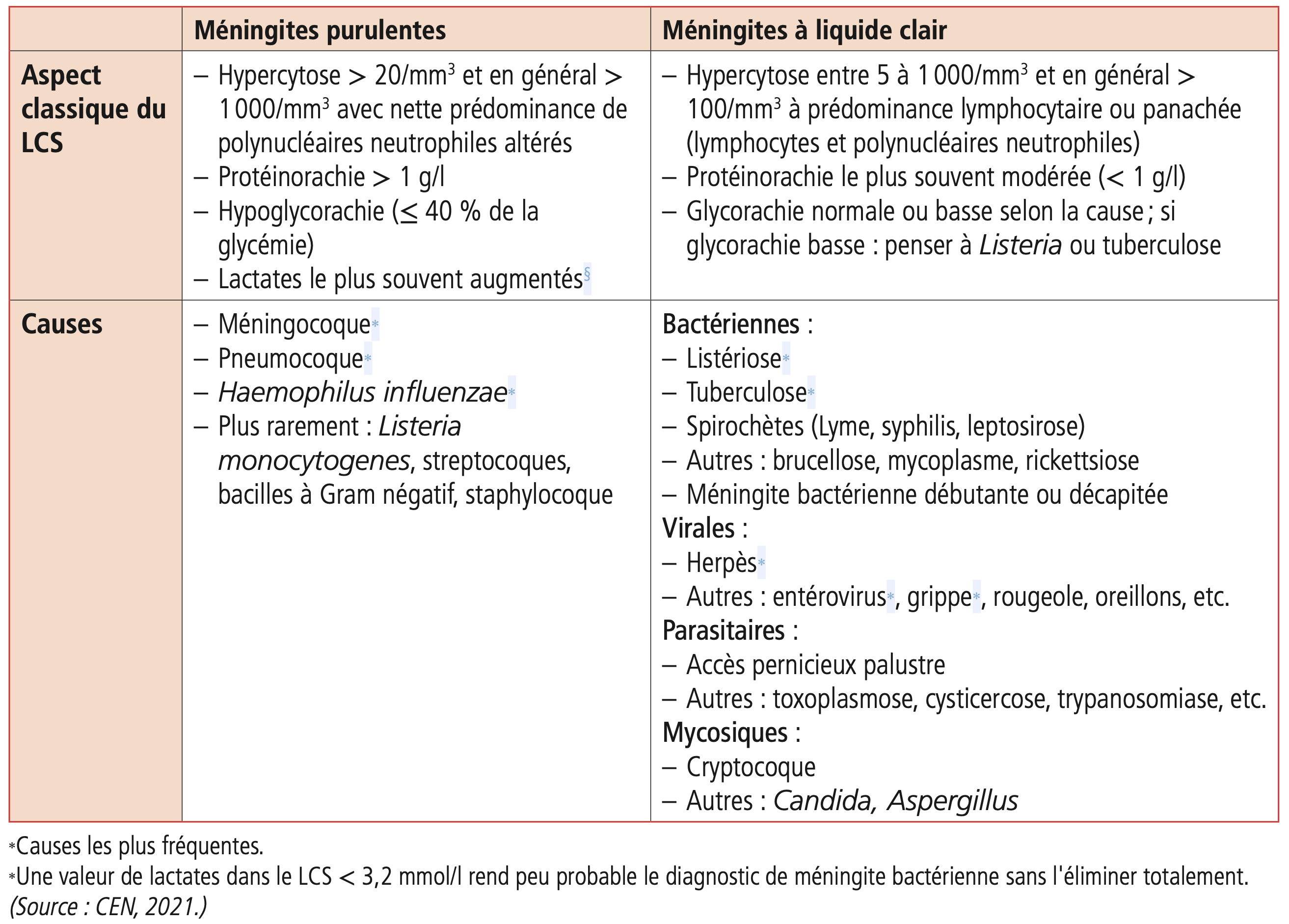
 Le diagnostic étiologique des méningites ou méningo-encéphalites est guidé par les résultats du LCS. L'aspect macroscopique et les données de l'analyse cytologique permettent la distinction entre méningite (ou méningo-encéphalite) purulente (bactérienne) et à liquide clair (bactériennes, virales, parasitaires ou fongiques) (tableau 23.1).
Le diagnostic étiologique des méningites ou méningo-encéphalites est guidé par les résultats du LCS. L'aspect macroscopique et les données de l'analyse cytologique permettent la distinction entre méningite (ou méningo-encéphalite) purulente (bactérienne) et à liquide clair (bactériennes, virales, parasitaires ou fongiques) (tableau 23.1).
A. Méningites et méningo-encéphalites bactériennes
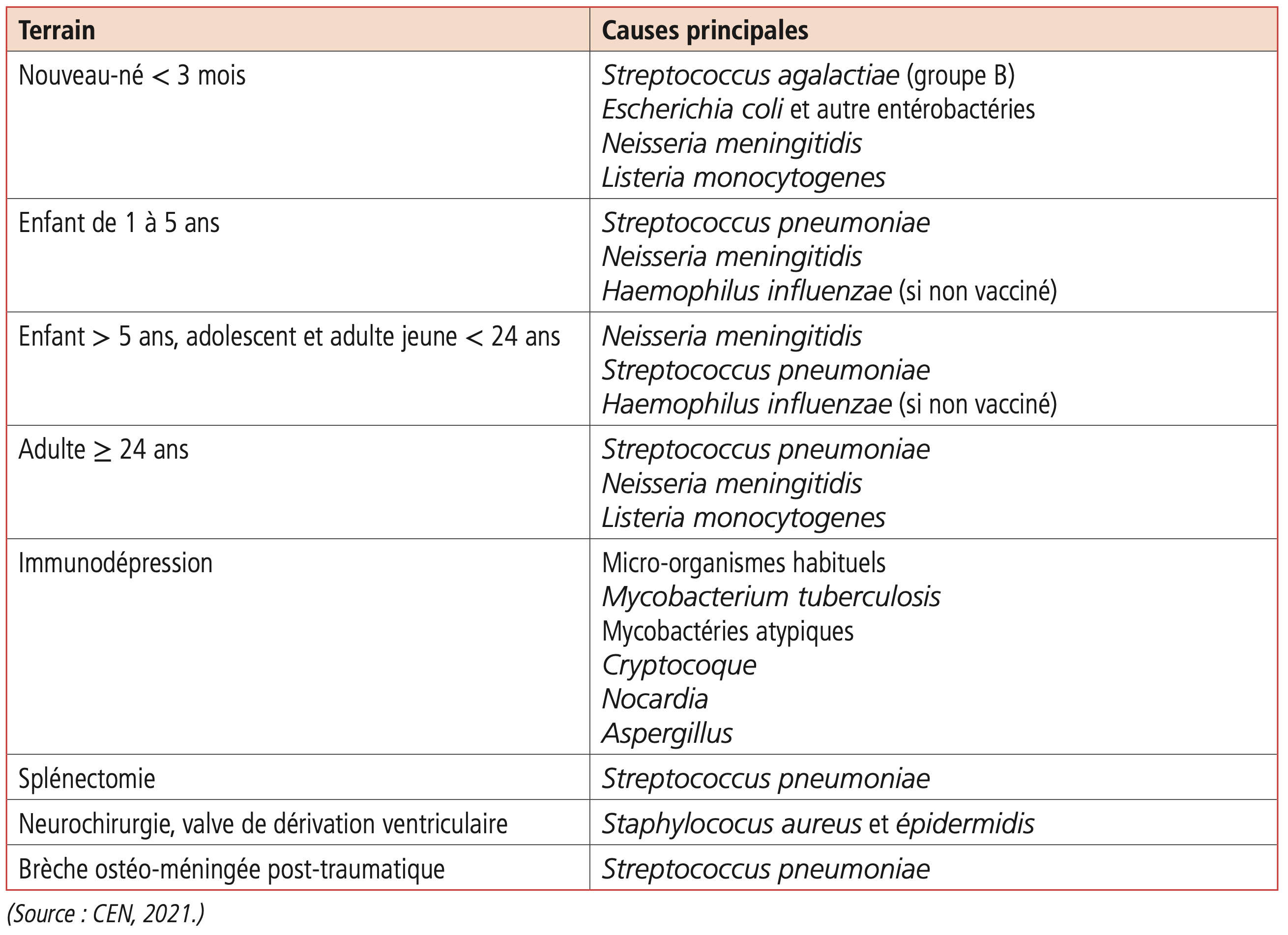
Les causes de méningites et méningo-encéphalites bactériennes varient en fonction du terrain du patient (âge et comorbidités) (tableau 23.2).
1. Méningites à méningocoque
- Deuxième cause la plus fréquente des méningites bactériennes chez l'adulte (environ 500 cas par an), mais première cause chez le jeune (15–24 ans).
- Neisseria meningitidis est un diplocoque à Gram négatif, aérobie.
- Transmission par voie aérienne.
- Se rencontrent à tout âge de façon sporadique ou épidémique, avec une recrudescence hivernale.
 Certains arguments cliniques peuvent orienter le diagnostic :
Certains arguments cliniques peuvent orienter le diagnostic :
- rhinopharyngite inaugurale;
- herpès nasolabial, arthralgies, injection conjonctivale;
- purpura pétéchial (membres, tronc, muqueuses);
 purpura extensif nécrotique (purpura fulminans des septicémies à méningocoque).
purpura extensif nécrotique (purpura fulminans des septicémies à méningocoque).
- LCS : le plus souvent, méningite purulente.
Tableau 23.1.  Principales causes de méningites ou méningo-encéphalites en fonction de l'aspect du LCS.
Principales causes de méningites ou méningo-encéphalites en fonction de l'aspect du LCS.
2. Méningites à pneumocoque
- Streptococcus pneumoniae est un diplocoque à Gram positif, encapsulé.
- Première cause de méningite bactérienne chez l'adulte (environ 700 cas/an) associée au pronostic le plus grave.
- Recrudescence hivernale.
- Peut survenir sur un terrain particulier :
- sujet âgé;
- pathologie chronique sous-jacente : diabète, éthylisme chronique, myélome ;
- immunodépression ;
- splénectomie.
- Peut résulter de :
- brèche ostéo-méningée post-traumatique (parfois ancienne);
- foyer infectieux de voisinage : pneumopathie, foyer ORL (sinusite, otite suppurée, mastoïdite).
 Une rhinorrhée ou des signes d'infection des voies aériennes peuvent accompagner le tableau clinique.
Une rhinorrhée ou des signes d'infection des voies aériennes peuvent accompagner le tableau clinique. LCS : le plus souvent, méningite purulente.
LCS : le plus souvent, méningite purulente.
Tableau 23.2.  Causes des méningites ou méningo-encéphalites bactériennes en fonction de l'âge et du terrain.
Causes des méningites ou méningo-encéphalites bactériennes en fonction de l'âge et du terrain.
3. Méningites à Haemophilus influenzae
- Haemophilus influenzae est un bacille à Gram négatif intra et extracellulaire.
- Première cause de méningite bactérienne chez le nourrisson et l'enfant de moins de 6 ans non vacciné.
 Peut s'accompagner d'une otite, épiglottite, arthrite ou pneumopathie.
Peut s'accompagner d'une otite, épiglottite, arthrite ou pneumopathie. LCS : le plus souvent, méningite purulente mais, parfois, une formule panachée peut être retrouvée.
LCS : le plus souvent, méningite purulente mais, parfois, une formule panachée peut être retrouvée.
4. Méningites et méningo-encéphalites à Listeria monocytogenes
- Listeria monocytogenes est un bacille à Gram positif intracellulaire facultatif.
- Transmission par voie digestive (notamment par consommation de produits laitiers crus).
- Une listériose neuroméningée est possible à tout âge mais doit être particulièrement évoquée dans certaines situations :
- sujet âgé;
- grossesse ;
- maladies chroniques : diabète, alcoolisme, cancer, cirrhose ;
- immunodépression : corticothérapie, chimiothérapie, greffe.
 Tableau clinique caractérisé par :
Tableau clinique caractérisé par :
- début progressif avec phase prodromale sur quelques jours associant fatigue, douleurs abdominales, nausées, vomissements, céphalées;
- syndrome méningé parfois fruste, avec fièvre inconstante ;
- tableau de rhombencéphalite par atteinte du tronc cérébral pouvant associer atteinte des nerfs crâniens (paralysie oculomotrice, paralysie faciale, troubles de la déglutition), syndrome cérébelleux, atteinte des voies longues, troubles de la vigilance, atteinte cardiorespiratoire.
 LCS : typiquement clair avec pléiocytose à prédominance lymphocytaire ou formule panachée, hyperprotéinorachie modérée, hypoglycorachie ou normoglycorachie ; plus rarement, aspect purulent.
LCS : typiquement clair avec pléiocytose à prédominance lymphocytaire ou formule panachée, hyperprotéinorachie modérée, hypoglycorachie ou normoglycorachie ; plus rarement, aspect purulent.
5. Méningites et méningo-encéphalites tuberculeuses
- La tuberculose neuroméningée peut survenir lors de la dissémination faisant suite à une primo-infection tuberculeuse ou à distance de celle-ci à partir d'une autre localisation.
- Diagnostic difficile, souvent retardé.
- Doit être évoqué notamment si :
- sujet originaire d'une zone d'endémie;
- absence de vaccination par le BCG;
- immunodépression ;
- notion de contage;
- tuberculose-maladie autre associée (pulmonaire ou extrapulmonaire...).
 Tableau clinique :
Tableau clinique :
- début progressif sur plusieurs jours ou semaines associant fièvre modérée, sueurs, altération de l'état général avec anorexie et amaigrissement, céphalées progressives, troubles psychiques (irritabilité, insomnie, troubles cognitifs);
- signes méningés souvent au second plan;
- méningite basilaire (atteinte des méninges de la base du cerveau) souvent rencontrée et associant :
- atteinte des nerfs crâniens : paralysie oculomotrice, paralysie faciale ;
- troubles neurovégétatifs : anomalies du rythme respiratoire, irrégularité du pouls et de la pression artérielle;
- troubles de la vigilance;
- signes de focalisation par atteinte d'autres structures du système nerveux central possibles : arachnoïdite, épidurite, infarctus localisé, hydrocéphalie.
 LCS : typiquement clair (parfois trouble) avec pléiocytose à prédominance lymphocytaire, hyperprotéinorachie dépassant souvent 1 g/l, hypoglycorachie constante sauf au début de l'évolution. Diagnostic posé sur la positivité de la culture du LCS sur milieu solide de Löwenstein ou sur milieu liquide (plus rapide) ou par PCR.
LCS : typiquement clair (parfois trouble) avec pléiocytose à prédominance lymphocytaire, hyperprotéinorachie dépassant souvent 1 g/l, hypoglycorachie constante sauf au début de l'évolution. Diagnostic posé sur la positivité de la culture du LCS sur milieu solide de Löwenstein ou sur milieu liquide (plus rapide) ou par PCR. L'imagerie cérébrale peut montrer une prise de contraste méningée à la base du cerveau, des tuberculomes ou des infarctus cérébraux témoignant d'une angéite cérébrale.
L'imagerie cérébrale peut montrer une prise de contraste méningée à la base du cerveau, des tuberculomes ou des infarctus cérébraux témoignant d'une angéite cérébrale. D'autres localisations tuberculeuses doivent être recherchées, pulmonaires et extrapulmonaires (notamment ophtalmique, péricardique, urogénitale, hépatique, par exemple).
D'autres localisations tuberculeuses doivent être recherchées, pulmonaires et extrapulmonaires (notamment ophtalmique, péricardique, urogénitale, hépatique, par exemple).
6. Causes plus rares de méningites et méningo-encéphalites de présentation subaiguë ou chronique
a. Maladie de Lyme
- Secondaire à une infection par Borrelia burgdorferi, un spirochète transmis par piqûre de tique en zone d'endémie, survenant en phase secondaire de la maladie, plusieurs semaines ou mois après un contage.
 Un antécédent d'érythème chronique migrateur doit être recherché à l'interrogatoire du patient, de même que d'autres manifestations de la phase secondaire : arthrites, atteinte cardiaque (bloc auriculoventriculaire, péricardite).
Un antécédent d'érythème chronique migrateur doit être recherché à l'interrogatoire du patient, de même que d'autres manifestations de la phase secondaire : arthrites, atteinte cardiaque (bloc auriculoventriculaire, péricardite).- Tableau clinique : comporte classiquement une atteinte pluriradiculaire très douloureuse associée à la méningite (méningo-encéphalite) avec possible paralysie des nerfs crâniens, en particulier le nerf facial (la maladie de Lyme est une cause de paralysie faciale périphérique bilatérale).
 LCS : typiquement clair avec pléiocytose à prédominance lymphocytaire, hyperprotéinorachie, normoglycorachie.
LCS : typiquement clair avec pléiocytose à prédominance lymphocytaire, hyperprotéinorachie, normoglycorachie.- Une sérologie dans le sang et LCS doit être réalisée.
b. Syphilis
- Les méningites aiguës à Treponema pallidum se rencontrent au cours de la phase secondaire ou tertiaire de la maladie.
 Peuvent entrer dans le cadre d'un neurosyphilis associant diverses atteintes neurologiques : méningite chronique, atteinte des nerfs crâniens (paralysie oculomotrice, atteinte du nerf optique ou auditif), signe d'Argyll-Robertson (abolition du réflexe photomoteur avec conservation de la contraction pupillaire à l'accommodation-convergence), tabès, infarctus cérébraux par angéite, démence frontale avec mégalomanie (appelée paralysie générale).
Peuvent entrer dans le cadre d'un neurosyphilis associant diverses atteintes neurologiques : méningite chronique, atteinte des nerfs crâniens (paralysie oculomotrice, atteinte du nerf optique ou auditif), signe d'Argyll-Robertson (abolition du réflexe photomoteur avec conservation de la contraction pupillaire à l'accommodation-convergence), tabès, infarctus cérébraux par angéite, démence frontale avec mégalomanie (appelée paralysie générale). LCS : typiquement clair avec pléiocytose à prédominance lymphocytaire, hyperprotéinorachie, normoglycorachie.
LCS : typiquement clair avec pléiocytose à prédominance lymphocytaire, hyperprotéinorachie, normoglycorachie.- Diagnostic : positivité de la sérologie (VDRL, TPHA, FTA) dans le sang et dans le LCS (même si inconstamment positive à ce niveau-là).
7. Autres méningites et méningo-encéphalites bactériennes
Le diagnostic sera évoqué en fonction du contexte et des atteintes extra-neurologiques associées. Parmi les bactéries incriminées, on retrouve :
- leptospirose ;
- brucellose ;
- bactéries intracellulaires : mycoplasme, Chlamydia, Legionella, Coxiella burnetii, Rickettsia.
B. Méningites et méningo-encéphalites virales
1. Méningo-encéphalite herpétique

- Due à une réplication de l'herpes simplex virus de type 1 (HSV-1, 95 % des cas) ou de type 2 (HSV-2, 5 % des cas, avec habituellement un tableau de méningite sans note encéphalitique) quiescent dans les ganglions nerveux céphaliques.
- Survient à tout âge (âge moyen : 40 ans).
- Symptomatologie clinique associant à divers degrés :
- début rapide à type de syndrome grippal, asthénie, altération de l'état général;
- syndrome infectieux avec fièvre quasi constante, souvent élevée ;
- syndrome méningé plus inconstant, parfois limité aux céphalées ;
- syndrome encéphalitique :
- syndrome confusionnel avec troubles du comportement (agitation, agressivité),
- troubles mnésiques antérogrades marqués (oubli à mesure),
- troubles de la vigilance fluctuants, pouvant aller jusqu'au coma,
- crises épileptiques partielles simples ou complexes (illusions, hallucinations olfactives, gustatives ou auditives, crises végétatives) avec ou sans généralisation secondaire ou d'emblée généralisées,
- troubles du langage : aphasie de Wernicke,
- plus rarement, atteinte du champ visuel (quadranospie supérieure) ou motrice (hémiparésie dans les formes graves nécrotiques ou œdémateuses).

- L'étude du LCS permet le diagnostic positif :
- typiquement clair avec pléiocytose à prédominance lymphocytaire (souvent < 500/mm3), hyperprotéinorachie généralement modérée (< 1 g/l), normoglycorachie;
- du fait de la nécrose associée, un aspect faiblement hémorragique peut être retrouvé (10 à 1000 hématies/mm3);
- dans les formes encéphalitiques pures, l'hypercytose peut être discrète et la protéinorachie légèrement augmentée;
- dans les formes débutantes, le LCS peut être normal ;
- la recherche dans le LCS d'une réplication virale de HSV par technique PCR est systématique. Elle peut être négative au début de la maladie (jusqu'à 4 jours) et doit être renouvelée en cas de suspicion clinique.

- L'apport des autres examens biologiques est plus limité :
- la recherche d'antigènes herpétiques sanguins peut être positive très précocement mais la technique est peu sensible;
- les anticorps (IgM) dans le sang et le LCS sont très spécifiques mais la positivité est tardive (environ 8 jours).
- D'autres examens complémentaires peuvent aider au diagnostic :
- imagerie cérébrale :
- IRM cérébrale : elle peut montrer des hypersignaux sur les séquences T2 et FLAIR, principalement localisés au niveau des lobes temporaux (topographie antérieure évoluant vers la région moyenne et médiale) et des régions frontales orbitaires, le plus souvent bilatéraux mais asymétriques, avec prise de contraste sur la séquence T1 au gadolinium (figure 23.5). L'évolution vers une atrophie des noyaux amygdaliens et de l'hippocampe est souvent retrouvée,
- scanner cérébral : moins sensible que l'IRM, il peut mettre en évidence une hypodensité avec œdème et prise de contraste gyriforme de ces mêmes régions,
- l'imagerie cérébrale peut retrouver un effet de masse avec signes d'engagement cérébral dans les formes graves;
- EEG : il peut montrer des ondes lentes séparées par d'intervalles réguliers prenant un
aspect pseudo-périodique ou périodique, ainsi que des pointes ou pointes-ondes. Les
anomalies prédominent dans les régions temporales et frontales.
- imagerie cérébrale :
2. Autres méningites virales

 Principaux virus en cause connus :
Principaux virus en cause connus :
- entérovirus : coxsackies A et B, echovirus, poliovirus ;
- myxovirus et paramyxovirus : grippe, rougeole, oreillons ;
- virus du groupe herpès : VZV (à évoquer devant vésicules cutanées, atteinte d'un nerf crânien ou signes de vasculopathie à l'imagerie cérébrale), EBV, CMV, HHV-6 ;
- arbovirus : tick-borne encephalitis, fièvre de la vallée du Rift, West-Nile, encéphalite japonaise ;
- primo-infection par le VIH (cf. chapitre 24, item 169).
- LCS : clair avec pléiocytose à prédominance lymphocytaire, hyperprotéinorachie modérée (< 1 g/l), normoglycorachie. L'identification du virus par PCR a peu d'intérêt du fait de l'absence de sanction thérapeutique, à l'exception du VIH et du VZV en cas d'encéphalite associée.
- L'évolution est favorable en quelques jours.
Fig. 23.5.  IRM cérébrale en séquence FLAIR chez un patient présentant une méningo-encéphalite herpétique.
IRM cérébrale en séquence FLAIR chez un patient présentant une méningo-encéphalite herpétique.
Hypersignal franc des régions antérieure et médiale du lobe temporal droit, avec atteinte plus subtile de la région médiale du lobe temporal gauche. (Source : CEN, 2021.)
C. Abcès cérébraux
 Les agents infectieux impliqués dans les abcès cérébraux dépendent de la porte d'entrée. Chez le patient immunocompétent, les bactéries les plus fréquemment retrouvées sont :
Les agents infectieux impliqués dans les abcès cérébraux dépendent de la porte d'entrée. Chez le patient immunocompétent, les bactéries les plus fréquemment retrouvées sont :
- en cas de porte d'entrée ORL et dentaire : streptocoques oraux et du groupe milleri (S. anginosus, S. constellatus et S. intermedius), anaérobies. La flore est souvent polymicrobienne ;
- en cas de porte d'entrée hématogène : S. aureus, Listeria (abcès cérébelleux et du tronc cérébral), Mycobacterium tuberculosis;
- en post-traumatique et post-neurochirurgical : S. aureus, entérobactéries, P. aeruginosa. Chez le patient immunodéprimé, d'autres agents peuvent être en cause : toxoplasmose cérébrale, nocardioses, champignons (Aspergillus, cryptocoques, Candida).


V. Prise en charge thérapeutique
A. Mesures générales
 En urgence en milieu hospitalier dans une unité ayant l'expérience de la prise en charge, et si possible avec une unité de surveillance continue.
En urgence en milieu hospitalier dans une unité ayant l'expérience de la prise en charge, et si possible avec une unité de surveillance continue.- Mesures d'isolement infectieux en attente du diagnostic bactériologique.
- Le traitement symptomatique comporte :
- antipyrétiques ;
- antalgiques ;
- correction des troubles hydroélectrolytiques;
- traitement antiépileptique si crise épileptique.

B. Traitement et évolution des méningites et méningo- encéphalites bactériennes
1. Antibiothérapie
- L'antibiothérapie est guidée par les résultats initiaux de l'analyse du LCS (tableau 23.3). Outre les situations imposant de débuter le traitement avant la réalisation de la ponction lombaire (cf. supra), l'antibiothérapie doit être administrée avant d'obtenir les premiers résultats du LCS en cas d'aspect trouble de ce dernier.
- En cas d'examen direct négatif et méningite purulente :
- en l'absence d'argument clinique pour une listériose, le traitement antibiotique doit comporter céfotaxime ou ceftriaxone par voie IV, en association avec gentamicine chez les nourrissons de moins de 3 mois ;
- en présence d'arguments cliniques pour une listériose, le traitement antibiotique doit comporter céfotaxime ou ceftriaxone par voie IV, en association avec amoxicilline et gentamicine.
- L'adaptation et la durée totale du traitement sont définies après documentation micro- biologique (tableau 23.3). Lorsque aucune documentation microbiologique n'a pu être obtenue et que le diagnostic de méningite bactérienne reste envisagé, l'antibiothérapie initiale est maintenue à l'identique pour une durée de 14 jours.
 Les autres causes bactériennes nécessitent un traitement spécifique :
Les autres causes bactériennes nécessitent un traitement spécifique :
- méningite tuberculeuse : quadrithérapie rifampicine, isoniazide, pyrazinamide et éthambutol pendant 2 mois, puis bithérapie rifampicine et isoniazide pendant 7 à 10 mois ;
- maladie de Lyme : ceftriaxone par voie IV pendant 3 à 4 semaines ;
- syphilis : pénicilline G par voie IV pendant 2 à 3 semaines.
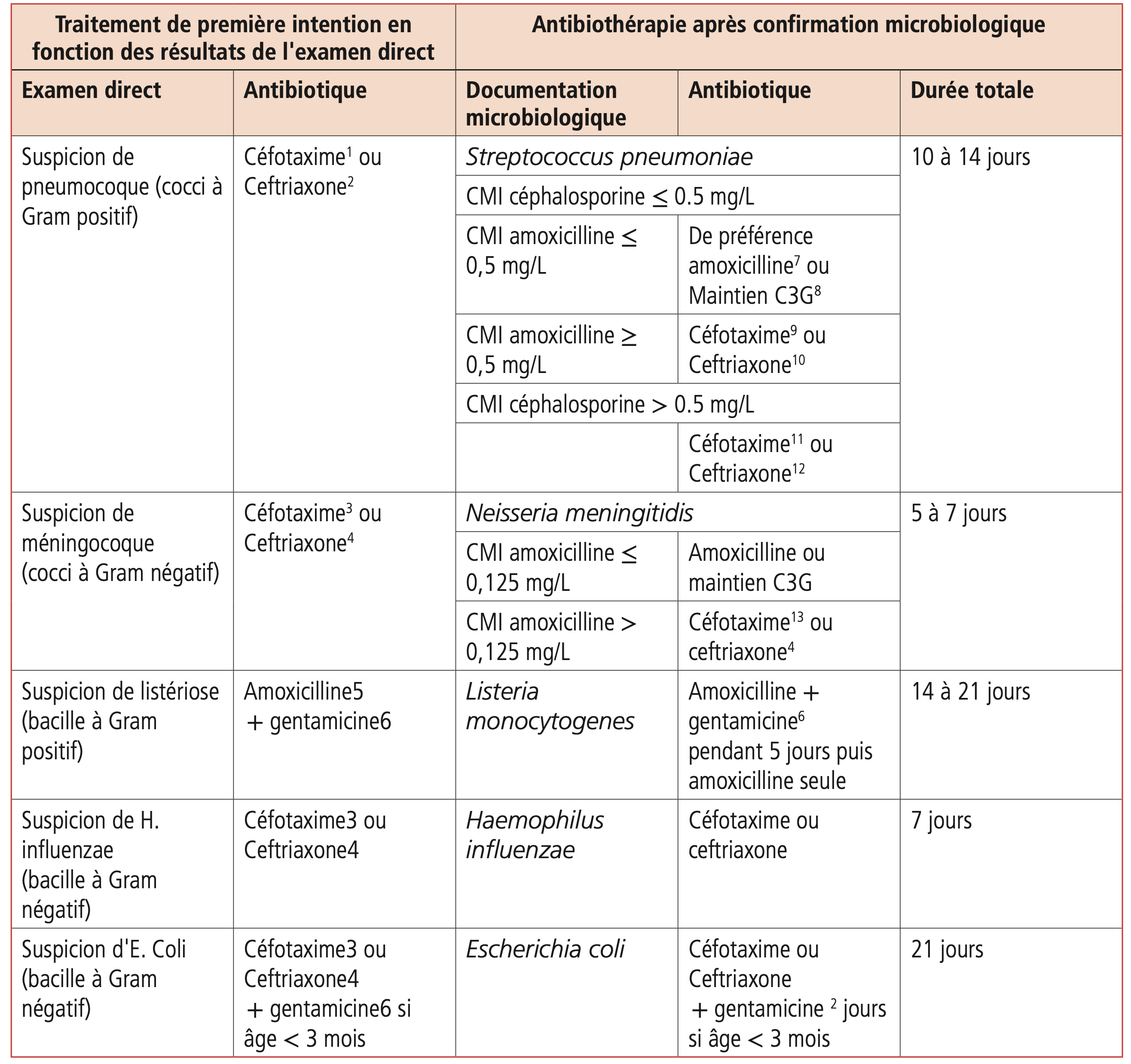
Tableau 23.3.  Choix de l'antibiothérapie de première intention en cas d'examen direct positif et après documentation microbiologique des méningites bactériennes aiguës en fonction des données du LCS.
Choix de l'antibiothérapie de première intention en cas d'examen direct positif et après documentation microbiologique des méningites bactériennes aiguës en fonction des données du LCS.
CMI : concentration minimal inhibitrice.
1. 300 mg/kg par jour en IV, soit en 4 perfusions, soit en administration continue avec dose de charge de 50 mg/kg sur 1 heure. 2. 100 mg/kg par jour en IV, en 1 ou 2 perfusions. 3. 200 mg/kg par jour en IV, soit en 4 perfusions, soit en administration continue avec dose de charge de 50 mg/kg sur 1 heure. 4. 75 mg/kg par jour en IV, en 1 ou 2 perfusions. 5. 200 mg/kg par jour en IV, soit en 4 perfusions, soit en administration continue. 6. 5 mg/kg en IV, en 1 perfusion unique journalière. 7. 200 mg/kg par jour soit en 4 à 6 perfusions, soit en administration continue. 8. Diminuer la dose de céfotaxime à 200 mg/kg par jour en IV et de ceftriaxone à 75 mg/kg par jour en IV 9. 200 mg/kg par jour en IV. 10. 75 mg/kg par jour en IV. 11. 300 mg/kg par jour en IV. 12. 100 mg/kg par jour en IV. 13. 200 mg/kg par jour en IV, soit en 4 à 6 perfusions, soit en administration continue.
(Source : CEN, 2021.)
2. Corticothérapie
 La dexaméthasone a une action anti-inflammatoire et son bénéfice est d'autant plus marqué si elle est administrée avant l'antibiothérapie.
La dexaméthasone a une action anti-inflammatoire et son bénéfice est d'autant plus marqué si elle est administrée avant l'antibiothérapie.- Les indications sont :
- diagnostic microbiologique chez l'adulte de méningite à pneumocoque ou à méningocoque ;
- diagnostic microbiologique chez l'enfant ou le nourrisson de méningite à pneumo-coque ou à H. influenzae;
- diagnostic présumé de méningite bactérienne sans certitude microbiologique mais décision de traitement probabiliste par antibiotique chez l'adulte et chez le nourrisson de 3 à 12 mois. Il s'agit des cas suivants :
- indication d'une imagerie cérébrale, qui retarde de facto la réalisation de la ponction lombaire,
- LCS trouble,
- examen direct du LCS négatif, mais les données fournies par les autres examens biologiques du LCS et du sang permettent de retenir le diagnostic de méningite bactérienne.
- Concernant ces dernières situations, il faut noter que si le diagnostic finalement retenu ne correspond pas aux indications de la corticothérapie, celle-ci doit être arrêtée. Elle est contre-indiquée en cas d'immunodépression. Elle ne doit pas être utilisée en cas de forte suspicion de listériose neuroméningée.
- Modalités d'administration : dose unitaire de 10 mg chez l'adulte et 0,15 mg/kg chez l'enfant, injection intraveineuse toutes les 6 heures pendant 4 jours, première injection immédiatement avant ou de façon concomitante à la première injection d'antibiotique

3. Mesures associées
- Méningite à pneumocoque ou Haemophilus influenzae : recherche et prise en charge spécifique d'un foyer infectieux pulmonaire ou ORL.
- Méningite à pneumocoque : scanner à la recherche d'une brèche ostéoméningée, en particulier en cas d'antécédent de traumatisme crânien, d'intervention neurochirurgicale ou ORL, d'otorrhée ou de rhinorrhée de LCS, ou de méningites bactériennes récidivantes.
- Méningite à méningocoque : déclaration obligatoire au médecin inspecteur de santé publique de l'agence régionale de santé (ARS) afin d'organiser l'antibioprophylaxie et la vaccination éventuelle des contacts du patient.
- Méningite tuberculeuse : déclaration obligatoire.
- Méningite à pneumocoque chez l'enfant : suivi audiométrique.

4. Mesures préventives
 Prévention autour d'un cas dans les méningites à méningocoque (instruction no DGS/ RI1/DUS/2014/301 du 24 octobre 2014 relative à la prophylaxie des infections invasives à méningocoque) (cf «Sites internet») :
Prévention autour d'un cas dans les méningites à méningocoque (instruction no DGS/ RI1/DUS/2014/301 du 24 octobre 2014 relative à la prophylaxie des infections invasives à méningocoque) (cf «Sites internet») :
- antibioprophylaxie en urgence chez les sujets en contact proche ou répété (sécrétions rhinopharyngées) dans les 10 jours précédant l'hospitalisation (doses ci-dessous données pour adulte) :
- 1. rifampicine (600 mg, 2 fois par jour, pendant 2 jours, voie orale),
- 2. ou si allergie, ciprofloxacine (500 mg en dose unique, voie orale),
- 3. ou ceftriaxone (250 mg en dose unique, voie injectable) ;
- vaccination en complément de l'antibioprophylaxie aux contacts qui se retrouvent de manière régulière et répétée dans l'entourage proche du cas-index, c'est-à-dire sa communauté de vie (sujets vivant sous le même toit, amis, voisins de classe).
- antibioprophylaxie en urgence chez les sujets en contact proche ou répété (sécrétions rhinopharyngées) dans les 10 jours précédant l'hospitalisation (doses ci-dessous données pour adulte) :
- Prévention des méningites à pneumocoque des sujets à risque : elle repose sur la vaccination des sujets à haut risque : asplénie fonctionnelle ou splénectomie, drépanocytose homozygote, infection à VIH, syndrome néphrotique, insuffisance respiratoire, insuffisance cardiaque, alcoolisme ou hépatopathie chronique, antécédents d'infection pulmonaire ou invasive à pneumocoque, immunosuppression.
C. Traitement et évolution des méningites et méningo-encéphalites virales
 Le traitement de la méningo-encéphalite herpétique est une urgence. Il doit être commencé avant d'obtenir les résultats de la recherche PCR. Il repose sur l'aciclovir IV (10 mg/kg toutes les 8 heures) pendant 21 jours. L'aciclovir doit être administré en perfusion lente et associé à une bonne hydratation, afin de limiter le risque d'insuffisance rénale aiguë par tubulopathie obstructive (cristaux d'aciclovir intra-tubulaires).
Le traitement de la méningo-encéphalite herpétique est une urgence. Il doit être commencé avant d'obtenir les résultats de la recherche PCR. Il repose sur l'aciclovir IV (10 mg/kg toutes les 8 heures) pendant 21 jours. L'aciclovir doit être administré en perfusion lente et associé à une bonne hydratation, afin de limiter le risque d'insuffisance rénale aiguë par tubulopathie obstructive (cristaux d'aciclovir intra-tubulaires).- Le traitement de l'encéphalite zostérienne (VZV) est identique à celui de l'encéphalite herpétique mais avec une dose d'aciclovir plus élevée (15 mg/kg en IV toutes les 8 heures).
- Les autres méningites virales requièrent un simple traitement symptomatique.

Site internet
Instruction No DGS/RI1/DUS/2014/301 du 24 octobre 2014 relative à la prophylaxie des infections invasives à méningocoque.
Mise à jour 2018 de la 17e Conférence de consensus en thérapeutique anti-infectieuse du 19 novembre 2008 : « Prise en charge des méningites bactériennes aiguës communautaires (à l'exclusion du nouveau- né) ». https://www.em-consulte.com/showarticle-file/1312343/main.pdf.
SPILF 2017 : « Recommandations de prise en charge des encéphalites infectieuses de l'adulte». https://www. em-consulte.com/showarticlefile/1121241/main.pdf.