Tatiana Horowitz et Éric Guedj
Principes
La médecine nucléaire repose sur l'administration de produits radioactifs pour :
- visualiser le fonctionnement des tissus ou organes par imagerie moléculaire ;
- traiter des pathologies essentiellement cancéreuses par radiothérapie interne vectorisée.
Ces produits radioactifs sont le plus souvent injectés par voie intraveineuse, ce sont des médicaments radiopharmaceutiques. Ils sont faiblement ionisants dans les indications diagnostiques. Ils correspondent à des radiotraceurs (figure 23.1) :
- le traceur fait référence à la molécule ciblant le processus biologique/moléculaire que l'on veut étudier : par exemple du sucre pour l'étude du métabolisme glucidique, les transporteurs de la dopamine pour la neurotransmission dopaminergique, etc. ;
- le suffixe radio correspond à l'isotope radioactif détecté par la caméra de médecine nucléaire transformant le signal en image quantifiée ; par exemple le fluor 18 ou l'iode 123 en fonction des caractéristiques chimiques du traceur.

Figure 23.1
Radiotraceur.
Le radiotraceur est composé d'un traceur qui permet de cibler le processus biologique que l'on souhaite étudier sur un plan moléculaire, et d'une partie radioactive, l'isotope, qui émet le signal physique que la caméra détecte et transforme en image quantifiée.
Le caractère fonctionnel de cette imagerie moléculaire est complémentaire d'autres modalités d'imagerie apportant des informations plus anatomiques ou structurales, comme la TDM ou l'IRM.
Il existe deux techniques d'imagerie en médecine nucléaire, selon le type de radioactivité détectée :
- la tomographie par émission de positons (TEP), pour détecter les positons, par exemple du fluor 18 ;
- la scintigraphie avec la tomographie par émission monophotonique (TEMP), pour détecter les rayonnements gamma, par exemple de l'iode 123.
Modalités de réalisation
Pour la réalisation d'une imagerie fonctionnelle moléculaire, que ce soit par TEP ou par TEMP en scintigraphie, le principe est globalement le même. Les radiotraceurs sont le plus souvent administrés par voie intraveineuse ; cette injection est ensuite suivie d'un temps de pause variable (le temps que le radiotraceur se fixe à sa cible) avant la réalisation des images. La détection des radiotraceurs est souvent couplée à la réalisation d'une TDM basse dose pour réaliser une correction d'atténuation et améliorer la qualité des images et leur quantification : c'est l'imagerie hybride par TEP-TDM ou TEMP-TDM, voire d'une IRM (TEP-IRM). On peut réaliser des images de l'ensemble du corps, ou cibler une région, par exemple le cerveau. Les algorithmes de recalage permettent par ailleurs aujourd'hui aisément de fusionner des examens TEP/TEMP à une imagerie morphologique, par exemple une IRM dans les indications cérébrales.
Imagerie de la neurotransmission dopaminergique
Principe de fonctionnement
L'imagerie fonctionnelle des voies dopaminergiques présynaptiques permet de vérifier l'intégrité de la neurotransmission nigrostriée. En cas de syndrome parkinsonien dégénératif (maladie de Parkinson ou syndrome parkinsonien atypique comme la maladie à corps de Lewy diffus ou MCL), on observe une perte de neurones dopaminergiques en lien avec le processus neurodégénératif. Ces neurones de la substance noire se projettent sur le striatum, composé du noyau caudé et du putamen (figure 23.2), formant à l'image un aspect en point-virgule.
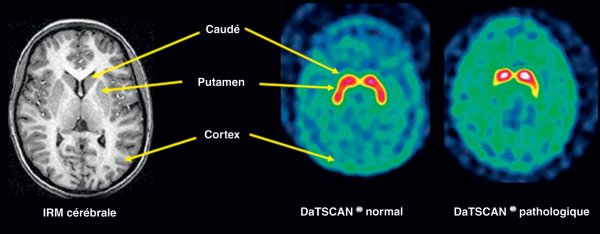
Figure 23.2
Confrontation de l'IRM (à gauche, séquence T1 injectée), avec un DaTSCAN® normal (milieu).
À droite, exemple de DaTSCAN® pathologique montrant une hypofixation asymétrique des deux putamens prédominant à droite,
en faveur d'une dénervation dopaminergique.
On peut imager ces voies dopaminergiques en imagerie fonctionnelle par deux traceurs présynaptiques :
- soit par scintigraphie : c'est le DaTSCAN®, du nom du radiotraceur qui fixe les transporteurs présynaptiques de la dopamine, marqué à l'iode 123 ;
- soit plus rarement en France par TEP à la 18F-DOPA, qui est un analogue de la L-dopa, reflet de l'activité dopadécarboxylase, transformant la L-dopa en dopamine.
L'analyse visuelle repose sur l'identification d'une hypofixation du radiotraceur en projection du striatum, avec une perte de l'aspect en virgule le plus souvent asymétrique, à prédominance postérieure, du côté opposé de l'atteinte clinique prévalente. Cette interprétation visuelle peut être complétée par une analyse quantifiée mesurant la dénervation dopaminergique en comparaison d'une population de sujets sains de même âge.
Indications
L'exploration fonctionnelle des voies dopaminergique est indiquée dans deux grandes situations cliniques (tableau 23.1) :
- l'exploration de tremblements atypiques ou d'étiologie incertaine. L'examen est recommandé lorsqu'il y a un doute clinique entre un tremblement en relation avec un syndrome parkinsonien dégénératif comme la maladie de Parkinson, et un tremblement essentiel idiopathique non dégénératif. Le tremblement essentiel n'est en effet pas secondaire à une dégénérescence des neurones dopaminergiques, il n'y a donc pas de perte dopaminergique en imagerie. L'examen peut aussi être réalisé chez un patient présentant un syndrome parkinsonien potentiellement lié à une prise médicamenteuse pour préciser si les symptômes sont purement iatrogènes, ou s'il existe un syndrome parkinsonien dégénératif sous-jacent. Dans le cas par exemple d'un syndrome parkinsonien iatrogène secondaire à la prise de neuroleptiques, ces médicaments bloquent les récepteurs dopaminergiques mais il n'y a pas de dégénérescence neuronale et donc pas de perte dopaminergique en imagerie ;
- un doute diagnostique entre deux pathologies neurodégénératives comme une maladie à corps de Lewy diffus (MCL) et une maladie d'Alzheimer (MA) : dans la MA, il n'y a pas de dégénérescence des neurones dopaminergiques : l'examen est normal, alors qu'il est altéré dans la MCL.
Tableau 23.1
Indications et résultats attendus de l'imagerie moléculaire dopaminergique.
| Dénervation dopaminergique | Absence de dénervation dopaminergique |
| Bilan de tremblement | |
| Tremblement parkinsonien | Tremblement essentiel |
| Bilan d'un syndrome parkinsonien sous neuroleptiques | |
| Syndrome parkinsonien dégénératif | Syndrome parkinsonien purement iatrogène |
| Bilan de troubles cognitifs | |
| Maladie à corps de Lewy diffus | Maladie d'Alzheimer |
Il existe également une autre indication dans laquelle l'imagerie fonctionnelle des voies dopaminergiques peut être utile au diagnostic. Il s'agit des patients présentant un syndrome parkinsonien associé à des lésions vasculaires des voies dopaminergiques :
- pour déterminer s'il est purement lié aux lésions vasculaires (comme des lacunes au niveau du striatum) ; dans ce cas, on visualise en confrontation de l'IRM une perte dopaminergique uniquement en regard des lésions vasculaires ;
- s'il est secondaire à un syndrome parkinsonien dégénératif ; dans ce cas, la perte dopaminergique est plus diffuse et pas uniquement en projection des lésions vasculaires.
TEP cérébrale au 18F-FDG
Le radiotraceur le plus fréquemment utilisé pour la TEP est le 18F-fluorodéoxyglucose (18F-FDG). Il s'agit d'une molécule de sucre (le glucose) sur laquelle a été rajouté un atome radioactif de fluor 18, émetteur de positons, qui peut être détectée par la caméra TEP. Ce radiotraceur permet d'étudier le métabolisme du glucose au repos (figure 23.3). Le patient doit être à jeun 4 à 6 heures avant l'examen afin de ne perturber la fixation du radiotraceur par le cerveau ; cet examen nécessite un équilibre glycémique, ce qui est parfois difficile à obtenir chez les patients diabétiques. Un contrôle glycémique est réalisé avant l'injection du radiotraceur afin de vérifier l'absence d'hyperglycémie qui diminuerait la sensibilité de l'examen. La consommation métabolique de glucose par le cerveau est le reflet de l'activité synaptique globale. C'est un biomarqueur non spécifique qui est altéré dans de nombreuses pathologies cérébrales. D'autres radiotraceurs que le 18F-FDG ont des indications aujourd'hui plus marginales, par exemple la 18F-DOPA qui peut être utilisée en alternative du DaTSCAN® déjà mentionné (mais qui constitue une cible dopaminergique moins sensible) ou, plus récemment, les radiotraceurs TEP permettant de mesurer d'éventuels dépôts amyloïdes, comme dans la maladie d'Alzheimer, en particulier lorsque l'analyse du liquide cérébrospinal par ponction lombaire n'est pas possible ou donne des résultats discordants ou indéterminés.
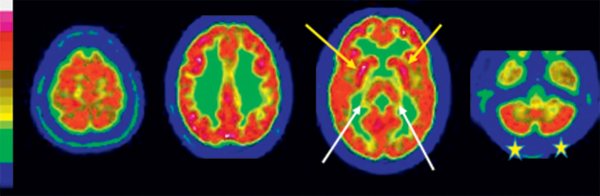
Figure 23.3
Exemple d'un aspect normal en TEP cérébrale au 18F-FDG en coupe axiale.
À gauche, l'échelle de couleur suivie des coupes axiales d'une TEP normale en partant du sommet du crâne à gauche vers le bas du crâne à droite. Le cortex cérébral, le striatum (flèches jaunes) et les thalami (flèches blanches) présentent une fixation homogène qui apparaît en rouge, de même que les deux hémisphères cérébelleux (étoile).
Intérêt dans les pathologies neurodégénératives
La TEP cérébrale au 18F-FDG présente un intérêt dans le diagnostic des maladies neurodégénératives car les altérations du métabolisme glucidique cérébral sont précoces : elles précèdent le plus souvent les altérations morphologiques visibles en IRM comme l'atrophie. Si l'hypométabolisme cérébral de la consommation de glucose n'est pas en soi spécifique, le profil global de l'atteinte peut néanmoins apporter des éléments de spécificité en fonction de sa sévérité et des régions précisément touchées et préservées, des profils distincts ayant été retrouvés sur les différentes pathologies corticales neurodégénératives.
La TEP cérébrale est en particulier recommandée dans l'exploration de troubles neurocognitifs en cas de présentation atypique/de début précoce et/ou d'incertitude au diagnostic. Elle permet d'apporter des arguments positifs en faveur d'une pathologie neurodégénérative.
Exemple
Dans la maladie d'Alzheimer, on observe sur la TEP cérébrale au 18F-FDG un hypométabolisme cortical des régions associatives postérieures (pariéto-temporo-occipitales) et plus tardivement du cortex temporal interne (figure 23.4), les régions primaires sont préservées ainsi que le cervelet et les ganglions de la base ; alors que dans la démence frontotemporale, on observe un hypométabolisme des lobes frontotemporaux, le plus souvent asymétrique (figure 23.5).
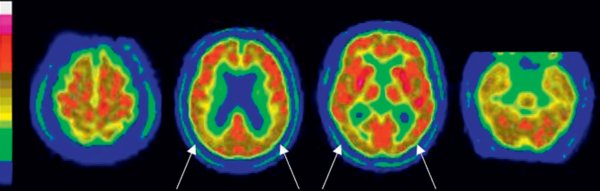
Figure 23.4
Exemple de l'aspect en TEP cérébrale au 18F-FDG en coupe axiale d'une maladie d'Alzheimer (de l'apex à gauche vers la base du crâne à droite).À gauche, l'échelle de couleur (le cortex présente normalement une fixation homogène qui apparaît en rouge), suivie des coupes axiales en TEP montrant un hypométabolisme modéré diffus qui prédomine au niveau des régions associatives postérieures (flèches).
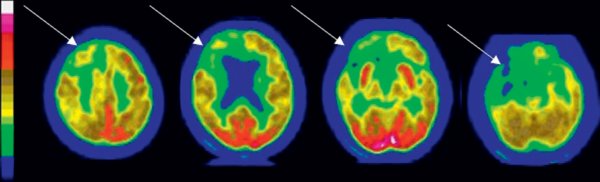
Figure 23.5
Exemple de l'aspect en TEP cérébrale au 18F-FDG en coupe axiale d'une démence frontotemporale.
Hypométabolisme cortical diffus, associé à un hypométaboblisme marqué du cortex frontotemporal à droite (flèches).
Intérêt dans les autres pathologies
La TEP cérébrale présente également un intérêt dans de nombreuses autres pathologies comme le diagnostic et suivi d'encéphalites, les tumeurs cérébrales, le bilan d'épilepsie pharmacorésistante, etc.
Scintigraphie de perfusion cérébrale
La scintigraphie de perfusion cérébrale ou débit sanguin cérébral permet, comme son nom l'indique, d'évaluer la perfusion cérébrale. Très schématiquement, elle détecte des anomalies superposables à celles observées sur la TEP au 18F-FDG, mais avec une nettement moins bonne résolution spatiale. Pour cette raison, elle est aujourd'hui souvent remplacée par la TEP au FDG. Elle garde un intérêt chez les patients diabétiques ou avec des troubles glycémiques chez qui la TEP n'a pas été contributive.
- L'imagerie moléculaire en médecine nucléaire permet l'exploration du fonctionnement d'un organe ou d'un processus : par exemple le métabolisme cérébral ou l'intégrité des voies dopaminergiques.
- Les deux modalités d'imagerie fonctionnelle sont la TEP et la TEMP en scintigraphie, selon le type de radioactivité émise par le radiotraceur.
- L'imagerie par TEP cérébrale au 18F-FDG permet le diagnostic et le suivi de nombreuses maladies, notamment dans le cadre des maladies neurodégénératives. Chaque maladie neurodégénérative présente un profil métabolique particulier en TEP, ce qui peut être utile pour leur diagnostic précoce, et en cas de clinique atypique.
- L'imagerie des récepteurs dopaminergiques permet de rechercher une dénervation dopaminergique, visible en cas de syndrome parkinsonien d'origine dégénérative. Ainsi, elle permet de différencier :
- un tremblement dans le cadre d'une maladie de Parkinson d'un tremblement essentiel ;
- un syndrome parkinsonien iatrogénique secondaire par exemple à la prise de neuroleptiques d'un syndrome parkinsonien dégénératif.
Voir QRM chapitre 32.
