Emmanuel Cognat et Virginie Desestret
Système nerveux
D'un point de vue histologique, le système nerveux central (SNC) est subdivisé en deux composantes dont la proportion et l'organisation varient selon les régions anatomiques, la substance grise et la substance blanche. Schématiquement, la substance grise contient les corps cellulaires des neurones alors que la substance blanche contient leurs prolongements. Les cellules dites gliales, c'est-à-dire astrocytes, oligodendrocytes et cellules microgliales sont présentes dans la substance grise comme dans la substance blanche, avec des différences morphologiques, organisationnelles et fonctionnelles. À ces deux composantes observées dans le SNC s'ajoutent les racines nerveuses et les nerfs qui sont formés par les prolongements neuronaux (entourés ou non de myéline) qui s'étendent au-delà de la moelle spinale et forment le système nerveux périphérique (SNP).
Cellules du système nerveux
Neurones
Les neurones sont des cellules spécialisées dans la genèse, la propagation, la réception et le traitement de l'information. Cette information prend la forme de signaux électriques qui se propagent le long de prolongements interconnectés. On peut ainsi distinguer différents compartiments ayant des fonctions distinctes (figure 2.1) :
- le corps ou soma qui contient le noyau et les principaux organites et dans lequel sont assurées la plupart des fonctions cellulaires essentielles ;
- l'axone, prolongement unique et non ramifié (hormis à sa terminaison) qui se projette parfois à très longue distance pour former, à sa terminaison, le bouton synaptique, des connexions avec d'autres neurones ou des cellules effectrices ;
- les dendrites, prolongements multiples, ramifiés et courts (comparativement à l'axone), sièges de très nombreuses connexions avec les axones par des jonctions spécialisées, les synapses.
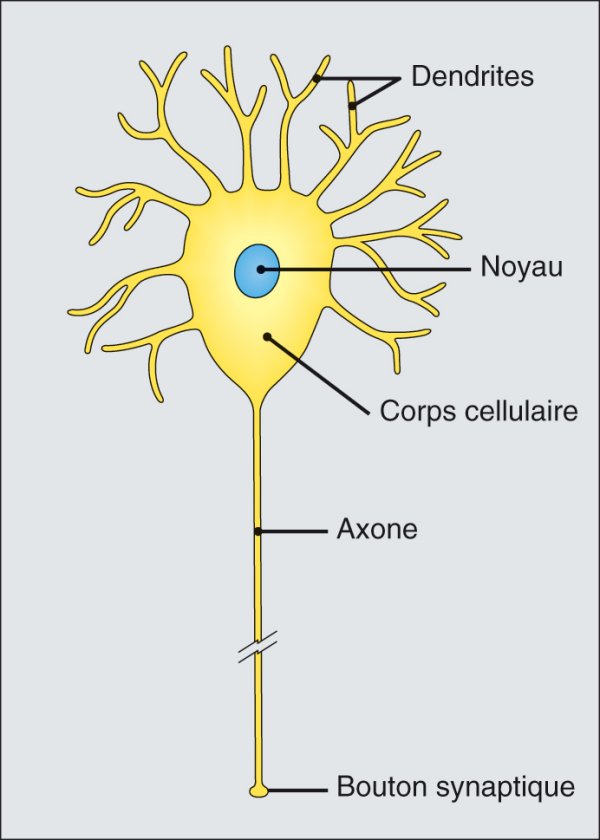
Figure 2.1
Structure générale du neurone.
Les neurones comprennent un corps cellulaire, un axone et des dendrites. L'axone transmet des influx vers son extrémité, le bouton synaptique, qui entre en contact avec une autre cellule. Les dendrites reçoivent des contacts avec des boutons synaptiques provenant d'autres neurones.
© Stevens A, Lowe JS. Histologie humaine, 3e éd. Trad fr. A. Défossez et C.-A. Maurage. Paris : Elsevier Masson ; 2006.
Corps cellulaire
Le corps cellulaire des neurones abrite un noyau volumineux et clair avec habituellement un seul nucléole de grande taille. Les organites habituels sont présents en abondance dans le cytoplasme dont un réticulum endoplasmique granuleux abondant qui s'organise en granules basophiles, les corps de Nissl. Avec le vieillissement, le cytoplasme se charge de dépôts pigmentaires de lipofuscine, qui sont des pigments insolubles dérivant des lysosomes.
Cytosquelette
Le cytosquelette abondant comprend trois types de filaments :
- filaments fins d'actine répartis dans toute la cellule, impliqués dans la cytoarchitecture, la mobilité des récepteurs membranaires et la plasticité synaptique ;
- filaments intermédiaires spécifiques du neurone, les neurofilaments, répartis dans toute la cellule et enrichis dans la région axonale. Ils sont constitués par l'assemblage de trois sous-unités (neurofilaments légers, moyens et lourds) et jouent principalement un rôle structural ;
- filaments épais ou microtubules principalement localisés dans les prolongements neuronaux et en particulier l'axone. Ils sont au centre du processus de transport axonal.
Dendrite
Les dendrites sont des prolongements neuronaux courts et ramifiés qui augmentent la surface de la membrane plasmique du neurone et permettent d'augmenter le nombre de connexions synaptiques réceptrices formées par le neurone. Ces connexions apparaissent comme de petites élevures sur la membrane dendritique appelées épines dendritiques. Les dendrites ne sont jamais recouvertes de myéline.
Axone
L'axone est un prolongement unique, long (jusqu'à 1,2 m), ramifié uniquement à son extrémité synaptique. Son diamètre varie entre 1 et 15 µm et est constant tout le long de l'axone. Il conduit l'influx nerveux du corps cellulaire vers la terminaison synaptique (centrifuge). Il peut être ou non recouvert de myéline.
Les caractéristiques des dendrites et des axones sont comparées dans le tableau 2.1.
Tableau 2.1
Caractéristiques des prolongements d'un neurone.
| Caractéristique | Dendrites | Axone |
|---|---|---|
| Nombre | Multiples | Unique |
| Aspect | Flou : épines dendritiques | Lisse |
| Diamètre | Diminuant vers la périphérie | Constant (segment principal) |
| Ramifications | Multiples précoces | Terminales |
| Myéline | Jamais | Parfois |
Astrocytes
Les astrocytes sont de grandes cellules étoilées dont les prolongements se projettent vers de nombreuses cellules et structures du SNC. Leur noyau est ovalaire, assez volumineux. Les astrocytes contiennent un filament intermédiaire spécifique, la GFAP (glial fibrillary acidic protein). On distingue deux types d'astrocytes :
- les astrocytes protoplasmiques ont un aspect étoilé avec des prolongements épais, courts et très ramifiés. Ils sont principalement observés dans la substance grise ;
- les astrocytes fibrillaires ont des prolongements longs, fins et peu ramifiés. Ils sont principalement observés dans la substance blanche.
Les astrocytes jouent de nombreux rôles : - soutien par la formation d'une charpente au sein de laquelle migrent et s'organisent les cellules nerveuses (figure 2.2) ;
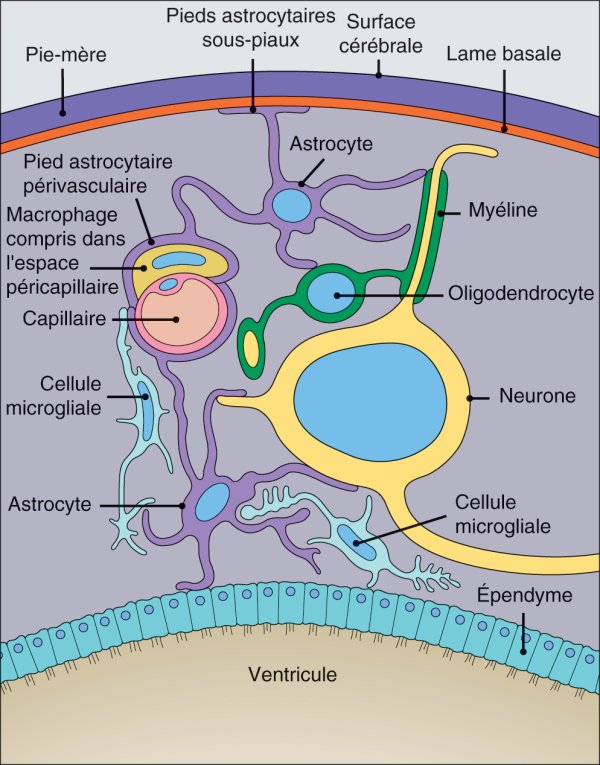
Figure 2.2
Les cellules de soutien du système nerveux central (SNC).
Les cellules de soutien du SNC ou cellules gliales ont différents rôles. Les astrocytes forment non seulement un échafaudage pour les autres types cellulaires mais également des prolongements ou pieds astrocytaires au pourtour des capillaires afin de constituer une barrière sang – cerveau. À la surface du cerveau, les astrocytes forment une lame basale et des prolongements cellulaires, la glie limitante, qui recouvrent l'ensemble du SNC. Les oligodendrocytes myélinisent l'axone des neurones. Un vaste réseau de cellules microgliales reconnaissant les antigènes s'étend sur tout le SNC. Des macrophages également impliqués dans les défenses immunitaires résident dans les espaces périvasculaires, en dehors du parenchyme du SNC. Les cellules épendymaires forment un revêtement continu, ne reposant pas à la surface d'une lame basale, à la différence des autres épithéliums. L'épendyme tapisse les cavités ventriculaires du cerveau, contenant le liquide cérébrospinal, ainsi que le canal épendymaire au centre de la moelle spinale.
© Stevens A, Lowe JS. Histologie humaine, 3e éd. Trad fr. A. Défossez et C.-A. Maurage. Paris : Elsevier Masson ; 2006.
- participation à la formation, à la maintenance et au fonctionnement des synapses ;
- participation à la formation de la barrière hématoencéphalique ;
- formation d'une couche sous-piale, la glia limitans (ou glie limitante) ;
- interaction avec les autres cellules gliales, les épendymocytes et d'autres astrocytes ;
- participation au couplage neurovasculaire (adaptation de l'apport sanguin à l'activité neuronale).
Cellules myélinisantes
Oligodendrocytes
Ce sont les cellules myélinisantes du SNC. Leur corps cellulaire est arrondi, de petite taille. Dans la substance blanche, les oligodendrocytes s'alignent le long des faisceaux de substance blanche (disposition interfasciculaire) et envoient des prolongements fins vers les axones qu'ils myélinisent. Un oligodendrocyte myélinise plusieurs axones environnants. On trouve également des oligodendrocytes dans la substance grise au contact du corps cellulaire des neurones (oligodendrocytes satellites, rôle dans le métabolisme neuronal).
Cellules de Schwann
Ce sont les cellules myélinisantes du SNP. En coupe transversale, elles prennent la forme d'un croissant aplati à la face externe de la gaine de myéline. Le noyau occupe la majorité du volume du corps cellulaire, avec un cytoplasme résiduel peu abondant. La membrane plasmique est en continuité directe avec la gaine de myéline. Contrairement aux oligodendrocytes, une cellule de Schwann ne myélinise qu'un seul segment axonal.
On trouve également des cellules de Schwann autour des axones non myélinisés. Le corps cellulaire de ces dernières apparaît moins aplati et envoie des prolongements qui englobent un ou plusieurs axones
Microglie
Les cellules microgliales sont les cellules macrophagiques résidentes du SNC. Ce sont de petites cellules au noyau ovale et dense avec des prolongements fins et ramifiés qui leur donnent un aspect étoilé à l'état basal. En cas d'agression du système nerveux, la morphologie des cellules microgliales se modifie avec augmentation de la taille du corps cellulaire et épaississement des prolongements (phénotype activé) et leur nombre augmente (cf. chapitre 25).
Épendymocytes
Ils sont classés parmi les cellules gliales. Cubiques ou prismatiques, ils sont organisés en une seule couche de cellules qui borde les ventricules cérébraux, le canal épendymaire médullaire et recouvrent les plexus choroïdes. Les épendymocytes jouent un rôle important dans la production/résorption du liquide cérébrospinal et sa circulation.
Structures particulières
Synapses
Elles permettent la communication entre la terminaison axonale d'un neurone et une autre cellule excitable (neurone, muscle, etc.) par le biais de petites molécules appelées neurotransmetteurs. La plupart des synapses neuro-neuronales sont formées entre axone et dendrite (au niveau d'une épine dendritique), mais d'autres configurations sont observées (axone – corps cellulaire, etc.).
La synapse est formée de trois parties (figure 2.3) :
- la terminaison axonale présente un renflement, le bouton synaptique qui contient de nombreuses vésicules remplies de neurotransmetteurs ;
- l'élément post-synaptique correspond à un épaississement de la membrane lié aux récepteurs des neurotransmetteurs qui sont enchâssés dans la membrane et à la présence d'un important appareil sous-synaptique ;
- les deux membranes sont séparées par un espace, la fente synaptique, dans laquelle sont déversés les neurotransmetteurs. La fente synaptique contient des enzymes de dégradation des neurotransmetteurs (ex : acétylcholinestérase) qui permettent de contrôler la durée de la transmission synaptique.
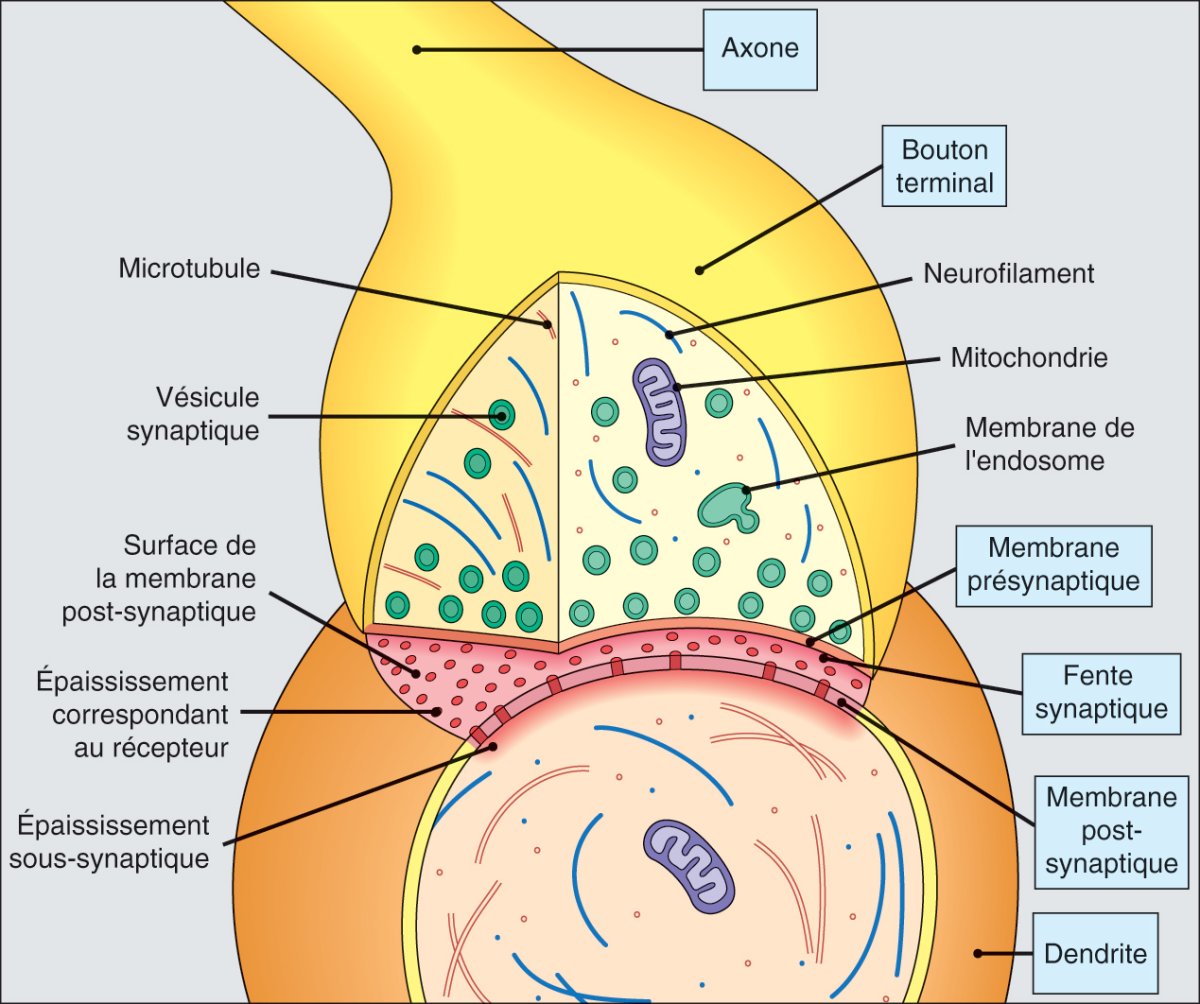
Figure 2.3
Synapse.
L'axone se termine par un bouton synaptique à la surface d'un neurone. La membrane post-synaptique expose des groupes de récepteurs pour le neurotransmetteur compris dans les vésicules synaptiques. Les vésicules sont libérées dans la fente synaptique par exocytose.
© Stevens A, Lowe JS. Histologie humaine, 3e éd. Trad fr. A. Défossez et C.-A. Maurage. Paris : Elsevier Masson ; 2006.
L'arrivée du potentiel d'action au niveau de la terminaison axonale déclenche la fusion des vésicules synaptiques à la membrane présynaptique et le déversement des neurotransmetteurs (exocytose) dans la fente synaptique. Les vésicules sont ensuite internalisées pour être recyclées. Les neurotransmetteurs libérés traversent la fente synaptique et se fixent sur les récepteurs de la membrane post-synaptique avec différents effets possibles selon le neurotransmetteur et l'appareil sous-synaptique (excitation, inhibition ou neuromodulation).
Myéline
C'est un manchon lipidique isolant qui entoure certains axones du SNC et du SNP. Elle est formée par l'enroulement de prolongements d'oligodendrocytes ou de cellules de Schwann dont les membranes plasmiques s'accolent. L'observation en microscopie électronique montre un aspect spiralé en coupe avec alternance de lignes denses dites lignes denses majeures (accolement des faces cytoplasmiques de la membrane oligodendrocytaire) et claires (accolement des faces externes). Ces accolements et la compaction de la myéline font intervenir un certain nombre de protéines clés, telles que, par exemple, pour la myéline du SNC, la MBP (myelin binding protein) ou la MOG (myelin oligodendrocyte glycoprotein). Du cytoplasme oligodendrocytaire reste présent dans les régions périaxonale, paranodale (proche du nœud de Ranvier) et périphérique (mésaxone) qui sont mises en contact par les incisures de Schmidt-Lanterman.
La gaine de myéline est interrompue régulièrement par des régions dénudées de l'axone, les nœuds de Ranvier, qui sont impliqués dans la conduction saltatoire de l'influx nerveux (figure 2.4).
 |
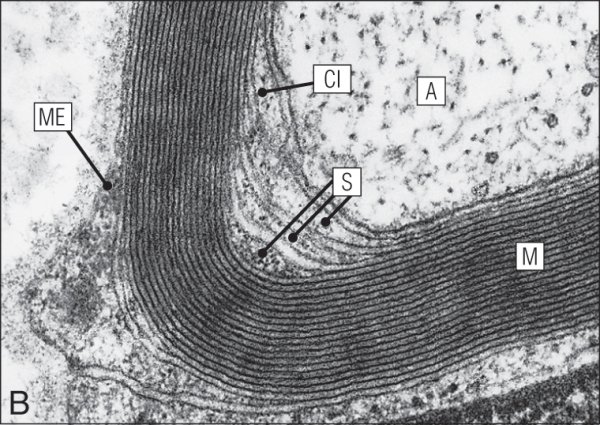 |
Figure 2.4
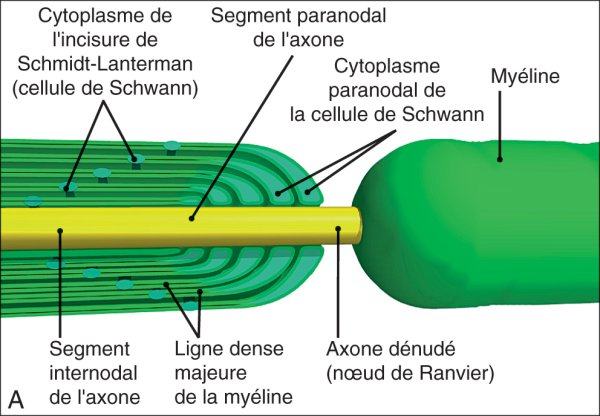
Nœud de Ranvier.
A. Coupe longitudinale d'un nœud de Ranvier. À l'extrémité d'un segment de myéline (internode), les lamelles de myéline laissent place à une série de boucles paranodales contenant du cytoplasme. Le segment d'axone adjacent, dénudé, est le plus souvent plus épais que l'axone internodal. Cette région renferme les canaux Na+ potentiel-dépendants, nécessaires à la création d'un potentiel d'action.
B. À grossissement intermédiaire, la microscopie électronique montre la structure de la myéline. L'axone (A) est entouré par des lamelles de myéline (M) en continuité avec la partie externe du mésaxone (ME). Les reliquats du cytoplasme dans la myéline forment des incisures de Schmidt-Lanterman (S) et le collier interne de cytoplasme schwannien (CI).
© Stevens A, Lowe JS. Histologie humaine, 3e éd. Trad fr. A. Défossez et C.-A. Maurage. Paris : Elsevier Masson ; 2006.
Barrière hématoencéphalique
Il s'agit d'un filtre physicochimique très sélectif qui protège le cerveau des agents pathogènes, des toxines et des hormones qui circulent dans le sang. Elle est formée au niveau des capillaires cérébraux par l'association :
- de cellules endothéliales reliées par de nombreuses jonctions serrées assurant l'étanchéité de l'endothélium ;
- entourées d'une membrane basale épaisse ;
- entourée de péricytes qui la recouvrent partiellement ;
- entourés de prolongements astrocytaires (pieds vasculaires) qui tapissent 99 % de la surface capillaire et contiennent certaines protéines, telles que, par exemple, l'aquaporine 4.
Des protéines d'efflux qui rejettent les molécules « non autorisées » vers le compartiment sanguin complètent cette barrière physique
Méninges
Les méninges sont des enveloppes protectrices qui entourent le SNC sur toute sa surface externe. La disposition générale des méninges spinales et encéphaliques est détaillée dans le chapitre 1. Elles sont faites de trois couches superposées :
- la dure-mère est un tissu conjonctif fibreux et résistant qui envoie des extensions entre les hémisphères cérébraux (faux) et entre cerveau et cervelet (tente du cervelet). Elle est creusée, en particulier dans ces régions, par les sinus veineux ;
- la pie-mère est une fine couche de tissu conjonctif en contact direct avec le SNC par le biais de la glie limitante ;
- l'arachnoïde est un tissu conjonctif lâche et ajouré au sein duquel circulent les vaisseaux cérébraux.
Des replis de pie-mère accompagnent les vaisseaux perforants, délimitant des espaces périvasculaires, les espaces de Virchow-Robin.
Plexus choroïdes
Situés dans les ventricules cérébraux, ils sont formés de vaisseaux disposés en grappes, entourés de tissu conjonctif et d'une couche de cellules épithéliales d'épendymocytes qui sécrètent le liquide cérébrospinal.
Organisations tissulaires
Cortex
Il recouvre le cerveau et le cervelet et contient la majorité des neurones qui les composent. Il est formé de 3 à 6 couches selon la localisation, qui se distinguent par le type de neurones qu'elles contiennent et leur densité. Le cortex contient également tous les types de cellules gliales, et en particulier des oligodendrocytes satellites et des astrocytes protoplasmiques. Les corps cellulaires reposent dans une matrice faite de l'enchevêtrement des prolongements de toutes les cellules corticales, le neuropile.
Substance blanche
La substance blanche, de localisation interne dans le cerveau et le cervelet et externe dans la moelle spinale, est formée principalement par les faisceaux d'axones myélinisés des neurones corticaux. Il s'agit d'un tissu peu vascularisé et peu cellulaire comparativement au cortex. Les principales populations cellulaires de la substance blanche sont les oligodendrocytes interfasciculaires et les astrocytes fibrillaires.
Moelle spinale et racines nerveuses
À l'inverse du cerveau et du cervelet, les cordons de substance blanche sont disposés en périphérie dans la moelle spinale. La substance grise, de localisation centrale, contient les corps cellulaires des neurones moteurs périphériques (deuxièmes motoneurones, localisés dans la corne ventrale) et d'interneurones (impliqués dans les réflexes tendineux). Les corps cellulaires des neurones sensitifs sont localisés dans le ganglion spinal qui fait protrusion sur la racine nerveuse dorsale. La racine ventrale contient les axones des neurones moteurs périphériques.
Nerfs périphériques
Ils contiennent les axones des neurones somatiques (moteurs et sensitifs) et des neurones végétatifs périphériques (figure 2.5). Les axones myélinisés ou emballés dans des cellules de Schwann (axones amyéliniques) sont entourés d'un tissu de soutien conjonctif appelé endonèvre. Ces axones se groupent en faisceaux, les fascicules, entourés par une gaine conjonctive, le périnèvre. Les fascicules sont regroupés et solidarisés en un tronc nerveux par l'épinèvre, tissu conjonctif et adipeux dans lequel circulent les vaisseaux nourriciers du nerf.
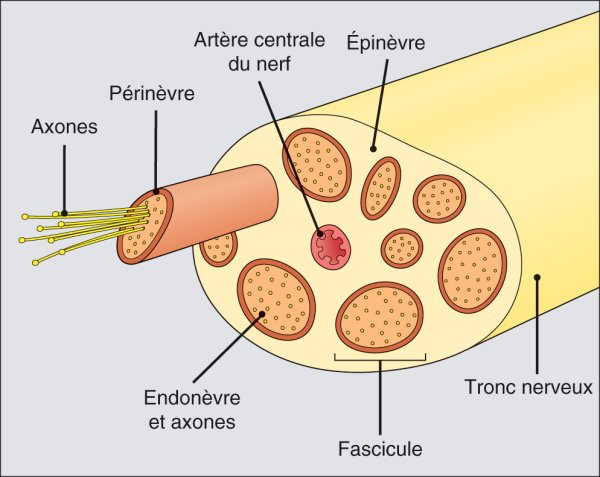
Figure 2.5
Tissu de soutien du nerf périphérique.
Sur ce schéma montrant l'organisation des tissus de soutien d'un nerf périphérique, chaque axone et les cellules de Schwann qui lui sont associées sont entourés par l'endonèvre et sont regroupés en fascicules par le périnèvre, tissu de type épithélial. L'épinèvre relie plusieurs fascicules en un même tronc nerveux, il peut également contenir l'artère irriguant le tronc nerveux.
© Stevens A, Lowe JS. Histologie humaine, 3e éd. Trad fr. A. Défossez et C.-A. Maurage. Paris : Elsevier Masson ; 2006.
Tissu musculaire
Le tissu musculaire est formé d'un type cellulaire principal : le myocyte qui est une cellule contractile dont le raccourcissement génère une force motrice. On distingue trois grands types de myocytes :
- les rhabdomyocytes ou cellules musculaires striées squelettiques qui composent les muscles squelettiques dont la contraction se fait sous contrôle volontaire (système nerveux somatique) ;
- les cardiomyocytes ou cellules musculaires striées cardiaques trouvés uniquement dans le muscle cardiaque dont la contraction est rythmique et involontaire (système nerveux autonome) ;
- les léiomyocytes ou cellules musculaires lisses dont la contraction est également involontaire (système nerveux autonome) et trouvés dans les vaisseaux sanguins et la paroi des organes creux. Trois autres types cellulaires sont apparentés aux léiomyocytes : les cellules myoépithéliales, les myofibroblastes et les péricytes.
Quel que soit le type de cellule musculaire, la force motrice est générée par l'interaction de deux protéines filamentaires, la myosine et l'actine, et dont résulte un raccourcissement de la cellule.
Muscle strié
Rhabdomyocytes
Les rhabdomyocytes ou cellules musculaires striées squelettiques, ou encore « fibres » musculaires sont de grandes cellules multinucléées d'environ 50 μm de diamètre et qui peuvent atteindre jusqu'à 10 cm de longueur, entourées d'une lame basale. Leurs nombreux noyaux sont disposés sous la membrane plasmique (sarcolemme), le cytoplasme appelé sarcoplasme étant principalement occupé par les myofibrilles contractiles entre lesquelles se trouvent de nombreuses mitochondries et un réticulum endoplasmique abondant (réticulum sarcoplasmique). Les tubules T sont des invaginations du sarcolemme qui s'associent à des citernes de réticulum sarcoplasmique (2 citernes/1 tubule) pour former des unités fonctionnelles appelées triades.
Myofibrilles
Ce sont de fins cylindres qui s'étirent parallèlement sur toute la longueur de la cellule. Les myofibrilles sont formées par la répétition d'unités contractiles élémentaires, les sarcomères (figure 2.6). Cette répétition est à l'origine de la striation périodique observée en microscopie, qui a inspiré le qualificatif donné à ces cellules.
 |
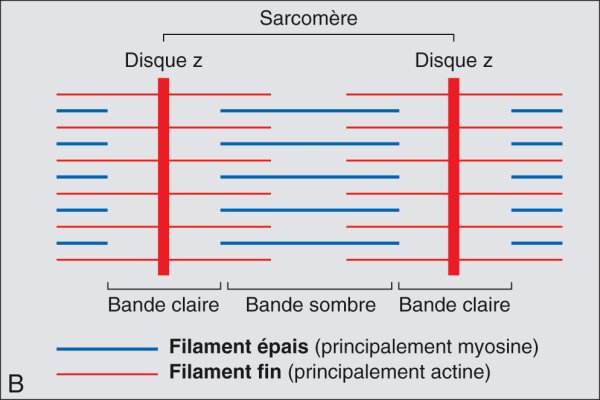 |
Figure 2.6
Myofibrilles.
A. En microscopie électronique, les myofibrilles se subdivisent en plusieurs secteurs. La bande A (sombre) correspond à la zone des filaments épais. Elle contient également une portion des filaments fins, au niveau du recouvrement entre filaments épais et fins. La bande H est une bande plus pâle située au centre de la bande A, elle ne contient que des filaments épais, en l'absence de tout filament fin. La bande I (claire) ne contient que la portion des filaments fins ne recouvrant pas les filaments épais. La strie Z est une strie sombre située au centre de la bande I et la strie M marque le centre de la bande H. Chaque unité délimitée par deux stries Z successives est nommée sarcomère.
B. Disposition des filaments dans un sarcomère. Les filaments fins sont majoritairement composés d'actine, les filaments épais de myosine.
© Stevens A, Lowe JS. Histologie humaine, 3e éd. Trad fr. A. Défossez et C.-A. Maurage. Paris : Elsevier Masson ; 2006.
Sarcomères
Ils sont formés par un assemblage de filaments fins d'actine et de filament épais de myosine qui délimite une alternance de bandes claires et sombres. Les filaments épais ont une disposition centrale dans le sarcomère et sont entourés par les filaments d'actine partiellement chevauchants et localisés en périphérie. On trouve donc dans la portion latérale du sarcomère une bande claire contenant uniquement des filaments fins, la bande I, et dans la région médiane une bande plus sombre formée par le chevauchement de filaments fins et épais, la bande A. Au repos, la région centrale du sarcomère (bande H) apparaît plus claire du fait de l'absence de filaments d'actine.
L'ensemble des filaments est solidarisé par des protéines de structure, qui forment en périphérie une densification au niveau de la jonction entre les sarcomères adjacents, le disque Z et une ligne dense centrale au niveau de chaque sarcomère, la strie M. D'autres complexes protéiques (complexe dystrophine/protéines associées et complexe intégrine/taline/vinculine) assurent l'ancrage des myofibrilles au sarcolemme.
Contraction
La dépolarisation du sarcolemme déclenche l'entrée de calcium dans le rhabdomyocyte au niveau des triades. Le calcium se fixe sur la troponine, protéine inhibitrice associée aux filaments d'actine, qui se déplace et dévoile un site de fixation de la myosine sur l'actine. La partie de la myosine accrochée à l'actine (tête) subit alors une modification de conformation impliquant l'hydrolyse de l'ATP (adénosine triphosphate), ce qui fait coulisser le filament d'actine vers le centre du sarcomère et entraîne son raccourcissement.
Organisation générale des muscles squelettiques
Les rhabdomyocytes sont entourés de tissu conjonctif, l'endomysium, et réunis en faisceaux. Chaque faisceau est entouré d'un tissu conjonctif vasculaire contenant les éléments nerveux qui commandent la contraction, le périmysium. Le muscle formé de l'ensemble de ces faisceaux est lui-même entouré d'une enveloppe conjonctive, l'épimysium. Cet épimysium se prolonge aux extrémités par un tissu conjonctif dense orienté formant les tendons par lesquels les muscles s'insèrent sur les os.
Autres cellules
Le muscle strié contient d'autres types cellulaires :
- les cellules satellites sont des cellules souches myogéniques inactives localisées entre le sarcolemme des myocytes et la membrane basale. Elles prolifèrent pour réparer le muscle après une lésion ou en réponse à l'exercice musculaire ;
- les fuseaux neuromusculaires sont des fibres musculaires spécialisées sensibles à l'étirement du muscle (récepteurs sensoriels) entourées de prolongements nerveux.
Muscle cardiaque
Cardiomyocytes
Ce sont des cellules musculaires striées qui diffèrent des rhabdomyocytes par plusieurs aspects :
- noyau unique et central ;
- taille réduite : 15 μm de diamètre, 100 μm de longueur ;
- liaison des cardiomyocytes entre eux par leurs extrémités disposées en marches d'escalier, les stries scalariformes. Ces structures permettent un double couplage, mécanique par la présence de jonctions d'ancrage qui solidarisent les cellules dans les portions transversales, et électrique par celle de jonctions communicantes (gap) qui permettent le passage d'ions d'une cellule à l'autre dans les portions longitudinales ;
- l'association des tubules T et du réticulum sarcoplasmique en dyades (un tubule pour une citerne).
En dehors de ces particularités, l'organisation interne des cardiomyocytes et en particulier celle des sarcomères est similaire à celle observée dans les rhabdomyocytes.
Autres cellules
Deux autres types de cellules dérivent des cellules musculaires cardiaques :
- cellules cardionectrices, cellules non contractiles spécialisées dans la genèse de potentiels d'action et la conduction électrique. Elles sont trouvées en particulier dans les nœuds (sinusal, etc.) et faisceaux de conduction (atrioventriculaire, etc.) myocardiques ;
- cellules myoendocriniennes.
Muscle lisse
Les léiomyocytes ont un aspect et une organisation très différents des autres types de cellules musculaires. Ce sont des cellules fusiformes de 20 à 500 μm de longueur, à noyau central, dont l'appareil contractile ne présente pas de striations transversales. Les cellules sont entourées d'une lame basale par laquelle elles sont unies. Le sarcolemme ne présente pas de tubules T, mais des invaginations ressemblant à des cavéoles qui ont une fonction équivalente.
- Les filaments de myosine et d'actine, qui ne sont pas organisées en myofibrilles, forment des faisceaux enchevêtrés qui s'accrochent à la membrane par le biais des filaments intermédiaires de desmine au niveau de dispositifs appelés plaques denses. Ces plaques denses s'organisent de manière symétrique dans les cellules adjacentes et forment des complexes, les plaques d'attaches, qui assurent le couplage mécanique lors de la contraction.
- Les mécanismes qui sous-tendent les interactions actine/myosine diffèrent de ceux observés dans les cellules musculaires striées.
Les caractéristiques des différents types de myocytes sont comparées dans le tableau 2.2.
Tissu nerveux
- Le système nerveux contient quatre principaux types cellulaires :
- neurones impliqués dans la propagation de l'influx nerveux ;
- astrocytes impliqués dans de nombreuses fonctions structurelles et de support ;
- oligodendrocytes et cellules de Schwann impliqués dans la myélinisation et le support métabolique ;
- cellules microgliales impliquées dans la défense immunitaire.
- L'organisation, les interactions entre ces cellules et leurs caractéristiques varient selon les régions du système nerveux (substance grise/blanche, cortex, nerf périphérique, etc.).
- Les spécificités fonctionnelles du système nerveux (barrière hématoencéphalique, communication interneuronale, etc.) reposent sur des structures histologiques particulières, rendant la connaissance de l'histologie du système nerveux fondamentale pour en appréhender la physiologie.
Tissu musculaire
- Les tissus musculaires sont constitués d'un type cellulaire principal, le myocyte.
- Cette cellule contient un appareil contractile formé par l'assemblage de filaments d'actine et de myosine, qui sont organisés dans le muscle strié squelettique en une unité contractile élémentaire : le sarcomère.
- La contraction musculaire résulte au niveau cellulaire d'un raccourcissement des sarcomères, induit par le coulissement des filaments d'actine sur les filaments de myosine.
Tableau 2.2 : Comparaison des caractéristiques des différents types de myocytes.
| Caractéristiques | Tissu musculaire strié squelettique | Tissu musculaire strié cardiaque | Tissu musculaire lisse |
|---|---|---|---|
| Topographie | Muscles insérés sur le squelette | Myocarde | Organes creux Vaisseaux |
| Noyau | Multiples périphériques | Unique central | Unique central |
| Sarcoplasme myofilamentaire | Central | Périphérique | Périphérique |
| Contrôle | Volontaire Système nerveux somatique |
Involontaire Système nerveux autonome |
Involontaire Système nerveux autonome |
| Appareil sarcoplasmique | Triade | Dyade | Invaginations |
Voir QRM chapitre 32.
