Situations de départ
 50 Malaise/perte de connaissance.
50 Malaise/perte de connaissance.
 120 Convulsions.
120 Convulsions.
 289 Consultation et suivi d’un patient épileptique.
289 Consultation et suivi d’un patient épileptique.
 328 Annonce d’une maladie chronique.
328 Annonce d’une maladie chronique.
 352 Expliquer un traitement au patient (adulte/enfant/adolescent).
352 Expliquer un traitement au patient (adulte/enfant/adolescent).
 354 Évaluation de l’observance thérapeutique.
354 Évaluation de l’observance thérapeutique.
Objectifs pédagogiques
 Connaître les principales définitions.
Connaître les principales définitions.
 Diagnostiquer les principales formes d’épilepsie de l’enfant et de l’adulte.
Diagnostiquer les principales formes d’épilepsie de l’enfant et de l’adulte.
 Identifier les situations d’urgence.
Identifier les situations d’urgence.
 Connaître les principes de la prise en charge.
Connaître les principes de la prise en charge.
Hiérarchisation des connaissances
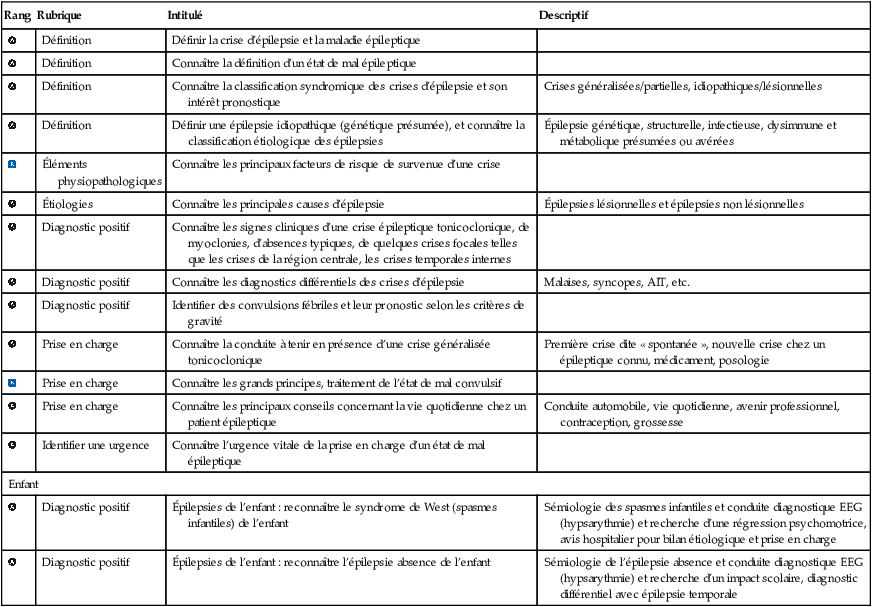
| Rang | Rubrique | Intitulé | Descriptif |
|---|---|---|---|
| Définition | Définir la crise d’épilepsie et la maladie épileptique | ||
| Définition | Connaître la définition d’un état de mal épileptique | ||
| Définition | Connaître la classification syndromique des crises d’épilepsie et son intérêt pronostique | Crises généralisées/partielles, idiopathiques/lésionnelles | |
| Définition | Définir une épilepsie idiopathique (génétique présumée), et connaître la classification étiologique des épilepsies | Épilepsie génétique, structurelle, infectieuse, dysimmune et métabolique présumées ou avérées | |
| Éléments physiopathologiques | Connaître les principaux facteurs de risque de survenue d’une crise | ||
| Étiologies | Connaître les principales causes d’épilepsie | Épilepsies lésionnelles et épilepsies non lésionnelles | |
| Diagnostic positif | Connaître les signes cliniques d’une crise épileptique tonicoclonique, de myoclonies, d’absences typiques, de quelques crises focales telles que les crises de la région centrale, les crises temporales internes | ||
| Diagnostic positif | Connaître les diagnostics différentiels des crises d’épilepsie | Malaises, syncopes, AIT, etc. | |
| Diagnostic positif | Identifier des convulsions fébriles et leur pronostic selon les critères de gravité | ||
| Prise en charge | Connaître la conduite à tenir en présence d’une crise généralisée tonicoclonique | Première crise dite « spontanée », nouvelle crise chez un épileptique connu, médicament, posologie | |
| Prise en charge | Connaître les grands principes, traitement de l’état de mal convulsif | ||
| Prise en charge | Connaître les principaux conseils concernant la vie quotidienne chez un patient épileptique | Conduite automobile, vie quotidienne, avenir professionnel, contraception, grossesse | |
| Identifier une urgence | Connaître l’urgence vitale de la prise en charge d’un état de mal épileptique | ||
| Enfant | |||
| Diagnostic positif | Épilepsies de l’enfant : reconnaître le syndrome de West (spasmes infantiles) de l’enfant | Sémiologie des spasmes infantiles et conduite diagnostique EEG (hypsarythmie) et recherche d’une régression psychomotrice, avis hospitalier pour bilan étiologique et prise en charge | |
| Diagnostic positif | Épilepsies de l’enfant : reconnaître l’épilepsie absence de l’enfant | Sémiologie de l’épilepsie absence et conduite diagnostique EEG (hypsarythmie) et recherche d’un impact scolaire, diagnostic différentiel avec épilepsie temporale | |
I 271Définitions
![]() Distinguer les notions de crise d’épilepsie et de maladie épileptique.
Distinguer les notions de crise d’épilepsie et de maladie épileptique.
A Crise d’épilepsie
Survenue transitoire de signes et/ou de symptômes cliniques due à une activité neuronale
cérébrale excessive et anormalement synchrone.
En pratique, ces signes ou symptômes cliniques peuvent comporter :
- • une altération de la conscience;
- • et/ou des signes moteurs;
- • et/ou des signes sensoriels;
- • et/ou des signes psychiques;
- • et/ou des signes cognitifs;
- • et/ou des signes neurovégétatifs.
272On distingue les crises d’origine généralisée (dites crises généralisées) des crises d’origine focale (dites crises focales) (fig. 16.1). Attention, les crises d’origine focale peuvent se propager et évoluer vers une crise secondairement généralisée. On parle de crise focale secondairement généralisée.
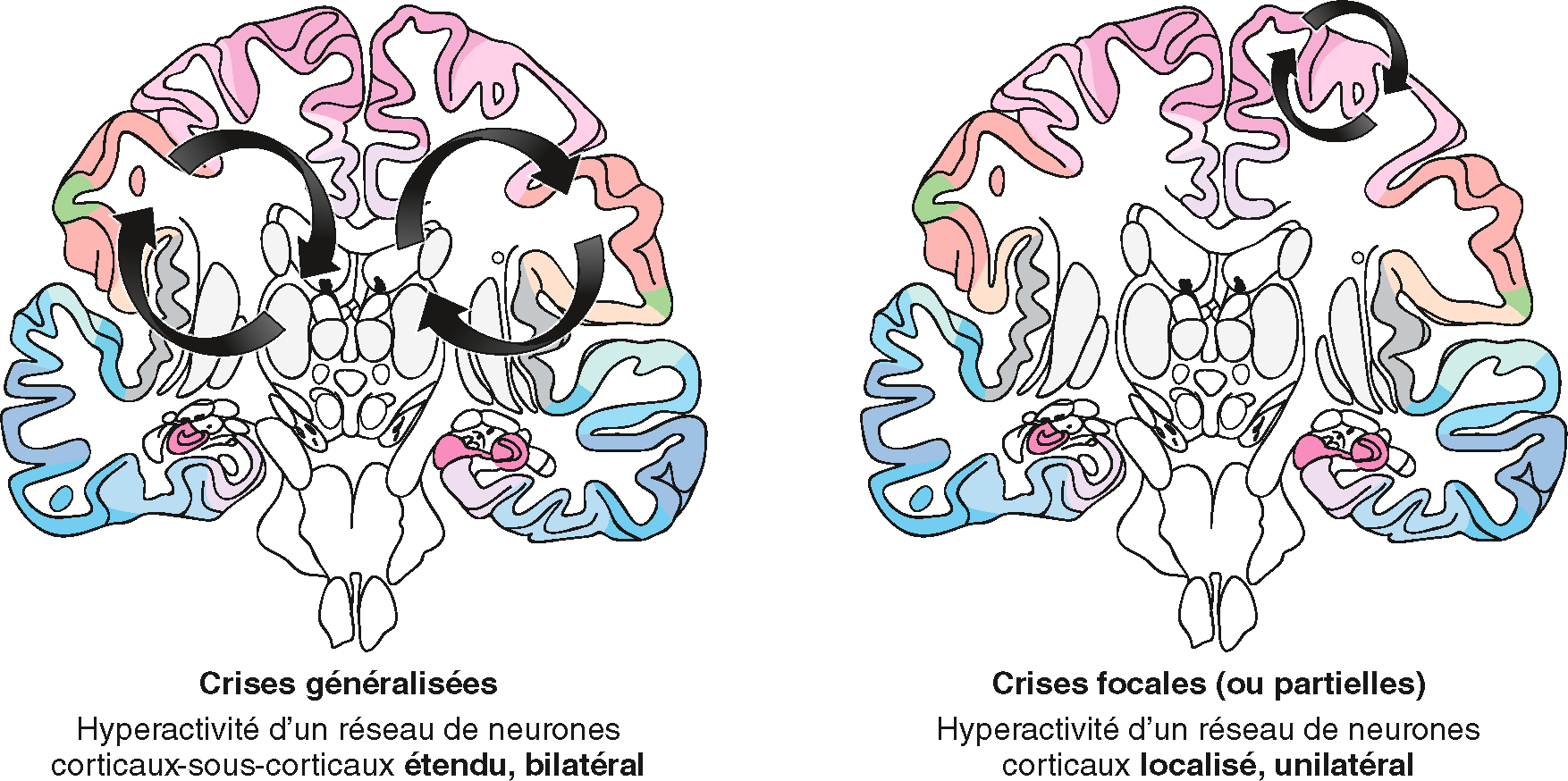
 Définition physiopathologique des crises d’origine focale et crises d’origine généralisée.
Définition physiopathologique des crises d’origine focale et crises d’origine généralisée. Illustration de Carole Fumat.
Les crises d'origine focale et les crises d'origine généralisée sont deux types de crises épileptiques qui diffèrent par leur origine et leur propagation dans le cerveau. Les crises généralisées se caractérisent par une hyperactivité d'un réseau de neurones qui s'étend de manière bilatérale et étendue à travers les régions corticales et sous-corticales du cerveau. L'activité épileptique commence simultanément dans les deux hémisphères du cerveau, affectant ainsi l'ensemble du cerveau dès le début de la crise. Les symptômes peuvent inclure des convulsions, une perte de conscience et des mouvements involontaires des muscles. En revanche, les crises focales, aussi appelées crises partielles, se caractérisent par une hyperactivité d'un réseau de neurones localisée et unilatérale. L'activité épileptique commence dans une région spécifique d'un seul hémisphère du cerveau. Les symptômes des crises focales varient en fonction de la région du cerveau affectée et peuvent inclure des sensations étranges, des mouvements involontaires d'une partie du corps, des troubles de la perception ou des comportements inhabituels. Les crises focales peuvent parfois se généraliser et se propager à l'ensemble du cerveau, devenant ainsi des crises généralisées. Ces distinctions sont importantes pour le diagnostic et le traitement de l'épilepsie, car elles permettent de déterminer l'origine des crises et d'adapter les stratégies thérapeutiques en conséquence.
B Épilepsies
Maladies cérébrales chroniques définies par l’association des trois caractéristiques suivantes :
- • la survenue d’au moins une crise épileptique cliniquement avérée;
- • une prédisposition durable à générer des crises;
- • leurs conséquences neurobiologiques, neuropsychologiques, sociales et psychiatriques.
En pratique, cette prédisposition cérébrale durable à générer des crises est établie par une ou plusieurs des trois caractéristiques suivantes :
- • la survenue d’au moins deux crises épileptiques cliniquement avérées non provoquées espacées d’au moins 24 heures;
- • l’identification d’un syndrome épileptique;
-
• la survenue d’une crise épileptique cliniquement avérée non provoquée et un risque estimé de récidive supérieur à 60 % dans les 10 ans, soit au moins un élément pathologique retrouvé :
- – présence d’anomalies paroxystiques à l’EEG,
- – lésion cérébrale préexistante épileptogène à l’imagerie,
- – trouble neurodévelopemental préexistant.
273En pratique, les épilepsies représentent un groupe hétérogène de maladies cérébrales chroniques qui peuvent débuter de la période néonatale jusqu’au grand âge, d’étiologies, de formes cliniques et de pronostics variables. Les épilepsies ont une prévalence en France de 0,5 à 1 % et une incidence de 0,5 pour 1 000 habitants par an.
II Diagnostic positif des crises épileptiques
A Crises généralisées
Les crises généralisées sont classées en fonction de la prédominance de signes moteurs ou de troubles de la conscience :
-
• les signes moteurs lorsqu’ils sont présents sont d’emblée bilatéraux et symétriques. Ils peuvent être :
- – toniques : contractions musculaires segmentaires des agonistes et antagonistes, soutenues,
- – cloniques : mouvements rythmiques soutenus résultant de secousses musculaires seg-mentaires répétitives et rythmiques,
- – tonicocloniques : succession dans le temps d’une phase tonique et d’une phase clonique,
- – atoniques : interruption brève et soudaine du tonus de tout ou partie du corps,
- – myocloniques : mouvement isolé ou en courte salve résultant d’une contraction musculaire isolée ou en courte salve,
- • les troubles de conscience : de durée variable, quelques secondes au cours d’une absence à quelques minutes en cas de crise tonicoclonique.
1 Classification des crises généralisées
L’identification des signes cliniques principaux permet de classer les crises généralisées :
- • avec signes moteurs au premier plan : par exemple, les crises tonicocloniques, les crises myocloniques,
- • avec altération de la conscience au premier plan : par exemple, les absences typiques.
2 Présentation clinique de quelques crises généralisées
a Crise généralisée tonicoclonique (vidéo 16.1)
Elle se déroule en trois phases successives :
-
• la phase tonique (20 à 30 secondes) comporte :
- – une vocalisation,
- – une abolition de la conscience,
- – une contraction tonique soutenue axiale et des membres,
- – une apnée avec cyanose,
- – des troubles végétatifs importants (tachycardie, augmentation de la tension artérielle, mydriase, rougeur du visage, hypersécrétion bronchique et salivaire),
- – une morsure latérale de langue fréquente;
-
• la phase clonique (20 à 30 secondes) comporte :
- – une persistance de l’abolition de conscience,
- – des secousses bilatérales, synchrones, intenses, s’espaçant progressivement;
-
• la phase résolutive (ou post-critique) de quelques minutes comporte :
- – une persistance de l’altération profonde de la conscience, puis un réveil progressif marqué par une confusion parfois une agitation et dont le patient ne gardera 274pas de souvenir. Il existe un décalage temporel entre les premiers signes de réveil rapportés par les témoins oculaires et les premiers souvenirs plus tardifs rapportés par le patient (« premier souvenir dans l’ambulance ou au service d’accueil des urgences »),
- – une hypotonie généralisée,
- – une énurésie possible,
- – un stertor : la respiration reprend, ample, bruyante, gênée par l’hypersécrétion bronchique et salivaire. Il est important à ce stade de mettre le patient en position latérale de sécurité pour libérer les voies aériennes supérieures,
- – des céphalées, des courbatures, des douleurs en relation avec la morsure latérale de la langue, le traumatisme occasionné par la chute, voire avec une luxation d’épaule ou un tassement vertébral survenus au cours de la phase tonique. Ces derniers symptômes peuvent persister plusieurs heures, voire plusieurs jours, et sont très importants à rechercher à l’anamnèse et à l’examen clinique.
b Crise myoclonique
Elle est le seul type de crise généralisée sans trouble de la conscience; elle est caractérisée par :
- • une conscience préservée;
- • sa brièveté (< 1 seconde à quelques secondes);
-
• des secousses musculaires :
- – très brèves (< 200 ms),
- – saccadées,
- – isolées ou répétées en courtes salves,
- – avec lâchage ou projection de l’objet tenu (signe de la tasse de café), voire chute brutale si elle affecte les membres inférieurs.
Elles sont spontanées ou provoquées par des stimulations, en particulier une stimulation lumineuse intermittente.
Fréquentes immédiatement après le réveil, elles surviennent en pleine conscience (à distinguer des myoclonies physiologiques survenant à l’endormissement).
c Absence typique
Les absences typiques (vidéo 16.2) sont caractérisées par :
- • une altération complète de la conscience, avec immobilité, aréactivité à l’environnement;
- • un début et une fin brutaux;
- • une fixité, voire un plafonnement, du regard pendant quelques secondes;
- • une décharge paroxystique généralisée, bilatérale, symétrique et synchrone de pointes-ondes à 3 Hz, de début et fin brusques, de quelques secondes, interrompant une activité de fond normale à l’EEG.
B Crises focales
1 Pour comprendre : principe des corrélations anatomocliniques et classification des crises focales
a Début
Les crises focales (vidéo 16.3 ) comportent des signes ou symptômes focaux initiaux qui traduisent le dysfonctionnement de la zone corticale perturbée par la décharge épileptique initiale.
) comportent des signes ou symptômes focaux initiaux qui traduisent le dysfonctionnement de la zone corticale perturbée par la décharge épileptique initiale.
Ces signes ont une grande valeur localisatrice (voir les exemples plus bas).
b 275Pendant la crise
Cette zone épileptique initiale peut ensuite entraîner d’autres régions corticales qui lui sont connectées (propagation) provoquant d’autres signes et symptômes. La séquence temporelle des signes cliniques reflète la séquence d’implication des régions corticales par la décharge épileptique.
c Après la crise
Les signes post-critiques témoignent de l’épuisement des régions corticales qui ont été impliquées par la décharge (hémiparésie controlatérale si implication du cortex moteur primaire par exemple, aphasie si implication des régions du langage, etc.).
En 2017, la Ligue internationale contre l’épilepsie a proposé de classer les crises focales selon la présence ou non d’un trouble de la conscience et le signe clinique initial prédominant :
- • moteur (de nature tonique ou atonique, clonique, myoclonique; spasmes; automatismes; hyperkinétique);
- • non moteur (de type sensoriel, émotionnel, cognitif; arrêt comportemental; dysautonomique). Cette classification forcément simplificatrice est en constante évolution.
2 En pratique : valeur localisatrice de quelques signes rencontrés au cours des crises focales
a Signes moteurs élémentaires (clonies unilatérales, myoclonies unilatérales, contraction tonique unilatérale d’un membre ou de la face)
- • Ils traduisent une implication des régions motrices primaires controlatérales (aussi appelées région centrale).
- • leur progression reflète l’organisation somatotopique du cortex moteur primaire (évolution ascendante le long du membre supérieur jusqu’à l’hémiface; on parle aussi de marche bravais-jacksonienne).
b Signes sensitifs ou sensoriels
Ces signes peuvent être des hallucinations (perceptions sans objet) ou des illusions (perceptions déformées), rapportées et critiquées par le patient; ils peuvent concerner toutes les modalités sensorielles, par exemple, la modalité :
- • somatosensitive : paresthésies avec progression reflétant l’organisation somatotopique du cortex somatosensitif primaire, controlatérales à la décharge, débutant au niveau de la main et d’évolution ascendante le long du membre supérieur jusqu’à l’hémiface. On parle également de « marche bravais-jacksonienne »;
- • visuelle : les hallucinations visuelles élémentaires positives (flashs lumineux localisés dans un hémichamp visuel) traduisent une implication du cortex visuel primaire dans le lobe occipital;
- • auditive : les hallucinations auditives élémentaires à type d’acouphènes (bourdonnement, sifflement) traduisent une implication par la décharge épileptique du cortex auditif primaire (gyrus temporal supérieur) controlatéral.
c Signes végétatifs
Troubles du rythme cardiaque, sensation de froid ou de chaleur, de soif, hypersalivation, sensation épigastrique ascendante ont une origine temporale interne ou insulaire.
d 276Signes cognitifs
Ils sont inconstants, mais peuvent avoir une valeur localisatrice :
- • état de rêve (réminiscence en pleine conscience), sensation de déjà-vu, de déjà-vécu rapportés par le patient ont une origine temporale interne (hippocampique);
- • les troubles phasiques paroxystiques reflètent une implication du lobe temporal de l’hémisphère dominant (gauche dans la majorité des cas).
Phénoménologie clinique des crises temporales internes
Elles comportent :
- • des sensations subjectives initiales végétatives (sensation épigastrique ascendante, sensation de chaleur), émotionnelles (angoisse) et/ou mnésiques (illusion de déjà-vu, état de rêve);
- • un trouble de la conscience qui est inconstant et secondaire;
- • des automatismes de mâchonnement;
- • des automatismes gestuels élémentaires répétitifs (émiettement, manipulation);
- • une durée prolongée supérieure à une minute;
- • les généralisations tonicocloniques secondaires sont exceptionnelles sous traitement.
Phénoménologie clinique des crises de la région centrale
Paresthésies et/ou clonies unilatérales débutant typiquement au niveau de la main avec une progression ascendante le long du membre supérieur puis implication de la face (marche bravais-jacksonienne). Ces signes sensitivo-moteurs sont controlatéraux à la zone corticale impliquée dans la crise.
III Classification et diagnostic syndromique
Un syndrome se définit comme une association non fortuite de signes élémentaires cliniques, voire paracliniques. L’identification du syndrome épileptique permet en effet d’orienter la recherche étiologique, le choix du traitement antiépileptique, de formuler un pronostic évolutif de l’épilepsie et d’une éventuelle comorbidité psychiatrique ou cognitive associée.
A Principes de la classification syndromique
Les syndromes sont définis selon :
- • l’âge de début des crises;
- • le(s) type(s) de crise(s) prédominant(s);
- • l’EEG intercritique et critique;
- • le niveau de développement au début de la maladie (normal ou retard);
- • l’examen neurologique et neuropsychologique intercritique (normal, ou signes de focalisation dans les formes focales, ou troubles du développement dans les encéphalopathies épileptiques);
- • le résultat de l’IRM cérébrale (normale dans les épilepsies présumées génétiques);
- • le devenir.
B 277Quelques syndromes à connaître
1 Épilepsie–absence de l’enfant
- • Appartient aux épilepsies généralisées d’origine génétique présumée et pharmaco-sensibles (= idiopathique).
- • Âge de début : autour de 6 ans (jamais avant 2 ans ou après 13 ans).
- • Type de crise prédominant : absences typiques (jusqu’à 100 par jour).
- • Autres types de crises associés possibles : crises généralisées tonicocloniques, rares et tardives dans l’évolution, myoclonies.
- • Pas de retard de développement mais difficultés scolaires et troubles attentionnels possibles.
- • Pronostic : pharmaco-sensible dans 80 % des cas; possibilité d’arrêter le traitement après la puberté dans 60 % des cas.
-
• EEG : décharges de pointes-ondes généralisées synchrones à 3 cycles/seconde, favorisées par l’hyperpnée (fig. 16.2).
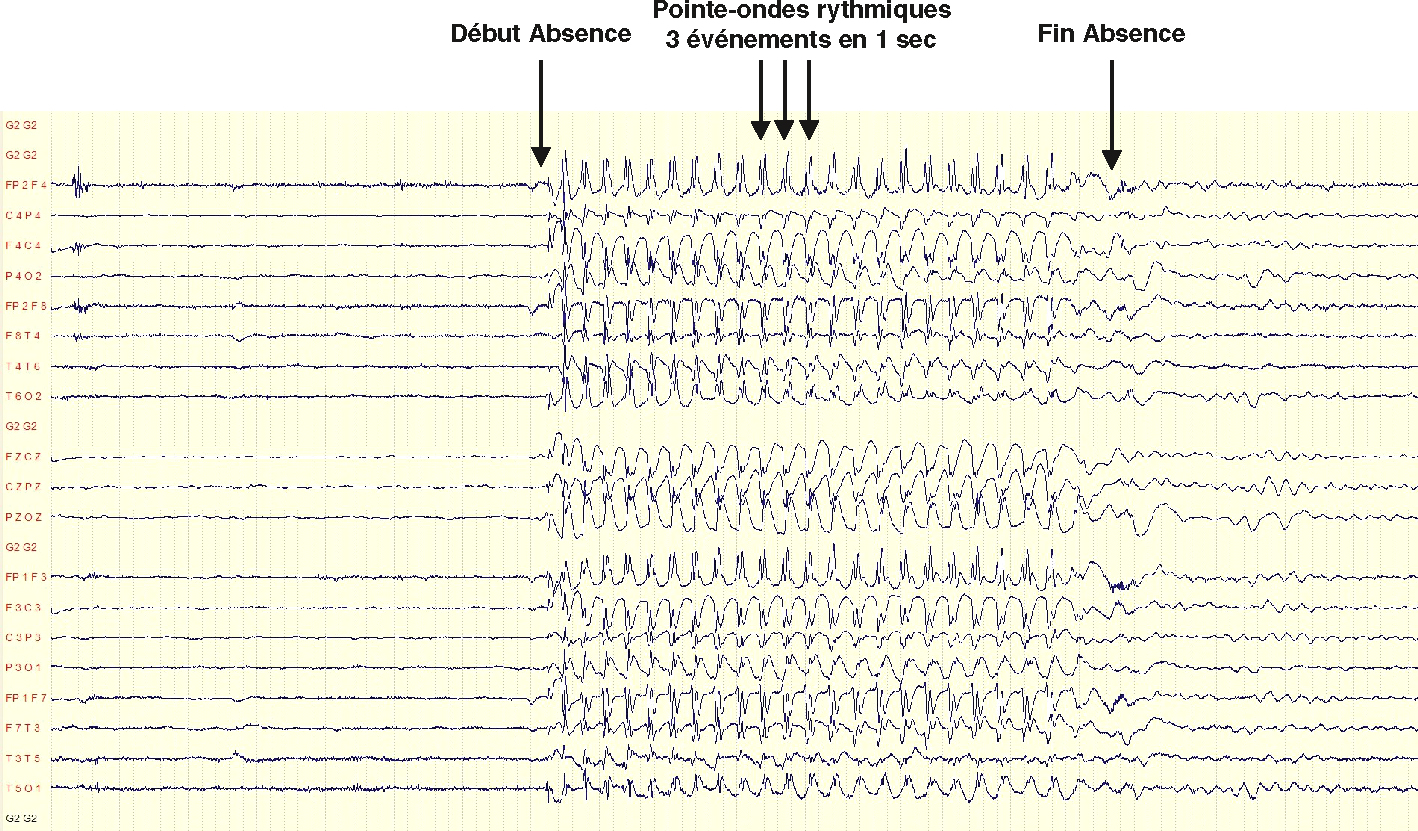
Fig. 16.2  Décharge de pointes-ondes généralisées synchrones à 3 Hz au cours d’une absence typique.
Décharge de pointes-ondes généralisées synchrones à 3 Hz au cours d’une absence typique.L'image montre un électroencéphalogramme (EEG) avec plusieurs canaux enregistrant l'activité électrique du cerveau. Les annotations en haut de l'image indiquent trois phases distinctes : "Début Absence", "Pointe-ondes rythmiques 3 événements en 1 sec", et "Fin Absence". Ces annotations marquent le début, le pic, et la fin d'une crise d'absence typique. Les pointes-ondes généralisées synchrones à 3 Hz sont visibles au milieu de l'enregistrement, caractérisées par des décharges rythmiques et régulières. Ces décharges sont typiques des crises d'absence, un type d'épilepsie où la personne perd brièvement conscience. Les pointes-ondes à 3 Hz signifient qu'il y a trois cycles de décharge par seconde, ce qui est une signature classique de ce type de crise. L'EEG montre clairement la transition entre l'activité cérébrale normale, l'apparition des pointes-ondes, et le retour à l'activité normale après la crise. Cette information est cruciale pour diagnostiquer et comprendre les crises d'absence, aidant ainsi les professionnels de la santé à fournir un traitement approprié.
2 Épilepsie myoclonique juvénile
- • Appartient aux épilepsies généralisées d’origine génétique présumée et pharmaco-sensibles (= idiopathique).
- • Âge de début : adolescence.
- • Type de crise prédominant : crises myocloniques matinales, souvent photosensibles.
- • Autres types de crises associées possibles : crises généralisées tonicocloniques, absences.
- • Pas de retard de développement, mais difficultés scolaires et troubles attentionnels possibles.
- • Pronostic : pharmaco-sensibles dans 80 % des cas, mais pharmaco-dépendance à l’âge adulte (il est rarement possible d’arrêter le traitement antiépileptique).
-
• EEG : bouffées de polypointes-ondes généralisées synchrones, favorisées par la stimulation lumineuse intermittente (fig. 16.3).
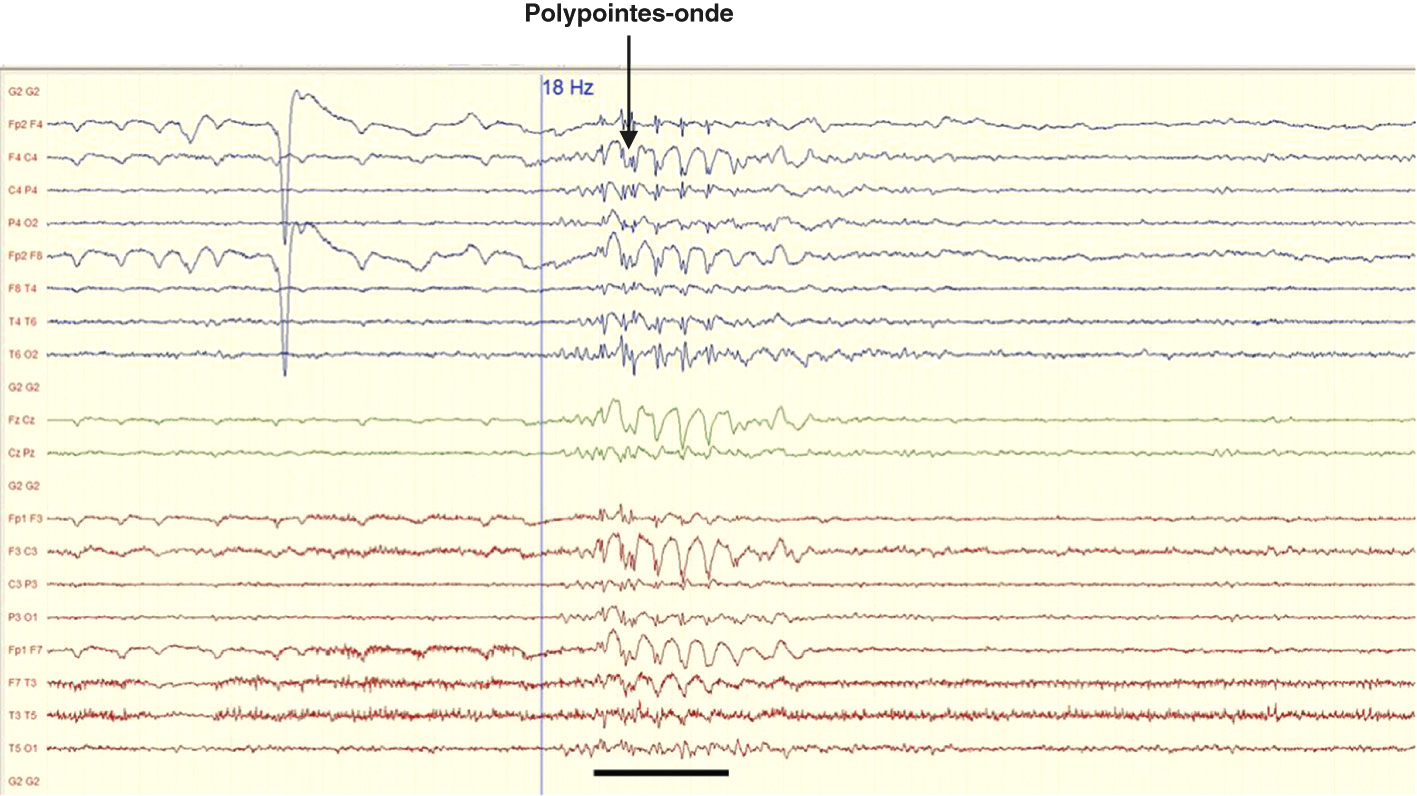
Fig. 16.3  Brève bouffée de polypointes-ondes généralisées synchrones.
Brève bouffée de polypointes-ondes généralisées synchrones.L'image montre un enregistrement d'électroencéphalogramme (EEG) avec plusieurs canaux représentant l'activité électrique du cerveau. Chaque ligne correspond à un canal différent, étiqueté par des abréviations telles que Fp1, Fp2, F7, F8, etc. L'EEG montre une brève bouffée de polypointes-ondes généralisées synchrones. Cela signifie qu'il y a une activité électrique anormale qui se produit simultanément dans plusieurs régions du cerveau. Cette activité est caractérisée par des pointes multiples suivies d'ondes lentes, visibles sur plusieurs canaux de l'EEG. La fréquence de cette activité est indiquée comme étant de 18 Hz. Cette information est importante car elle peut aider à diagnostiquer et comprendre certains types de troubles neurologiques, tels que l'épilepsie. L'enregistrement EEG permet de visualiser cette activité anormale et de fournir des informations cruciales pour l'évaluation des patients présentant des symptômes de crises épileptiques.
3 278Épilepsie avec crises tonicocloniques seules
- • Appartient au groupe des épilepsies généralisées d’origine génétique présumée et pharmaco-sensibles (= idiopathique).
- • Âge de début : adolescence, adulte.
- • Un seul type de crise exclusif par définition : crise généralisée tonicoclonique, favorisée par le manque de sommeil, l’alcool.
- • Pas de retard de développement, mais difficultés scolaires et troubles attentionnels possibles.
- • EEG : pointes-ondes et pointes généralisées.
- • Pronostic : pharmaco-sensible dans 90 % des cas à condition que les règles d’hygiène concernant le sommeil et l’alcool soient bien respectées.
4 Syndrome de West
- • Encéphalopathie épileptique liée à l’âge qui appartient aux groupes des épilepsies avec crises généralisées ou avec crises focales ou de début inconnu, et dont les étiologies peuvent également être diverses (génétique, structurelle…).
- • Âge de début : 6 mois.
- • Un type de crise prédominant : les spasmes en flexion.
- • Défini par l’association avec une régression psychomotrice et une hypsarythmie à l’EEG.
- • Pronostic variable mais avec un risque élevé de pharmaco-résistance et de troubles permanents du développement.
5 Syndromes spéciaux : crise hyperthermique simple et crise hyperthermique compliquée
- • Souvent d’origine génétique.
- • Elles répondent à des critères diagnostiques très stricts.
- • Âge de début à 1 an ou plus.
- • Chez un enfant sans antécédent.
- • 279Crise survenant dans un contexte de fièvre > 37,5 °C sans autre facteur provoquant identifié (pas de trouble métabolique notamment), de type généralisé moteur, durant moins de 15 minutes, sans déficit post-critique, restant unique pour un épisode fébrile donné.
- • Si ces conditions sont remplies, il n’y a pas d’indication d’examen complémentaire, notamment pas d’EEG ni de PL et pas d’indication de traitement antiépileptique au long cours. La prévention se fait par un contrôle de l’hyperthermie.
- • Lorsque l’un de ces critères n’est pas rempli, on parle de crises hyperthermiques compliquées, qui justifient alors un bilan étiologique (EEG, PL) et un traitement antiépileptique de fond.
6 Épilepsie temporale médiale sur sclérose de l’hippocampe (Vidéo 16.4)
- • Antécédents de crises hyperthermiques compliquées.
- • Âge de début des premières crises non fébriles : 5 à 15 ans.
- • Types de crises prédominants : crises focales comportant des sensations subjectives végétatives (sensation épigastrique ascendante), émotionnelles (angoisse) et/ou mnésique (déjà-vu, état de rêve), un trouble de la conscience qui est secondaire, des automatismes de mâchonnement, des automatismes gestuels élémentaires (émiettement, manipulation), une durée prolongée supérieure à 1 minute; crise focale secondairement généralisée exceptionnelle sous traitement.
- • Pronostic : mauvais, avec pharmaco-résistance fréquente, mais accessible alors à un traitement chirurgical qui permet la guérison dans 70 % des cas.
-
• IRM : aspect de sclérose hippocampique unilatérale (fig. 16.4).
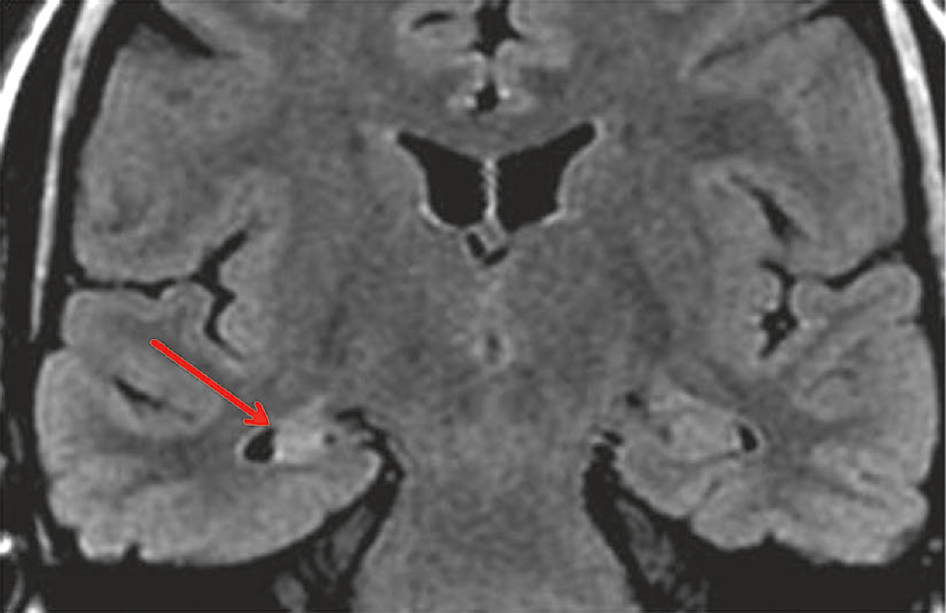
Fig. 16.4  IRM cérébrale en coupe coronale et séquence FLAIR montrant une atrophie associée à une sclérose (hypersignal) de l’hippocampe droit (flèche rouge).
IRM cérébrale en coupe coronale et séquence FLAIR montrant une atrophie associée à une sclérose (hypersignal) de l’hippocampe droit (flèche rouge).L'image montre une IRM cérébrale en coupe coronale utilisant la séquence FLAIR, qui permet de détecter des anomalies cérébrales en supprimant le signal du liquide céphalorachidien. Sur cette image, on observe une atrophie associée à une sclérose (hypersignal) de l'hippocampe droit, indiquée par une flèche rouge. L'hippocampe est une structure cérébrale cruciale pour la mémoire et l'orientation spatiale. L'atrophie signifie une réduction du volume de l'hippocampe, tandis que la sclérose désigne une zone de tissu durci ou cicatriciel, visible comme un hypersignal sur les séquences FLAIR. Cette combinaison d'atrophie et de sclérose est souvent associée à des conditions neurologiques comme l'épilepsie temporale médiale, où l'hippocampe est fréquemment affecté. La détection de ces anomalies par l'IRM est essentielle pour diagnostiquer et comprendre les troubles neurologiques, en visualisant précisément les altérations structurelles du cerveau. En résumé, l'IRM révèle une atrophie et une sclérose de l'hippocampe droit, fournissant des informations importantes pour l'évaluation des conditions neurologiques.
IV Diagnostic étiologique
Les crises épileptiques sont des symptômes. Les étapes diagnostiques comportant une description phénoménologique de la (des) crise(s) présentée(s) par le patient, l’identification du type de crise (focale, généralisée ou inconnue) puis du type d’épilepsie (focale, généralisée ou inconnue), puis l’identification du syndrome vont finalement orienter le diagnostic étiologique.
280Les causes des épilepsies sont classées dans cinq grandes catégories qui ne sont pas exclusives les unes des autres :
- • causes génétiques : 40 % des épilepsies, mais seules quelques-unes sont monogéniques et accessibles à un diagnostic génétique précis; les autres sont dites « génétiques présumées »; lorsqu’elles ont une évolution bénigne elles sont dites idiopathiques;
- • causes structurelles (lésionnelles) :
-
- – congénitales : malformations corticales, malformations vasculaires telles que les cavernomes,
- – ou acquises : post-traumatique, tumorale, vasculaire, dégénérative;
- • causes inflammatoires ou dysimmunes : encéphalites auto-immunes;
- • causes infectieuses : post-méningitique, post-encéphalitique;
- • causes métaboliques : génétiques ou acquises.
Lorsque aucune cause n’est suspectée ou identifiée, l’étiologie est dite « inconnue ».
La figure 16.5 synthétise le cadre de classification des épilepsies.
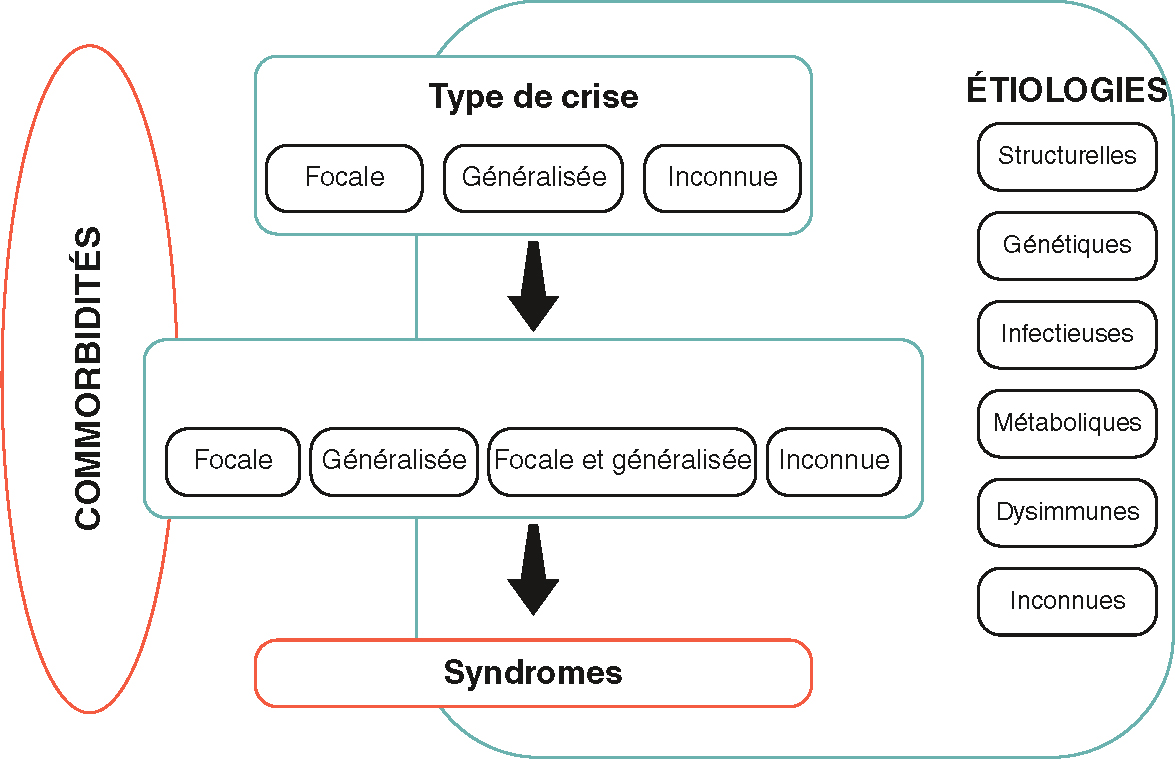
 Principes de la classification des épilepsies.
Principes de la classification des épilepsies. Illustration de Carole Fumat.
La classification des épilepsies repose sur plusieurs principes clés. D'abord, il est crucial de distinguer le type de crise : focale, généralisée ou inconnue. Les crises focales commencent dans une zone spécifique du cerveau, tandis que les crises généralisées affectent les deux hémisphères dès le début. Les crises inconnues ont une origine indéterminée. Ensuite, on classe le type d'épilepsie : focale, généralisée, focale et généralisée, ou inconnue. L'épilepsie focale concerne les crises localisées. L'épilepsie généralisée touche tout le cerveau. L'épilepsie focale et généralisée combine les deux types. L'épilepsie inconnue a un type non identifié. Les étiologies ou causes des épilepsies sont structurelles, génétiques, infectieuses, métaboliques, dysimmunes ou inconnues. Les causes structurelles sont des anomalies physiques ; les génétiques, des mutations héréditaires ; les infectieuses, des infections ; les métaboliques, des troubles du métabolisme ; les dysimmunes, des dysfonctionnements immunitaires ; les causes inconnues ne sont pas déterminées.
V Démarche diagnostique
Différentes étapes sont nécessaires pour établir le diagnostic (fig. 16.6).
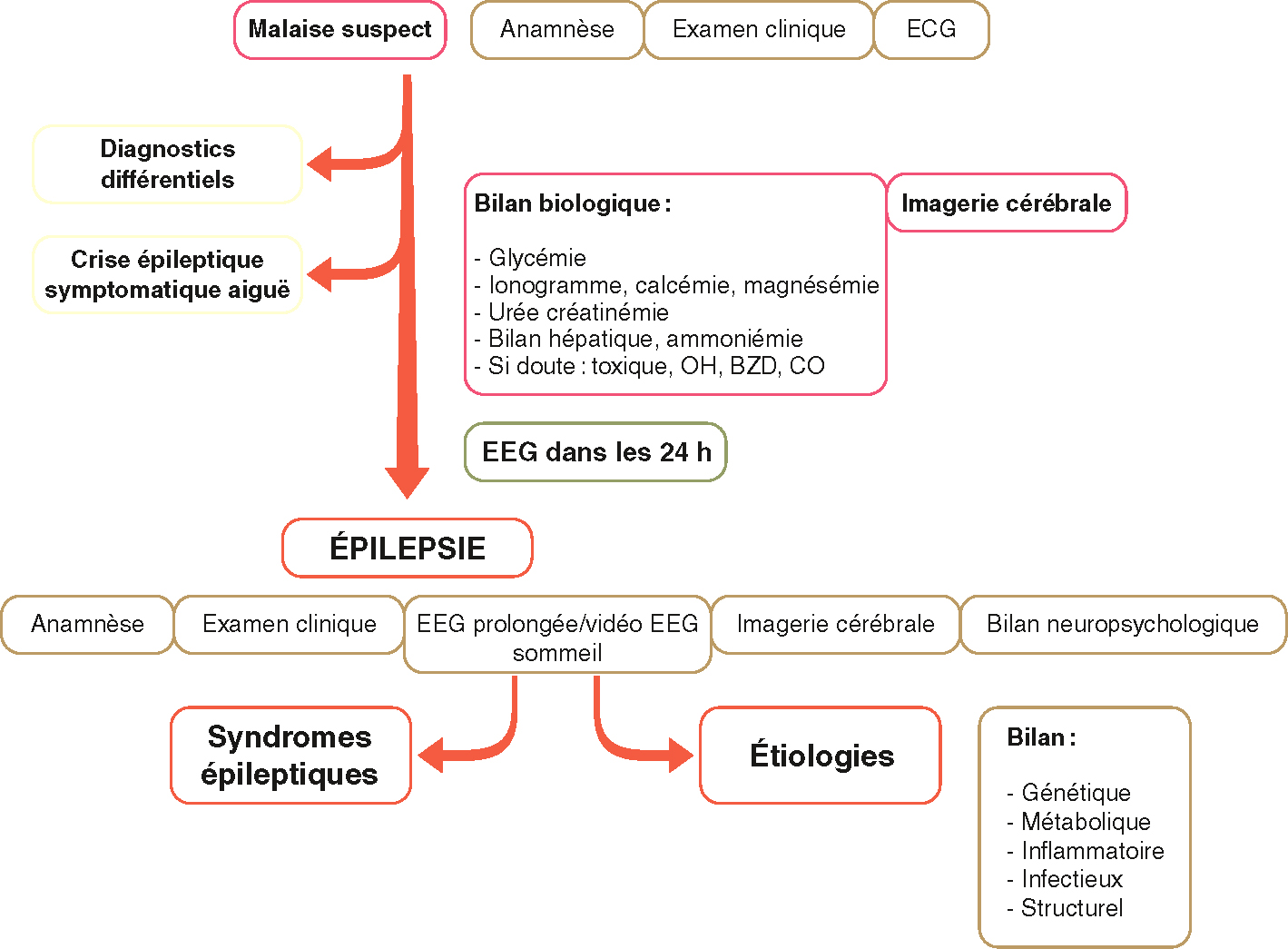
 Étapes nécessaires au diagnostic positif d’une épilepsie.
Étapes nécessaires au diagnostic positif d’une épilepsie. Illustration de Carole Fumat.
Pour diagnostiquer positivement une épilepsie, plusieurs étapes sont nécessaires. Tout d'abord, en cas de malaise suspect, il est important de réaliser une anamnèse, un examen clinique et un ECG. Ensuite, il faut envisager des diagnostics différentiels et évaluer la possibilité d'une crise épileptique symptomatique aiguë. Un bilan biologique est alors requis, comprenant des tests de glycémie, ionogramme, calcémie, magnésémie, urée, créatininémie, bilan hépatique et ammoniémie. Si une intoxication est suspectée, des tests pour détecter des substances toxiques, de l'alcool, des benzodiazépines ou du monoxyde de carbone doivent être effectués. Une imagerie cérébrale est également nécessaire. Un EEG doit être réalisé dans les 24 heures suivant le malaise suspect. Si l'épilepsie est confirmée, des étapes supplémentaires incluent une anamnèse, un examen clinique, un ECG prolongé ou une vidéo EEG de sommeil, une imagerie cérébrale et un bilan neuropsychologique. Les syndromes épileptiques et les étiologies doivent être identifiés, en tenant compte des bilans génétique, métabolique, inflammatoire, infectieux et structurel.
A 281Étape 1 – Diagnostic positif d’une crise d’épilepsie non symptomatique aiguë
La première étape consiste en la confirmation de la nature épileptique du malaise initial et de son caractère non provoqué (vidéo 16.5). Est exclue de fait, de ce chapitre, la prise en charge des crises symptomatiques aiguës (crises sur lésion cérébrale aiguë, troubles métaboliques ou toxiques…). Cette première étape diagnostique est traitée dans le chapitre 32 – item 342. Il ne faut pas confondre avec cette étiologie symptomatique aiguë d’éventuels facteurs précipitants de la crise initiale tels que la privation de sommeil, la stimulation lumineuse intermittente.
B Étape 2 – Diagnostic différentiel d’une crise d’épilepsie
Les erreurs diagnostiques sont fréquentes à cette étape. Les pathologies « mimant » une crise d’épilepsie sont fréquentes et parfois graves.
Devant une suspicion de crise généralisée tonicoclonique, principalement deux autres diagnostics peuvent être discutés (voir chapitre 30 – item 342) :
- • la syncope convulsivante :
- • la crise non épileptique psychogène (CNEP) aussi appelée crise fonctionnelle dissociative. Devant une suspicion de crise focale, peuvent être discuter les diagnostics différentiels suivants :
-
• aura migraineuse :
- – marche migraineuse plus progressive et plus longue qu’une crise épileptique : sur une période de 5 à 60 minutes,
- – 282succession plus ou moins complète d’hallucinations visuelles à type de phosphènes, puis troubles sensitifs à type de paresthésies latéralisées, puis de troubles phasiques (manque du mot, paraphasies…),
- – les céphalées apparaissent en fin de séquence et peuvent alors persister plusieurs heures;
-
• accident ischémique transitoire :
- – fréquent contexte de facteurs de risque cardiovasculaire,
- – déficit neurologique transitoire correspondant à un territoire vasculaire avec imagerie normale;
-
• malaise hypoglycémique :
- – contexte de diabète, intoxication à l’insuline…; des phénomènes déficitaires neurologiques jusqu’au coma peuvent être observés durant une hypoglycémie sévère,
- – phénomènes hyperadrénergiques associés : agitation, tremblements, sueurs, tachycardie, hypertension,
- – symptômes corrigés par le resucrage;
- • crise non épileptique psychogène.
C Étape 3 – Diagnostic positif d’une épilepsie
Cette étape consiste à réunir les arguments en faveur de l’existence d’une prédisposition cérébrale durale à générer des crises (voir plus haut I. Définitions) associée à la crise épileptique initiale.
Il convient donc de mener une enquête précise :
-
• anamnèse :
- – recherche d’événements antérieurs suspects de crises passées inaperçues (par exemple, myoclonies, absences, pertes de connaissance itératives, épisodes de morsure de langue ou de perte d’urines nocturnes.);
- • examen neurologique intercritique : recherche de signes de focalisation, retard des acquisitions;
-
• imagerie cérébrale :
- – recherche d’une lésion épileptogène, en dehors de syndromes d’origine génétique bien identifiés,
- – repose sur l’IRM encéphalique, qui est systématique,
- – elle peut être réalisée en différé si un scanner cérébral a déjà été réalisé lors de la prise en charge en aigu de la crise;
-
• un EEG :
- – recherche des éléments paroxystiques épileptiques : leur présence permet d’affirmer de façon rétrospective l’origine épileptique d’une crise suspectée cliniquement.
D Étape 4 – Diagnostic syndromique et étiologique
L’enquête étiologique et l’enquête syndromique s’effectuent de manière conjointe. Elles sont essentielles afin de guider le pronostic et la stratégie thérapeutique : certaines molécules peuvent aggraver des épilepsies de syndrome et/ou de cause spécifique (notamment génétiques et métaboliques).
Le diagnostic étiologique vise à rechercher les causes de l’épilepsie. Le diagnostic étiolo-gique est guidé par le diagnostic syndromique. Un syndrome épileptique regroupe les épilepsies 283présentant un profil clinique, paraclinique, pronostique et de réponse thérapeutique identique mais pouvant être associées à des étiologies distinctes.
Les diagnostics étiologique et syndromique reposent avant tout sur :
- • une anamnèse précise du patient et de son entourage afin de documenter les antécédents personnels et familiaux, l’histoire de la maladie épileptique :
-
-
–
 antécédents personnels :
antécédents personnels :- – souffrance fœtale aiguë à la naissance, crise convulsive fébrile dans l’enfance, notion de méningite ou d’encéphalite, traumatisme crânien sévère, retard des acquisitions psychomotrices, malformations congénitales, difficultés scolaires,
- – pathologies associées : surdité, pathologies auto-immunes, troubles psychiatriques…,
- – histoire de l’épilepsie : âge au début des crises; évolution du type, de la fréquence des crises et leur sémiologie; essais thérapeutiques; évolution cognitive et psychiatrique parallèlement à celle de l’épilepsie,
- – antécédents familiaux : notamment histoire familiale d’épilepsie;
-
- •
 un examen neurologique et général complet;
un examen neurologique et général complet; - •
 une IRM cérébrale avec recherche d’une lésion épileptogène (par exemple, séquelles vasculaires ou traumatiques, malformation de développement cortical, sclérose hippocam-pique, cavernome…);
une IRM cérébrale avec recherche d’une lésion épileptogène (par exemple, séquelles vasculaires ou traumatiques, malformation de développement cortical, sclérose hippocam-pique, cavernome…); -
•
 un enregistrement EEG, si besoin complété d’un enregistrement vidéo-EEG prolongé avec sommeil :
un enregistrement EEG, si besoin complété d’un enregistrement vidéo-EEG prolongé avec sommeil :- –
 identification des éléments paroxystiques intercritiques,
identification des éléments paroxystiques intercritiques, - – parfois des crises électrocliniques au repos ou lors des manœuvres d’activation (hyperp-née, stimulation lumineuse intermittente);
- –
-
•
 un bilan neuropsychologique :
un bilan neuropsychologique :- –
 recherche d’une atteinte cognitive spécifique associée à la symptomatologie des crises, comorbidité dépendante du diagnostic étiologique et syndromique;
recherche d’une atteinte cognitive spécifique associée à la symptomatologie des crises, comorbidité dépendante du diagnostic étiologique et syndromique;
- –
-
•
 un bilan complémentaire si nécessaire :
un bilan complémentaire si nécessaire :- –
 étiologie auto-immune : PL pour analyse du LCS (cellules, protéinorachie, recherche de bandes oligoclonales, anticorps antineuronaux et antineuropiles); bilan sanguin auto-immun; TEP au fluorodésoxyglucose (FDG) cérébrale;
étiologie auto-immune : PL pour analyse du LCS (cellules, protéinorachie, recherche de bandes oligoclonales, anticorps antineuronaux et antineuropiles); bilan sanguin auto-immun; TEP au fluorodésoxyglucose (FDG) cérébrale; - – étiologie métabolique : à adapter selon les cas (glycorachie, lactates et pyruvate dans le LCS, etc.);
- – enquête génétique : si des éléments de l’anamnèse, cliniques et paracliniques, orientent vers une origine monogénique possible (notamment si épilepsie associée à des troubles importants du développement cognitif).
- –
![]() La synthèse diagnostique initiale doit être réalisée par un spécialiste neurologue ou neuropédiatre.
La synthèse diagnostique initiale doit être réalisée par un spécialiste neurologue ou neuropédiatre.
VI Diagnostic de gravité : l’état de mal épileptique généralisé tonicoclonique, une urgence vitale
- • Définition physiopathologique : « crise épileptique qui persiste suffisamment longtemps ou qui se répète à des intervalles suffisamment brefs pour créer une condition épileptique stable et durable » (H. Gastaut, 1967).
-
• Définition opérationnelle :
- – crises anormalement prolongées qui peuvent mettre en jeu le pronostic vital ou fonctionnel du patient;
- – 284la durée des crises étant variable selon le type de crise, la durée au-delà de laquelle le diagnostic d’état de mal épileptique est posé dépend du type de crise;
- – en ce qui concerne les crises tonicocloniques généralisées, un diagnostic d’état de mal épileptique est posé si les phases toniques et cloniques réunies durent plus de 5 minutes.
Le diagnostic est clinique et des mesures thérapeutiques urgentes s’imposent dès le diagnostic clinique posé car, s’il dure plus de 30 minutes, le pronostic vital et fonctionnel est engagé (hypotension artérielle et collapsus, hypoxie, rhabdomyolyse, atteinte multiviscérale, ischémie cérébrale).
Pour les autres formes d’état de mal (non convulsif, d’expression confusionnelle), la durée au-delà de laquelle le diagnostic peut être posé est variable, entre 10 et 30 minutes. De même, la mise en jeu du pronostic vital et fonctionnel est retardée et le diagnostic plus difficile : dans ces cas, l’urgence est de faire un diagnostic précis (en évitant le surdiagnostic). Celui-ci repose sur une analyse clinique fine corrélée à la réalisation d’un EEG en urgence.
VII Principes thérapeutiques
A Conduite à tenir en présence d’une crise généralisée tonicoclonique
- • Noter l’heure de début (afin de pouvoir en déterminer la durée qui conditionne le diagnostic de gravité de l’état de mal épileptique).
- • Libérer les voies aériennes supérieures (ne pas introduire les doigts ou tout objet).
- • Position latérale de sécurité (participe à libérer les voies aériennes supérieures, prévient une pneumopathie d’inhalation en cas de vomissements).
-
• En pré-hospitalier :
- – s’il s’agit d’une crise habituelle chez un patient épileptique connu et traité, pas d’hospitalisation systématique;
- – s’il s’agit d’une première crise, ou d’une crise inhabituelle, ou si la durée est supérieure à 5 minutes, appel du 15 pour prise en charge au service d’accueil des urgences (SAU).
- • Au SAU, pas de traitement antiépileptique systématique en l’absence d’état de mal épileptique.
B Prise en charge médicamenteuse :
indication d’un traitement antiépileptique de fond
Est-il nécessaire d’introduire un traitement antiépileptique de fond ?
- • Il s’agit d’une question fondamentale.
- • Un traitement antiépileptique ne doit pas être commencé de manière systématique devant toute première crise d’épilepsie.
- • Seuls les patients présentant un risque de récidive élevé de crises à long terme doivent être traités.
- • En l’absence de tels critères, il n’existe aucune indication de traitement antiépileptique même temporaire (par exemple, benzodiazépines).
- • Les patients pour lesquels une épilepsie a été diagnostiquée sont par définition à haut risque de récidive.
- • L’introduction d’un traitement doit cependant s’effectuer après une information claire, idéalement par un neurologue ou un neuropédiatre, et avec l’accord du patient. Ce dernier doit en comprendre les risques et bénéfices attendus.
C 285Prise en charge médicamenteuse de l’état de mal épileptique
L’état de mal épileptique est la seule indication d’un traitement antiépileptique urgent de la crise. Seul l’état de mal épileptique convulsif (généralisé tonicoclonique) a fait l’objet de recommandations d’experts (Société de réanimation de langue française et Société française de médecin d’urgence) actualisées en 2018.
Les principes de la prise en charge médicamenteuse sont résumés dans la figure 16.7.
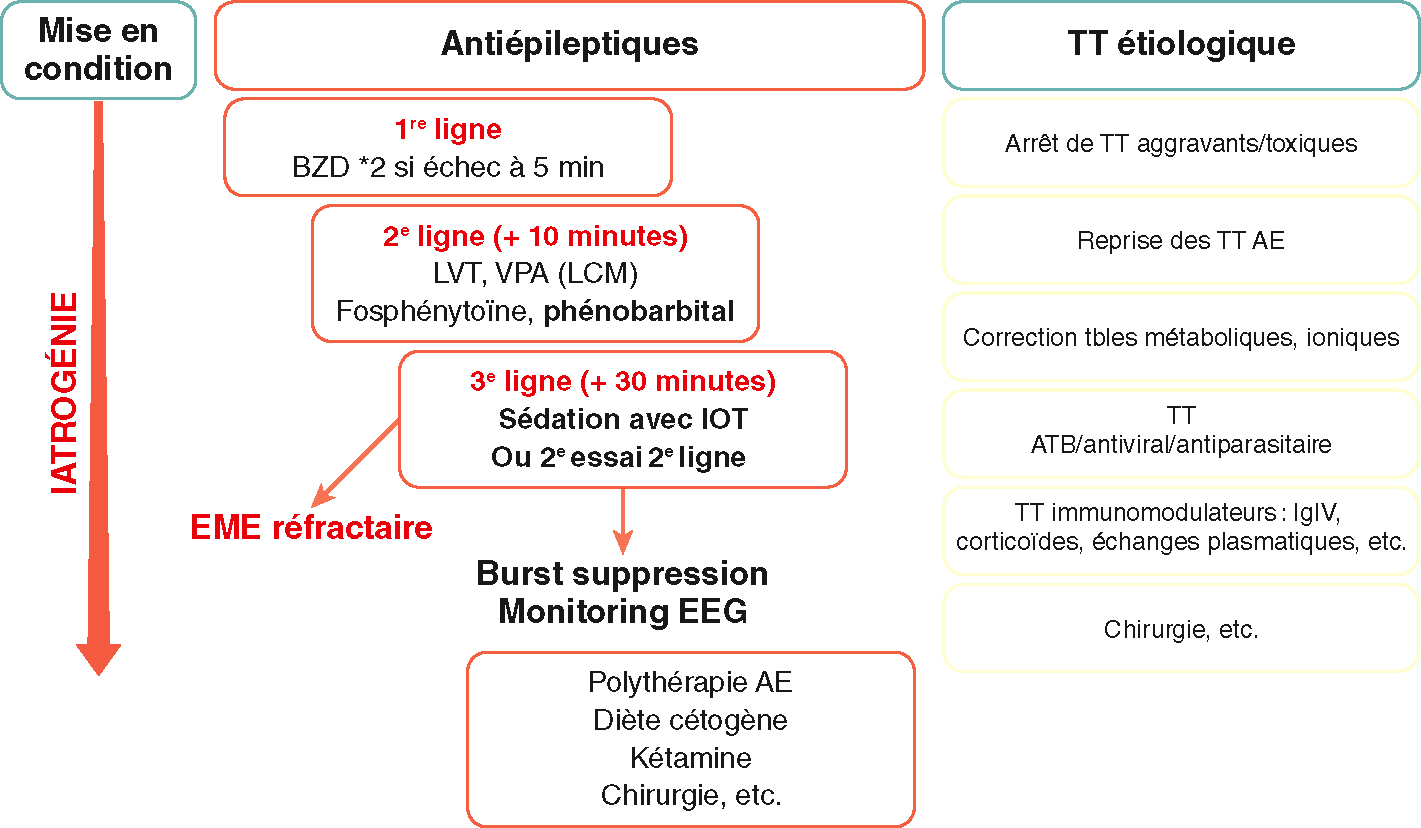
 Prise en charge médicamenteuse de l’état de mal épileptique.
Prise en charge médicamenteuse de l’état de mal épileptique. AE : antiépileptiques; EME : état de mal épileptique; LVT : lévétiracétam; VPA : acide valproïque; LCM : lacosa-mide; IOT : intubation orotrachéale; TT : traitement.
Illustration de Carole Fumat.
La prise en charge médicamenteuse de l’état de mal épileptique se divise en plusieurs étapes. Tout d'abord, il y a la mise en condition, qui est une étape iatrogène. Ensuite, on passe aux antiepileptiques, qui sont classés en trois lignes de traitement. La première ligne de traitement consiste en l'administration de benzodiazépines (BZD). Si cela échoue après 5 minutes, on passe à la deuxième ligne de traitement. La deuxième ligne de traitement, qui intervient après 10 minutes, inclut des médicaments tels que le lévétiracétam (LVT), le valproate (VPA), la lacosamide (LCM), le fosphénytoïne et le phénobarbital. Si ces traitements échouent, on passe à la troisième ligne de traitement après 30 minutes. Cette ligne inclut la sédation avec intubation orotrachéale (IOT) ou un deuxième essai de la deuxième ligne de traitement. En cas d'état de mal épileptique réfractaire, on utilise la suppression par bouffées et la surveillance par électroencéphalogramme (EEG). En parallèle, il y a le traitement étiologique qui comprend l'arrêt des traitements aggravants ou toxiques, la reprise des traitements antiepileptiques, la correction des troubles métaboliques et ioniques, et divers traitements spécifiques comme les antibiotiques, antiviraux, antiparasitaires, immunomodulateurs, immunoglobulines (IgIV), corticoïdes, échanges plasmatiques, et la chirurgie. Enfin, pour les cas réfractaires, des options supplémentaires incluent la polythérapie antiepileptique, le régime cétogène, la kétamine et la chirurgie.
1 En cas d’intervention avant 30 minutes
- 1.
 Première ligne de traitement : benzodiazepine en IV rapide (clonazepam 1 mg) répété une fois si échec au bout de 5 minutes.
Première ligne de traitement : benzodiazepine en IV rapide (clonazepam 1 mg) répété une fois si échec au bout de 5 minutes. - 2. Deuxième ligne de traitement : en cas d’échec 5 minutes après la deuxième injection de benzodiazépine, antiépileptique d’action prolongée en IV à la seringue électrique : fosphénytoïne (Prodilantin®) 20 mg/kg d’équivalent phénytoïne ou phénobarbital (Gardénal®) 15 mg/kg ou lévétiracétam 30–60 mg/kg < 4 g; acide valproïque 40 mg/kg et < 3 g en IV; lacosamide 200 mg de dose de charge.
- 3. Troisième ligne de traitement : si persistance de l’état de mal 30 minutes après l’administration de la deuxième ligne, sédation (propofol ou midazolam ou thiopental) avec intubation orotrachéale. Cette situation correspond à l’état de mal épileptique réfractaire.
![]() Toutefois, si l’intubation orotrachéale apparaît déraisonnable (limitation thérapeutique) ou s’il s’agit d’un patient ayant une épilepsie connue et que l’état de mal épileptique évolue depuis moins de 60 minutes, ou chez l’enfant, il est possible de retarder le coma thérapeutique et d’avoir recours à un autre antiépileptique de deuxième ligne en cas d’état de mal réfractaire.
Toutefois, si l’intubation orotrachéale apparaît déraisonnable (limitation thérapeutique) ou s’il s’agit d’un patient ayant une épilepsie connue et que l’état de mal épileptique évolue depuis moins de 60 minutes, ou chez l’enfant, il est possible de retarder le coma thérapeutique et d’avoir recours à un autre antiépileptique de deuxième ligne en cas d’état de mal réfractaire.
2 En cas d’intervention après 30 minutes
Benzodiazepine et antiépileptique d’action prolongée en IV de deuxième ligne.
3 286Dans tous les cas
- •
 Mise en condition du patient : libération des voies aériennes supérieures, oxygénothéra-pie, voie veineuse périphérique, surveillance en soins continus, voire en réanimation médicale (SaO2, fréquence cardiaque, fréquence respiratoire, tension artérielle, glycémie, ionogramme sanguin, pH).
Mise en condition du patient : libération des voies aériennes supérieures, oxygénothéra-pie, voie veineuse périphérique, surveillance en soins continus, voire en réanimation médicale (SaO2, fréquence cardiaque, fréquence respiratoire, tension artérielle, glycémie, ionogramme sanguin, pH). - • Traitement étiologique.
- • Mise en place rapide d’un traitement antiépileptique de relais de la dose de charge.
D Prise en charge non médicamenteuse chronique : informations à donner aux patients
![]() De manière toute aussi importante que le traitement médicamenteux, la prise en soins d’un patient épileptique repose sur une éducation complète.
De manière toute aussi importante que le traitement médicamenteux, la prise en soins d’un patient épileptique repose sur une éducation complète.
L’observance, la tolérance et l’efficacité thérapeutiques dépendent principalement de la qualité de cette information.
Plusieurs points doivent être abordés au cours des premières consultations :
1 Conseils sur l’observance thérapeutique
- • Importance d’être régulier dans les prises du traitement antiépileptique.
- • La mauvaise observance est l’une des principales causes de la persistance des crises sous traitement.
- • Cette observance sera facilitée si le choix de la molécule est adapté au rythme de vie du patient et à sa tolérance attendue.
- • Prévenir du danger d’état de mal épileptique en cas d’un arrêt intempestif des médicaments antiépileptiques.
2 Règles hygiénodiététiques
- • Favoriser un sommeil régulier.
-
• Éviter ou limiter les facteurs favorisants des crises :
- – dette de sommeil;
- – exposition prolongée aux écrans et jeux vidéo dans les épilepsies généralisées d’origine génétique photosensibles (5 % des épilepsies);
- – aliments ou drogues proconvulsivantes (cocaïne, héroïne, cannabis non appauvri en THC, prise d’alcool importante ou sevrage brutal, sevrage en benzodiazépines); éviter l’excès d’excitants tels que café, thé, Coca-Cola® non décaféiné;
- – certaines plantes qui sont à éviter, notamment sous forme d’huile essentielle (sauge, thym, eucalyptus, etc.) ou de gélule (millepertuis).
3 Risques domestiques
Prévenir le risque de traumatisme lors des crises : mobilier sans arêtes, literie basse, système limitant la température de l’eau chaude, protection des plaques de cuisson, éviter les bains non supervisés.
4 287Permis de conduire
- • La législation en vigueur dépend d’un arrêté dont la dernière mise à jour date du 28 mars 2022.
- • La décision d’aptitude est prise par un médecin agréé auprès de la préfecture, s’appuyant sur le certificat médical fourni par le neurologue traitant.
- • Dans le cadre d’une épilepsie nouvellement diagnostiquée, un délai d’un an sans crise est nécessaire avant d’accorder une première aptitude pour le permis B.
- • Bien expliquer au patient qu’en absence de validation de son aptitude par le médecin agréé, la conduite automobile est interdite.
- • Cette démarche doit être effectuée par le patient lui-même, le médecin étant tenu de l’informer de la législation.
- • Pour le permis poids lourd et de véhicule de transport en commun, la conduite n’est autorisée qu’après 10 ans de guérison sans récidive et sans aucun traitement.
5 Loisirs
- • Activités proscrites : plongée sous-marine, escalade sans sécurité, tir sportif, saut en parachute.
- • Activités à éviter en l’absence de contrôle de la maladie : baignade sans surveillance, équi-tation, activités en eau vive.
- • En cas de photosensibilité, limiter : jeux vidéo, écrans d’ordinateur, usage de la tablette et du téléphone dans le noir; soirées en boîte de nuit avec lumière stroboscopique. Des lunettes de soleil polarisantes peuvent être prescrites si la photosensibilité est handicapante.
6 Scolarité
- • La scolarité doit être maintenue en milieu normal autant que possible.
- • Un aménagement peut être proposé avec l’accord d’un tiers-temps pour les examens, l’aide d’une auxiliaire de la vie scolaire.
- • L’établissement d’un projet d’accueil individualisé (PAI) facilite cette insertion scolaire.
- • Une scolarité adaptée peut être envisagée selon la sévérité de la maladie et des comorbidités.
7 Activités professionnelles
Certaines activités professionnelles sont interdites aux personnes épileptiques même en cas de maladie bien contrôlée :
- • emploi nécessitant un port d’armes;
- • chauffeur professionnel (conducteur de poids lourds, de bus, d’ambulance…);
- • surveillant de baignade;
- • profession du bâtiment nécessitant de travailler en hauteur (charpentier couvreur…).
Dans ces cas, une reconversion professionnelle doit être envisagée le plus tôt possible.
Dans les autres cas, les situations sont variables et l’interlocuteur privilégié est le médecin du travail. Il faut encourager le patient à contacter ce dernier afin qu’un aménagement de poste puisse être effectué.
En cas d’inaptitude professionnelle, une demande de reconnaissance en qualité de travailleur handicapé (RQTH) doit être instruite.
8 Contraception
288Les traitements antiépileptiques inducteurs enzymatiques (tels que la carbamazépine) réduisent l’efficacité des contraceptifs oraux et en implants. Une alternative par dispositif intra-utérin ou contraception mécanique doit être proposée.
La prise d’une contraception orale par œstroprogestatifs peut conduire à une baisse d’efficacité de la lamotrigine. Il convient d’être prudent devant cette association et d’en avertir le neurologue traitant.
9 Grossesse
Toutes les femmes en âge de procréer, même en dehors d’un désir de grossesse imminent, doivent recevoir une information complète.
La grossesse est un événement qui conduit à des changements divers pouvant être responsables d’une aggravation de l’épilepsie.
La grossesse est un événement à préparer avec le neurologue traitant.
Il est essentiel d’assurer un équilibre optimisé des crises avant d’envisager une grossesse selon les règles suivantes :
- •
 limiter le nombre de molécules antiépileptiques;
limiter le nombre de molécules antiépileptiques; - • posologie minimale efficace si possible avec fractionnement des doses;
- • choisir une molécule antiépileptique efficace présentant le plus faible risque tératogène (actuellement le valproate de sodium et le topiramate sont interdits chez la femme enceinte sauf avis contraire d’un neurologue spécialisé en épileptologie);
- • prescrire de l’acide folique 3 mois avant la conception et durant le 1er trimestre de grossesse, afin de compenser les risques malformatifs du tube neural.
![]() Une surveillance échographique régulière devra être réalisée afin de dépister toutes malformations à la fin du 1er trimestre et durant l’ensemble de la grossesse.
Une surveillance échographique régulière devra être réalisée afin de dépister toutes malformations à la fin du 1er trimestre et durant l’ensemble de la grossesse.
289
 Compléments numériques
Compléments numériques
Des compléments numériques sont associés à ce chapitre. Ils proposent des vidéos indiquées dans le texte par un picto. Pour voir ces compléments, connectez-vous sur http://www.emconsulte/e-complement/478607 et suivez les instructions.
Vidéo 16.1. A Crise généralisée tonico-clonique (vidéo-EEG).
Source : vidéothèque du Collège des enseignants de neurologie (https://www.cen-neurologie.fr/videotheque).
Vidéo 16.2. A Absence typique (vidéo-EEG).
Source : vidéothèque du Collège des enseignants de neurologie (https://www.cen-neurologie.fr/videotheque).
Vidéo 16.3. A Crise partielle complexe (vidéo-EEG).
Source : vidéothèque du Collège des enseignants de neurologie (https://www.cen-neurologie.fr/videotheque).
Vidéo 16.4. A Crise partielle complexe (interrogatoire).
Source : vidéothèque du Collège des enseignants de neurologie (https://www.cen-neurologie.fr/videotheque).
Vidéo 16.5. A Interrogatoire par rapport à un malaise avec des convulsions.
Source : vidéothèque du Collège des enseignants de neurologie (https://www.cen-neurologie.fr/videotheque).
