Situations de départ
Symptômes ou signes cliniques
 27 Chute de la personne âgée.
27 Chute de la personne âgée.
 28 Coma et troubles de la conscience.
28 Coma et troubles de la conscience.
 31 Perte d’autonomie progressive.
31 Perte d’autonomie progressive.
 49 Ivresse aiguë.
49 Ivresse aiguë.
 50 Malaise perte de connaissance.
50 Malaise perte de connaissance.
 97 Rétention aiguë d’urines.
97 Rétention aiguë d’urines.
 114 Agitation.
114 Agitation.
 117 Apathie.
117 Apathie.
 118 Céphalées.
118 Céphalées.
 119 Confusion mentale/désorientation.
119 Confusion mentale/désorientation.
 120 Convulsions.
120 Convulsions.
 122 Hallucinations.
122 Hallucinations.
 124 Idées délirantes.
124 Idées délirantes.
 129 Troubles de l’attention.
129 Troubles de l’attention.
 131 Troubles de la mémoire/déclin cognitif.
131 Troubles de la mémoire/déclin cognitif.
 134 Troubles du langage et/ou phonation.
134 Troubles du langage et/ou phonation.
 390135 Troubles du sommeil, insomnie ou hypersomnie.
390135 Troubles du sommeil, insomnie ou hypersomnie.
 172 Traumatismes crâniens.
172 Traumatismes crâniens.
Données paracliniques
 183 Analyse du liquide cérébrospinal.
183 Analyse du liquide cérébrospinal.
 194 Analyse du bilan thyroïdien.
194 Analyse du bilan thyroïdien.
 199 Créatinine augmentée.
199 Créatinine augmentée.
 200 Dyscalcémie.
200 Dyscalcémie.
 202 Dysnatrémie.
202 Dysnatrémie.
 209 Hypoglycémie.
209 Hypoglycémie.
 226 Découverte d’une anomalie du cerveau à l’examen d’imagerie médicale.
226 Découverte d’une anomalie du cerveau à l’examen d’imagerie médicale.
 233 Identifier/reconnaître les différents examens d’imagerie.
233 Identifier/reconnaître les différents examens d’imagerie.
 236 Interprétation d’un résultat de sérologie.
236 Interprétation d’un résultat de sérologie.
Prise en charge aiguë et chronique
 247 Prescription d’une rééducation.
247 Prescription d’une rééducation.
 279 Consultation de suivi d’un patient ayant des troubles cognitifs.
279 Consultation de suivi d’un patient ayant des troubles cognitifs.
Prévention
 324 Modification thérapeutique du rythme de vie.
324 Modification thérapeutique du rythme de vie.
Situations diverses
 327 Annonce d’un diagnostic de maladie grave au patient et/ou à sa famille.
327 Annonce d’un diagnostic de maladie grave au patient et/ou à sa famille.
 345 Situation de handicap.
345 Situation de handicap.
 352 Expliquer un traitement au patient adulte.
352 Expliquer un traitement au patient adulte.
Objectifs pédagogiques
Item 108 – Confusion, démences
 Diagnostiquer un syndrome confusionnel, savoir évoquer un hématome sous-dural chronique.
Diagnostiquer un syndrome confusionnel, savoir évoquer un hématome sous-dural chronique.
 Diagnostiquer un syndrome démentiel, une maladie d’Alzheimer.
Diagnostiquer un syndrome démentiel, une maladie d’Alzheimer.
 Diagnostiquer un syndrome confusionnel chez le sujet âgé.
Diagnostiquer un syndrome confusionnel chez le sujet âgé.
Item 132 – Troubles cognitifs du sujet âgé
 Orientation diagnostique devant des troubles cognitifs du sujet âgé et principales causes.
Orientation diagnostique devant des troubles cognitifs du sujet âgé et principales causes.
 Connaître les principes de la prise en charge médicale et psychosociale d’un patient avec troubles neurocognitifs.
Connaître les principes de la prise en charge médicale et psychosociale d’un patient avec troubles neurocognitifs.
 Argumenter l’attitude thérapeutique et planifier le suivi du patient en abordant les problématiques techniques, relationnelles, éthiques, organisationnelles consécutives à l’évolution de la maladie.
Argumenter l’attitude thérapeutique et planifier le suivi du patient en abordant les problématiques techniques, relationnelles, éthiques, organisationnelles consécutives à l’évolution de la maladie.
Item 343 – État confusionnel et trouble de conscience chez l’adulte et chez l’enfant
 Diagnostiquer un état confusionnel et un trouble de la conscience.
Diagnostiquer un état confusionnel et un trouble de la conscience.
 Identifier les situations d’urgence et planifier leur prise en charge préhospitalière et hospitalière.
Identifier les situations d’urgence et planifier leur prise en charge préhospitalière et hospitalière.
Hiérarchisation des connaissances
Item 108 – Confusion, démences
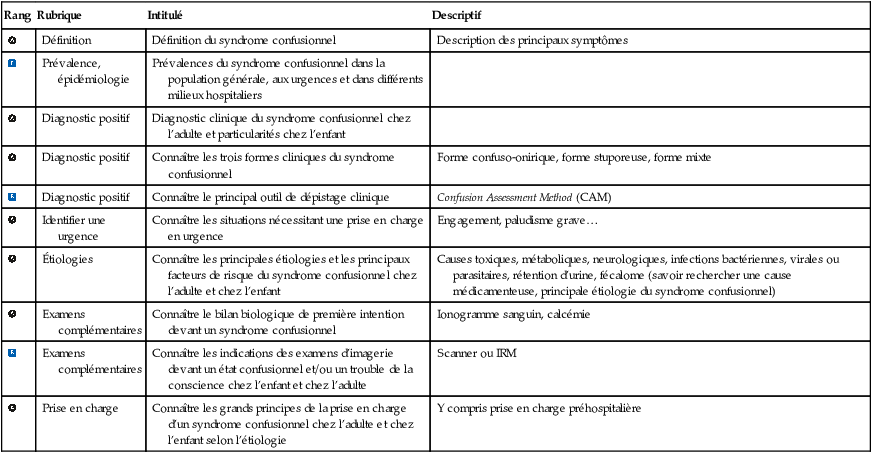
| Rang | Rubrique | Intitulé | Descriptif |
|---|---|---|---|
| Éléments physiopathologiques | Comprendre le mécanisme physiopathologique de la confusion mentale | ||
| Définition | Connaître la définition d’une confusion et d’une démence | Description des principaux symptômes | |
| Étiologies | Connaître les principales causes neurologiques de confusion mentale | Méningites, tumeurs, traumatismes, accident vasculaire cérébral, épilepsie | |
| Étiologies | Connaître les principales causes non neurologiques de confusion mentale | Toxiques, métaboliques, infectieuses | |
| Diagnostic positif | Savoir rechercher les causes de la confusion mentale | Démarche clinique : conduire l’examen clinique, décider de l’indication éventuelle d’une ponction lombaire ou d’un scanner cérébral | |
| Prise en charge | Connaître les principes de la prise en charge thérapeutique d’un patient confus | Faire les prescriptions d’urgence et traitement de la cause | |
| Éléments physiopathologiques | Connaître les principales lésions de la maladie d’Alzheimer (MA) | Perte des neurones, accumulation protéine amyloïde, accumulation protéine tau | |
| Diagnostic positif | Connaître les manifestations cliniques de la MA aux différentes phases | Phases prodromale, démentielle et de démence sévère | |
| Diagnostic positif | Connaître le profil des troubles de la mémoire de la MA | Trouble de la consolidation en mémoire épisodique | |
| Diagnostic positif | Connaître les principaux diagnostics différentiels de la MA | Confusion, causes fonctionnelles, causes organiques curables | |
| Prise en charge | Connaître les principes de prise en charge non médicamenteuse de la MA, y compris l’aide des réseaux ville–hôpital | Aides humaines et financières, hygiène de vie, iatrogénie | |
| Éléments physiopathologiques | Préciser les principes du raisonnement topographique devant un syndrome démentiel | Attention, fonctions d’intégration perceptive, mémoire et fonctions exécutives | |
| Examens complémentaires | Connaître les indications et les objectifs d’imagerie devant une démence ou une confusion | Démence : IRM cérébrale, à défaut TDM | |
| Examens complémentaires | Connaître la sémiologie en imagerie de l’hématome sous-dural (HSD) chronique | Collection extraparenchymateuse à contenu liquidien, parfois associée à un saignement récent, habituellement en forme de « croissant », limitée par les sinus duraux, et assez souvent bilatérale | |
| Contenu multimédia | Exemple HSD chronique sur une TDM | ||
| Examens complémentaires | Connaître la sémiologie en imagerie de l’hydrocéphalie chronique de l’adulte | ||
| Examens complémentaires | Connaître les indications des examens de médecine nucléaire dans les démences | Scintigraphie de perfusion cérébrale, scintigraphie des transporteurs de la dopamine, TEP au 18FDG |
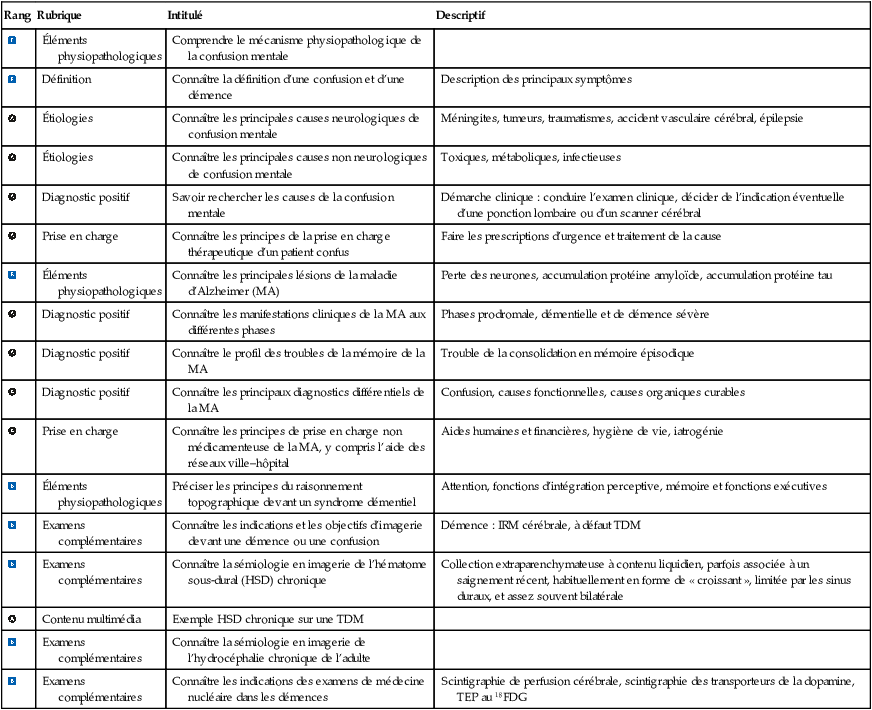
391Item 132 – Troubles cognitifs du sujet âgé
| Rang | Rubrique | Intitulé | Descriptif |
|---|---|---|---|
| Définition | Définition trouble neurocognitif | Définition du DSM-5 | |
| Diagnostic positif | Maladie d’Alzheimer | Connaître les éléments cliniques positifs qui permettent de poser le diagnostic | |
| Diagnostic positif | Encéphalopathie vasculaire | Connaître les éléments cliniques positifs qui permettent de poser le diagnostic | |
| Diagnostic positif | Maladie à corps de Lewy | Connaître les éléments cliniques positifs qui permettent de poser le diagnostic | |
| Diagnostic positif | Diagnostic différentiel de la maladie d’Alzheimer et des maladies apparentées | Connaître les maladies curables pouvant induire un trouble neurocognitif | |
| Étiologies | Connaître les causes principales d’un trouble neurocognitif | ||
| Examens complémentaires | Connaître les outils de repérage d’un trouble neurocognitif | Application en médecine générale | |
| Examens complémentaires | Connaître les examens de biologie à pratiquer devant un trouble neurocognitif | Application des critères HAS 2011 | |
| Prise en charge | Prise en charge médicale d’un patient avec trouble neurocognitif | Connaître les grandes lignes de la prise en charge médicale | |
| Prise en charge | Prise en charge psychosociale d’un patient avec trouble neurocognitif | Connaître les grandes lignes de la prise en charge psychosociale | |
| Diagnostic positif | Symptômes psychologiques et comportementaux des démences | Savoir identifier les principaux troubles du comportement associés aux maladies responsables d’un trouble neurocognitif | |
| Prise en charge | Démarche thérapeutique devant une agitation ou une agressivité dans un contexte de trouble neurocognitif | Connaître les grands principes de la prise en charge hiérarchisée, médico-psychosociale et médicamenteuse (voir item 347) | |
| Éléments physiopathologiques | Maladie d’Alzheimer | Connaître les grandes lignes de la physiopathologie de la maladie d’Alzheimer | |
| Diagnostic positif | Dégénérescence lobaire frontotemporale | Connaître les éléments cliniques positifs qui permettent de poser le diagnostic | |
| Examens complémentaires | Connaître les grandes lignes des résultats attendus de l’IRM devant un trouble neurocognitif | Application des critères HAS 2011 | |
| Contenu multimédia | Exemple HSD chronique sur une TDM (déjà dans l’item 108) |
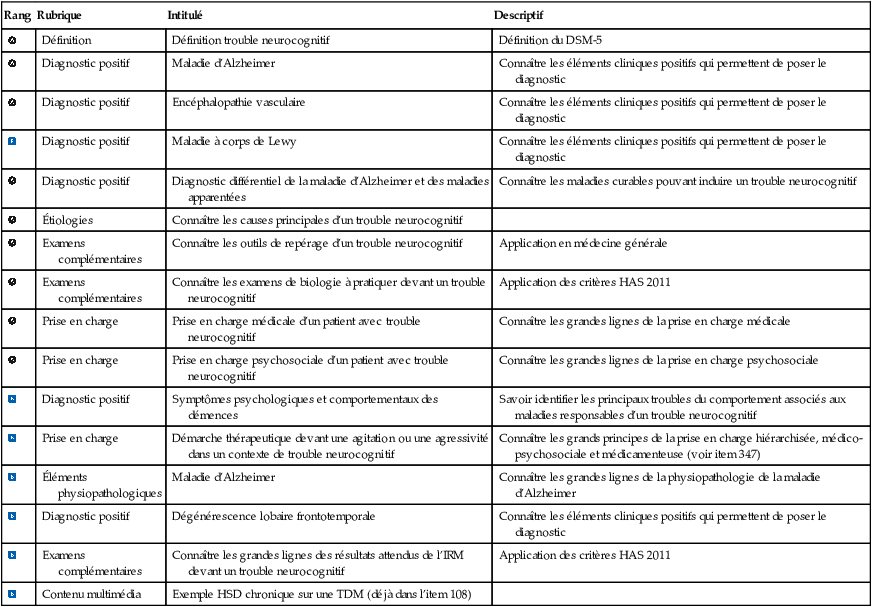
392Item 343 – État confusionnel et trouble de conscience chez l’adulte et chez l’enfant
| Rang | Rubrique | Intitulé | Descriptif |
|---|---|---|---|
| Définition | Définition du syndrome confusionnel | Description des principaux symptômes | |
| Prévalence, épidémiologie | Prévalences du syndrome confusionnel dans la population générale, aux urgences et dans différents milieux hospitaliers | ||
| Diagnostic positif | Diagnostic clinique du syndrome confusionnel chez l’adulte et particularités chez l’enfant | ||
| Diagnostic positif | Connaître les trois formes cliniques du syndrome confusionnel | Forme confuso-onirique, forme stuporeuse, forme mixte | |
| Diagnostic positif | Connaître le principal outil de dépistage clinique | Confusion Assessment Method (CAM) | |
| Identifier une urgence | Connaître les situations nécessitant une prise en charge en urgence | Engagement, paludisme grave… | |
| Étiologies | Connaître les principales étiologies et les principaux facteurs de risque du syndrome confusionnel chez l’adulte et chez l’enfant | Causes toxiques, métaboliques, neurologiques, infections bactériennes, virales ou parasitaires, rétention d’urine, fécalome (savoir rechercher une cause médicamenteuse, principale étiologie du syndrome confusionnel) | |
| Examens complémentaires | Connaître le bilan biologique de première intention devant un syndrome confusionnel | Ionogramme sanguin, calcémie | |
| Examens complémentaires | Connaître les indications des examens d’imagerie devant un état confusionnel et/ou un trouble de la conscience chez l’enfant et chez l’adulte | Scanner ou IRM | |
| Prise en charge | Connaître les grands principes de la prise en charge d’un syndrome confusionnel chez l’adulte et chez l’enfant selon l’étiologie | Y compris prise en charge préhospitalière |
I 393Pour comprendre
- • A Un trouble neurocognitif (TNC) est une réduction acquise, significative et évolutive des capacités dans un ou plusieurs domaines cognitifs. Ce déclin cognitif est persistant, non expliqué par une dépression ou des troubles psychotiques, souvent associé à un changement de comportement, de personnalité.
-
• La démence ou TNC majeur est un syndrome défini par la présence simultanée des deux critères suivants :
- – altération durable et acquise d’une ou plusieurs fonctions cognitives (ou fonctions intellectuelles : mémoire, attention, langage, gnosies, praxies, raisonnement, jugement, etc.) et/ou comportementales (personnalité, affects, régulation des conduites sociales, etc.);
- – les troubles ci-dessus sont suffisamment sévères pour entraîner, indépendamment des autres atteintes (de la motricité, par exemple), une altération de l’autonomie dans la vie quotidienne.
-
• Ce qui n’est pas une démence :
- – les affections de début brusque à leur phase aiguë : un accident vasculaire, une encé-phalopathie de Gayet-Wernicke (encéphalopathie aiguë carentielle), une méningo-encéphalite herpétique, etc.;
- – l’état confusionnel : début brusque, atteinte globale des fonctions cognitives, troubles de la vigilance, de physiopathologie différente;
- – les troubles cognitivo-comportementaux innés (retard mental, troubles du développement).
- • Il existe une gradation de la sévérité de la démence en fonction de son retentissement dans la vie quotidienne (légère, modérée et sévère).
- • Les causes des démences sont dominées par les maladies neurodégénératives (70 à 90 % des démences) et surtout par la maladie d’Alzheimer (plus de 70 % des démences neurodégénératives).
- •
 Les démences dégénératives sont des démences dont la cause n’est pas directement reliée à un mécanisme carentiel, métabolique, vasculaire, inflammatoire, tumoral, infectieux, toxique ou traumatique.
Les démences dégénératives sont des démences dont la cause n’est pas directement reliée à un mécanisme carentiel, métabolique, vasculaire, inflammatoire, tumoral, infectieux, toxique ou traumatique. - • La neurodégénérescence est un processus conduisant à la perte lente mais inexorable des cellules nerveuses. Il ne faut pas confondre la neurodégénérescence pathologique avec le vieillissement normal.
- • La première étape du diagnostic des démences repose sur le principe d’un regroupement des signes et symptômes en syndrome puis sur une interprétation topographique du syndrome, qui conditionne souvent le diagnostic étiologique. Il est donc indispensable d’avoir au minimum une représentation schématique des grandes fonctions cérébrales et 394de disposer de quelques outils cliniques de base permettant de tester ces grandes fonctions (encadrés 22.1 et 22.2).
-
• Le vieillissement normal peut entraîner un TNC n’entravant pas l’autonomie et touchant ce que l’on appelle les fonctions exécutives (encadré 22.1). Il s’agit principalement d’un léger trouble de la flexibilité de la pensée, d’une réduction de la vitesse de traitement des informations et d’une diminution des capacités d’attention divisée. La modestie de ces troubles et leur nature les distinguent des troubles cognitifs pathologiques associés aux maladies neurologiques. En outre, les résultats des tests psychométriques rendus au clinicien sont ajustés à l’âge et au niveau d’éducation.
- • La maladie d’Alzheimer étant de loin la cause la plus fréquente des démences du sujet âgé (mais aussi la plus fréquente de toutes les démences), elle constitue dans ce chapitre le modèle de description du syndrome démentiel.
II 395396Maladie d’Alzheimer
A Pour comprendre
-
• La maladie d’Alzheimer est un enjeu majeur de santé publique1 car :
- – elle touche environ un million de personnes en France; c’est la première cause de démence;
- – sa prévalence est liée à l’âge et est en augmentation régulière; elle touche 2 à 4 % de la population après 65 ans et atteint 15 % à 80 ans;
- – sa morbidité est majeure (perte d’autonomie pour le patient, souffrance pour les aidants);
- – son coût socio-économique est massif (soins chroniques très coûteux au domicile ou en institution).
-
• La cause de la maladie d’Alzheimer n’est pas identifiée, mais la cascade biologique conduisant à la mort progressive des neurones est de mieux en mieux connue (fig. 22.2 de l’encadré 22.3).
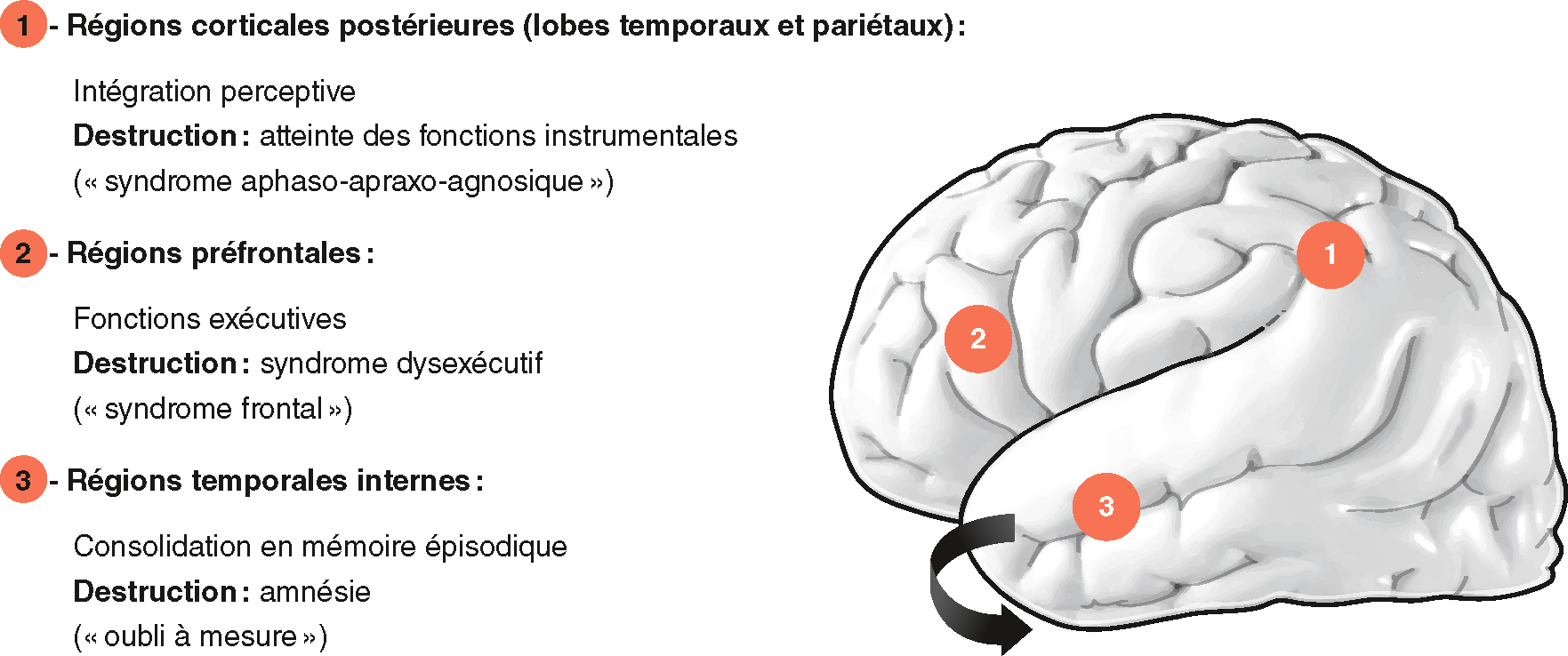
Fig. 22.1  Schéma (simplifié) d’organisation des fonctions intellectuelles.
Schéma (simplifié) d’organisation des fonctions intellectuelles.
1. Régions corticales postérieures (libres temporaux et pariétaux) : intégration perceptive; destruction : atteinte des fonctions instrumentales (« syndrome aphaso-apraxo-agnosique »). 2. Régions préfrontales : fonctions exécutives; destruction : syndrome dysexécutif (« syndrome frontal »). 3. Régions temporaires internes : consolidation en mémoire épisodique; destruction : amnésie (« oubli à mesure »).
Illustration de Carole Fumat.Le schéma simplifié d’organisation des fonctions intellectuelles présente trois régions principales du cerveau et leurs fonctions associées, ainsi que les conséquences de leur destruction. Régions corticales postérieures (lobes temporaux et pariétaux) : Ces régions sont responsables de l'intégration perceptive. La destruction de ces zones entraîne une atteinte des fonctions instrumentales, ce qui peut provoquer le syndrome aphaso-apraxo-agnosique. Ce syndrome se caractérise par des difficultés à parler (aphasie), à exécuter des mouvements coordonnés (apraxie) et à reconnaître des objets ou des visages (agnosie). Régions préfrontales : Ces régions sont impliquées dans les fonctions exécutives, qui incluent la planification, la prise de décision et le contrôle des comportements. La destruction de ces zones peut entraîner le syndrome dysexécutif, également connu sous le nom de syndrome frontal. Les personnes atteintes de ce syndrome peuvent avoir des difficultés à organiser leurs pensées et leurs actions, à prendre des décisions et à contrôler leurs impulsions. Régions temporales internes : Ces régions jouent un rôle crucial dans la consolidation de la mémoire épisodique, qui est la mémoire des événements personnels et des expériences vécues. La destruction de ces zones peut entraîner une amnésie, caractérisée par une perte de mémoire progressive, souvent décrite comme un "oubli à mesure". Ce schéma est intéressant car il met en évidence l'importance de différentes régions du cerveau dans les fonctions intellectuelles et les conséquences potentielles de leur dysfonctionnement.
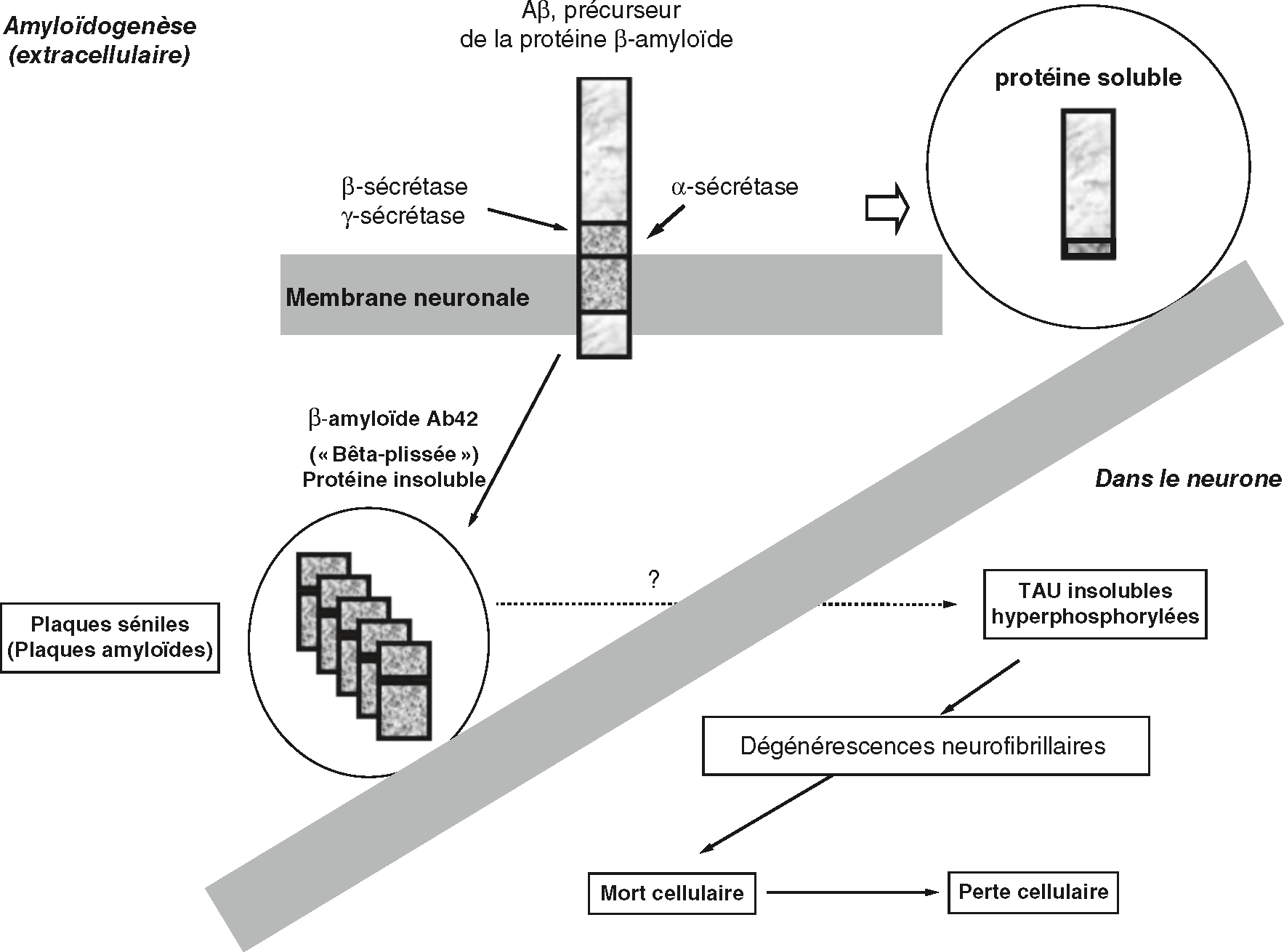
Fig. 22.2  Cascade biologique de la maladie d’Alzheimer.
Cascade biologique de la maladie d’Alzheimer.La cascade biologique de la maladie d'Alzheimer débute par l'amyloïdogénèse, un processus à l'extérieur des neurones. La protéine précurseur amyloïde (APP) est clivée par les enzymes β-sécrétase et γ-sécrétase, générant des peptides β-amyloïdes Aβ42, insolubles. Ces peptides s'agrègent pour former des plaques amyloïdes à l'extérieur des neurones. À l'intérieur des neurones, Aβ42 favorise la phosphorylation anormale de la protéine TAU, normalement associée aux microtubules. Cette hyperphosphorylation rend TAU insoluble, formant des dégénérescences neurofibrillaires, des enchevêtrements à l'intérieur des neurones. Ces plaques amyloïdes et enchevêtrements TAU perturbent la communication neuronale, conduisant à la mort neuronale. La perte progressive de neurones et de synapses entraîne une atrophie cérébrale, visible principalement dans le cortex cérébral et l'hippocampe, zones essentielles à la mémoire et aux fonctions cognitives. En résumé, la cascade biologique de la maladie d'Alzheimer implique la formation de plaques amyloïdes et de dégénérescences neurofibrillaires, menant à la mort neuronale et à une atrophie cérébrale progressive.
-
• Les facteurs de risque ne sont pas identifiés dans leur ensemble :
- – certains sont génétiques (par exemple, le portage de l’homozygotie pour l’allèle ε4 de l’apolipoprotéine E);
- – certains sont environnementaux ou liés au mode de vie (par exemple, les facteurs de risque cérébrovasculaire et le faible niveau d’éducation).
-
• 397Trois grandes anomalies biologiques2 caractérisent l’affection :
- – l’accumulation anormale de protéines β-amyloïdes (Aβ-42) en amas extracellulaires (« plaques amyloïdes » ou « plaques séniles »). Celles-ci sont surtout présentes dans les cortex cérébraux associatifs (cortex préfrontaux, pariétaux et temporaux) et épargnent relativement le cortex visuel primaire (lobes occipitaux) et le cortex moteur (frontale ascendante);
- – l’accumulation anormale dans les prolongements neuronaux de protéine TAU anormalement phosphorylée formant les dégénérescences neurofibrillaires (DNF); ces DNF sont trouvées en grande quantité dans les régions temporales internes (hippocampes en particulier);
- – la perte des neurones dont les prolongements ont préalablement été le siège des DNF. Cette perte cellulaire, lorsqu’elle est massive, conduit à l’atrophie des régions affectées.
B 398Comment faire le diagnostic de la maladie d’Alzheimer ?
- •
 Il s’agit d’une démarche diagnostique reposant certes sur la présence d’arguments négatifs, mais aussi et surtout sur le recueil d’arguments positifs.
Il s’agit d’une démarche diagnostique reposant certes sur la présence d’arguments négatifs, mais aussi et surtout sur le recueil d’arguments positifs. - • Le diagnostic du vivant du patient est un diagnostic de probabilité. Le diagnostic de certitude repose sur la neuropathologie (post mortem).
- • La probabilité de porter un bon diagnostic repose sur le faisceau d’arguments associant les signes positifs et les signes négatifs. Plus la concordance des arguments est importante, plus la probabilité du diagnostic est élevée.
-
• Le diagnostic repose sur cinq types d’arguments3 :
- – arguments positifs cliniques : le profil des troubles cognitifs;
- – arguments de neuro-imagerie négatifs (pas d’autres lésions) et positifs (atrophie hippocampique);
- – arguments négatifs par la pratique d’un bilan biologique plasmatique, servant à éliminer des diagnostics différentiels, en particulier de démences dites curables;
- – arguments positifs d’imagerie métabolique (hypométabolisme et/ou hypoperfusion des cortex associatifs);
- – 399arguments positifs par dosage des biomarqueurs de la pathologie Alzheimer dans le LCS (profil caractéristique des taux intrathécaux des protéines TAU phosphorylée et β-amyloïde 42 [AβM-42], voir plus loin).
-
• Dans l’immense majorité des cas, l’association examen clinique (incluant le bilan précis des fonctions cognitives) + imagerie cérébrale par IRM + bilan biologique suffit à obtenir un diagnostic de haute probabilité (voir plus loin fig. 22.5). Le recours à l’imagerie métabolique et au dosage des biomarqueurs du LCS n’est actuellement pas systématique.
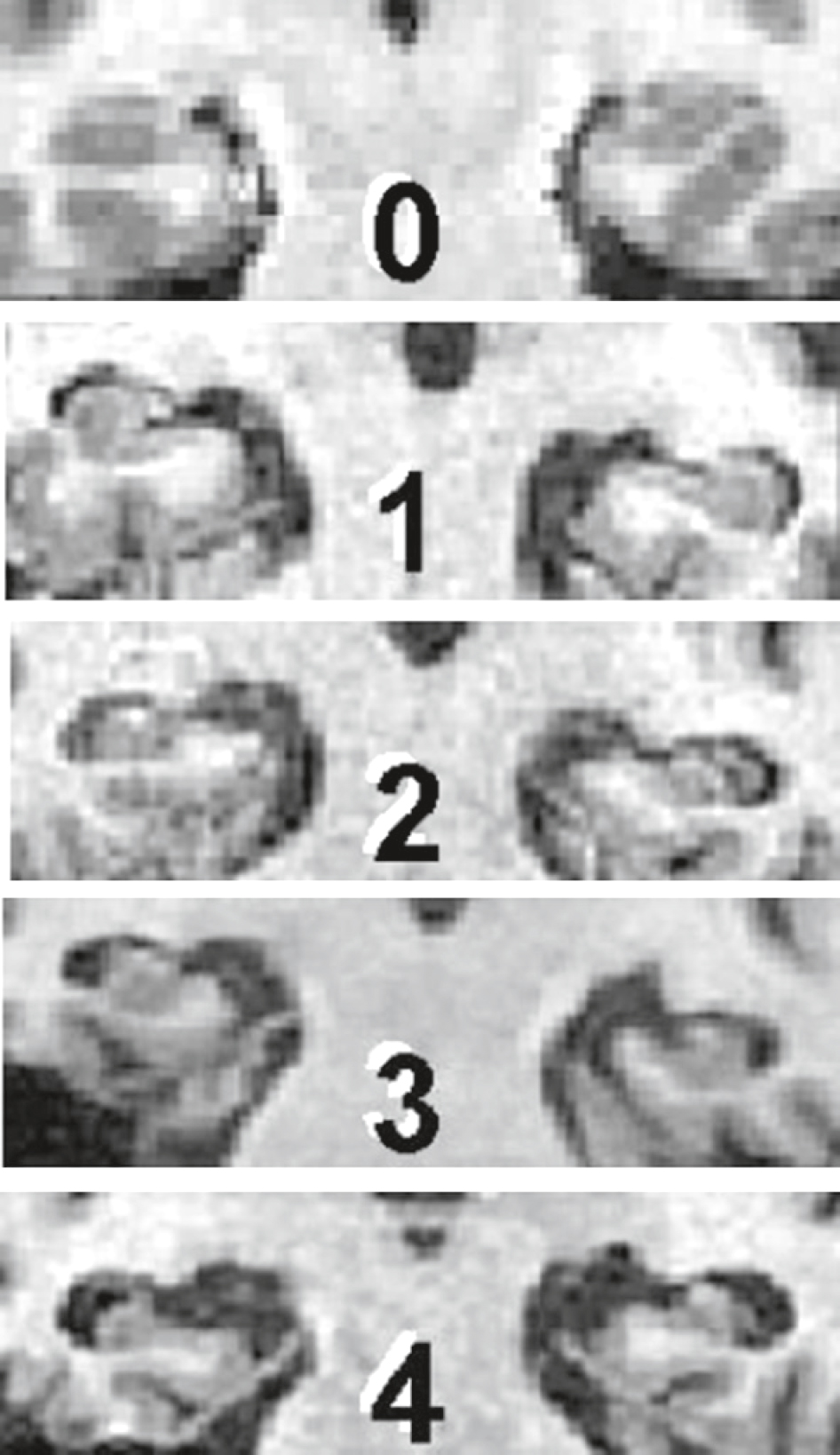
Fig. 22.5  Échelle de Scheltens.
Échelle de Scheltens.
Elle est graduée de 0 à 4. 0 : pas d’atrophie; 1 : atrophie possible; 2 : atrophie discrète; 3 : atrophie modérée; 4 : atrophie sévère.L'échelle de Scheltens est utilisée pour évaluer la sévérité de l'atrophie cérébrale, en particulier dans les maladies neurodégénératives comme la maladie d'Alzheimer. L'image montre des coupes transversales du cerveau, numérotées de 0 à 4, représentant différents stades d'atrophie. À l'étape 0, il n'y a pas d'atrophie visible, les structures cérébrales apparaissent normales et bien définies. À l'étape 1, une légère atrophie commence à être visible, avec un rétrécissement des structures cérébrales et une augmentation des espaces entre elles. À l'étape 2, l'atrophie est plus prononcée, avec des structures cérébrales rétrécies et des espaces interstitiels plus larges. À l'étape 3, l'atrophie est encore plus marquée, avec des structures cérébrales significativement rétrécies et des espaces encore plus larges. Enfin, à l'étape 4, l'atrophie est sévère, avec des structures très rétrécies et des espaces interstitiels très larges. Cette échelle permet de quantifier la progression de l'atrophie cérébrale et d'évaluer l'efficacité des traitements. Elle est utile pour le diagnostic et le suivi des patients atteints de maladies neurodégénératives. En comprenant les différents stades d'atrophie, les professionnels de la santé peuvent mieux adapter leurs approches thérapeutiques et offrir des soins plus personnalisés aux patients.
1 Histoire naturelle
Il faut distinguer trois phases évolutives (fig. 22.3) :
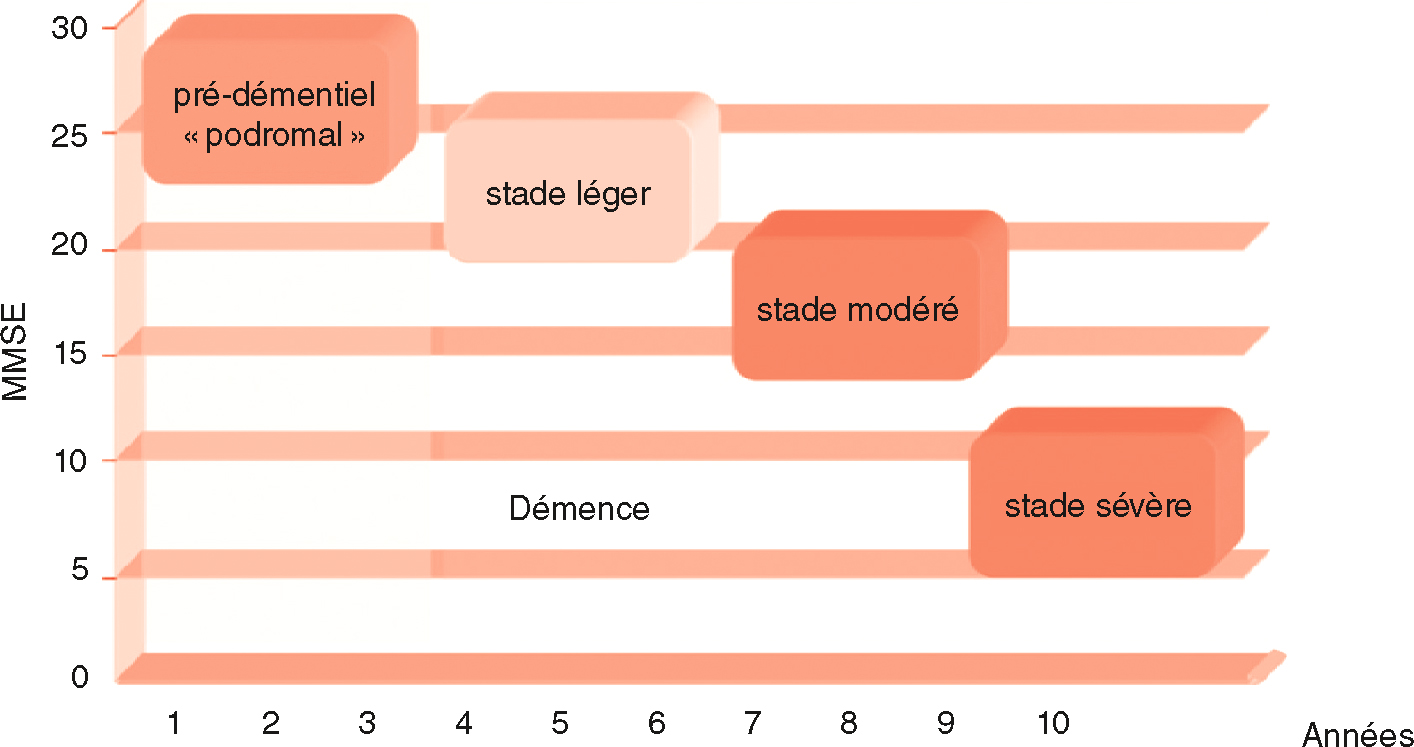
 Histoire naturelle de la maladie d’Alzheimer symptomatique.
Histoire naturelle de la maladie d’Alzheimer symptomatique. N.B. : le test MMSE (Mini Mental State Examination) permet d’effectuer un examen cognitif global et, en cas de démence, donne une indication sur sa sévérité; il ne permet pas de poser un diagnostic étiologique.
L'image montre l'évolution naturelle de la maladie d'Alzheimer symptomatique sur une période de 10 ans, mesurée par le score MMSE (Mini-Mental State Examination). L'axe vertical représente le score MMSE, allant de 0 à 30, tandis que l'axe horizontal représente les années, de 1 à 10. La progression de la maladie est divisée en plusieurs stades : Pré-démentiel « prodromal » : Ce stade se situe entre les scores MMSE de 25 à 30 et dure environ 3 ans. C'est la phase initiale où les symptômes commencent à apparaître mais ne sont pas encore suffisamment graves pour être diagnostiqués comme une démence. Stade léger : Ce stade se situe entre les scores MMSE de 20 à 25 et dure environ 4 ans. Les symptômes deviennent plus apparents et peuvent commencer à interférer avec les activités quotidiennes. Stade modéré : Ce stade se situe entre les scores MMSE de 15 à 20 et dure environ 3 ans. Les symptômes sont plus sévères et nécessitent souvent une aide pour les activités quotidiennes. Stade sévère : Ce stade se situe entre les scores MMSE de 10 à 15 et dure environ 2 ans. Les symptômes sont très graves et les patients nécessitent une assistance constante. Démence : Ce stade se situe en dessous des scores MMSE de 10. Les patients ont une perte sévère de la fonction cognitive et nécessitent des soins intensifs. Cette représentation visuelle montre clairement la progression de la maladie d'Alzheimer et la durée approximative de chaque stade, aidant à comprendre l'évolution de la maladie et à planifier les soins nécessaires.
- • la phase prédémentielle ou prodromale : c’est le début de la phase symptomatique;
- • la phase d’état ou de démence (légère à sévère);
- • la phase de démence très sévère.
a Phase « prédémentielle » ou « prodromale »
- • À cette phase de la maladie, les patients sont autonomes pour la plupart des gestes de la vie quotidienne.
-
• L’anomalie la plus fréquemment retrouvée est un trouble de la consolidation en mémoire épisodique :
- – il est le reflet clinique de l’atteinte sévère des régions temporales internes (hippocampes et cortex adjacents) (voir encadré 22.1);
- – la plainte mnésique est, de loin, le symptôme conduisant le plus fréquemment à évoquer le diagnostic. Il s’agit d’un oubli à mesure (par exemple, le patient fait répéter plusieurs fois la même chose) témoignant de l’incapacité à former un souvenir durable à partir d’un événement vécu. Il n’est pas rare que le patient minimise la plainte (anosognosie), alors que l’entourage s’en inquiète.
-
• À l’épreuve des cinq mots (voir encadré 22.2), les patients présentant un trouble de la consolidation en mémoire épisodique ne sont pas capables de donner les cinq mots après un délai de quelques minutes. Surtout, ils ne sont pas aidés par les indices de catégorie proposés par l’examinateur. Cela suggère qu’ils n’ont pas enregistré les mots.
- • 400L’évaluation de la mémoire par un neuropsychologue complète le bilan, en confirmant par un test de mémoire (le plus utilisé est le « Rappel libre/rappel indicé à 16 items ») l’effondrement des capacités à rappeler des informations (par exemple, des mots à mémoriser), et en confirmant le trouble de la consolidation (par exemple, pour les mots, par la faiblesse de l’aide normalement pourvue par les indices de catégorie). La répétition des phases de rappel n’améliore pas la restitution. Les patients introduisent dans la liste des mots à rappeler des mots ne faisant pas partie de la liste à mémoriser (« intrusions »).
- • Ce profil de troubles de la mémoire s’oppose à d’autres types de déficits de mémoire secondaires aux troubles de l’attention ou des fonctions exécutives, qui altèrent la qualité de l’enregistrement ou de la récupération des informations (mais pas directement la consolidation). Dans ce cas, les sujets ont des difficultés à restituer spontanément une liste de mots (par exemple, les cinq mots), mais ils sont significativement aidés par les indices. On observe notamment ce profil dans les situations fonctionnelles suivantes : dépression, troubles du sommeil, anxiété, prise excessive de psychotropes.
b Phase démentielle
- • L’autonomie est significativement altérée pour les activités dites instrumentales de la vie quotidienne (aptitudes à utiliser le téléphone, à utiliser les moyens de transport, à gérer la prise de médicaments, à manipuler l’argent).
- • Outre les troubles de la mémoire, il existe une atteinte plus ou moins sévère des autres fonctions cognitives : syndrome dit « aphaso-apraxo-agnosique » et atteinte des fonctions exécutives.
- • Ces nouvelles atteintes cognitives reflètent l’extension des lésions aux régions corticales associatives (cortex préfrontal, pariétal et temporal externe).
c Phase très avancée de la maladie (démence sévère)
- • La perte de l’autonomie est totale du fait d’une atteinte des activités de base de la vie quotidienne (toilette, habillage, locomotion, alimentation). Souvent, les patients sont en institution. Cette phase précède la fin de vie et survient en moyenne 7 à 8 ans après la détection des premiers symptômes de la maladie.
- • Outre les troubles touchant l’ensemble des fonctions cognitives (et pouvant aller jusqu’à la non-reconnaissance des proches), il peut exister des troubles psychologiques et des troubles du comportement (agitation ou apathie, hallucinations, troubles délirants, déambulation, troubles du sommeil et de l’appétit, troubles du contrôle des sphincters), des troubles du rythme veille–sommeil, des signes de dénutrition et d’autres troubles d’origine neurologique (troubles de la marche et de la posture avec chutes, épilepsie, myoclonies).
- • Le décès survient par une complication générale due à l’état grabataire (surinfection bronchique, suite d’une chute avec alitement prolongé…) ou par mort subite.
2 Arguments diagnostiques
a Arguments négatifs et positifs et de neuro-imagerie
Les objectifs sont d’éliminer une cause non dégénérative et de rechercher une atrophie cérébrale, en particulier des hippocampes.
401Il s’agit de :
- • éliminer un processus expansif intracrânien (tumeur intra- ou extracérébrale, hématome sous-dural…) ou une hydrocéphalie;
- • détecter des lésions vasculaires ischémiques et hémorragiques (séquences utiles : T2/FLAIR et T2 en écho de gradient, respectivement);
-
• évaluer visuellement l’atrophie des hippocampes (séquence utile : T1 coronal avec un plan de coupes perpendiculaire au grand axe de l’hippocampe) (fig. 22.4). Pour cela, il est possible de s’aider de l’échelle d’évaluation de l’atrophie des hippocampes de Scheltens (fig. 22.5). Toutefois, c’est une mesure subjective qui dépend de l’expérience du clinicien.
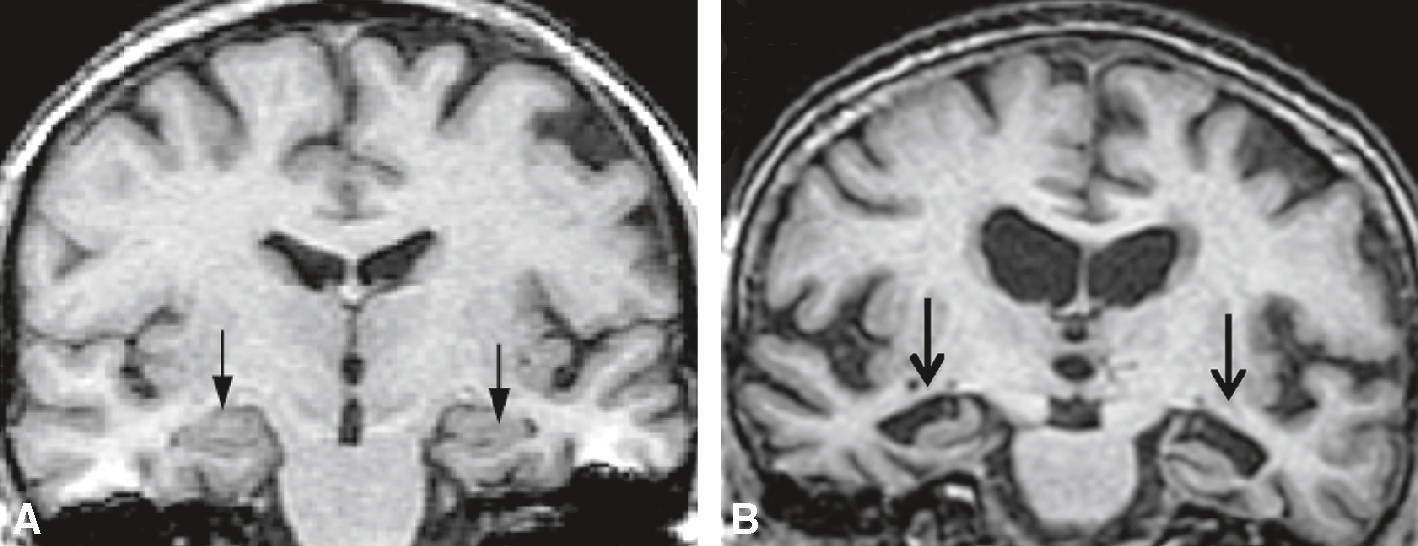
Fig. 22.4  IRM cérébrale pour le diagnostic positif de la maladie d’Alzheimer.
IRM cérébrale pour le diagnostic positif de la maladie d’Alzheimer.
IRM en séquence pondérée T1. Les flèches localisent les hippocampes. Coupes coronales passant par le grand axe de l’hippocampe. A. Cerveau sain, pas d’atrophie des hippocampes. B. Patient Alzheimer : atrophie hippocam-pique bilatérale.L'IRM cérébrale est une technique d'imagerie médicale utilisée pour diagnostiquer la maladie d'Alzheimer. Sur l'image, on peut voir deux coupes coronales du cerveau. L'image A montre une vue antérieure du cerveau, tandis que l'image B montre une vue légèrement plus postérieure. Les flèches noires indiquent des zones spécifiques du cerveau, probablement les hippocampes, qui sont souvent affectées par la maladie d'Alzheimer. Les hippocampes sont des structures cruciales pour la mémoire et l'orientation spatiale. Dans le contexte de la maladie d'Alzheimer, ces régions peuvent montrer des signes d'atrophie, c'est-à-dire une réduction de volume, ce qui est un indicateur clé de la maladie. L'IRM permet de visualiser ces changements structurels et d'aider au diagnostic en fournissant des images détaillées des tissus cérébraux. Cette technique est non invasive et utilise des champs magnétiques et des ondes radio pour produire des images précises du cerveau. Les images obtenues peuvent révéler des anomalies qui ne seraient pas visibles avec d'autres méthodes d'imagerie, ce qui en fait un outil précieux pour les neurologues dans le diagnostic et le suivi de la maladie d'Alzheimer. En résumé, les images montrent des signes d'atrophie hippocampique, un élément diagnostique clé pour la maladie d'Alzheimer, et l'IRM est un outil essentiel pour visualiser ces changements et confirmer le diagnostic.
b 402Arguments négatifs par la pratique d’un bilan biologique plasmatique4
- • Le bilan minimal comprend : NFS-plaquettes, VS, ionogramme plasmatique, calcémie, albu-minémie, fonction rénale (créatinine et sa clairance), CRP, thyroid stimulating hormone ultrasensible (TSHus) et glycémie à jeun.
- • La Haute Autorité de santé (HAS) recommande d’ajouter selon le contexte : fonction hépatique (transaminases, gamma GT) et vitamine B12-folates (ces deux examens seront en pratique assez systématiques), les sérologies syphilitique, Lyme et VIH étant réservées à des cas particuliers.
c 403Arguments positifs d’imagerie métabolique
![]() La scintigraphie de perfusion peut mettre en évidence une hypoperfusion des régions corticales associatives et temporales internes. La tomographie par émission de positons (TEP) détermine le métabolisme cérébral par un radiomarquage fluoré du déoxyglucose (TEP-FDG), qui peut mettre en évidence un hypométabolisme de ces mêmes régions.
La scintigraphie de perfusion peut mettre en évidence une hypoperfusion des régions corticales associatives et temporales internes. La tomographie par émission de positons (TEP) détermine le métabolisme cérébral par un radiomarquage fluoré du déoxyglucose (TEP-FDG), qui peut mettre en évidence un hypométabolisme de ces mêmes régions.
d Arguments positifs par dosage des biomarqueurs dans le LCS de la pathologie Alzheimer
- •
 Dosage dans le LCS des taux de la protéine β-amyloïde (Aβ-42) et de la protéine TAU hyperphosphorylée (TAU-p).
Dosage dans le LCS des taux de la protéine β-amyloïde (Aβ-42) et de la protéine TAU hyperphosphorylée (TAU-p). -
• Le profil typique est :
- – une baisse d’Aβ1-42 absolue ou relative (évaluée par le ratio d’Aβ1-42/Aβ1-40), témoignant probablement de la séquestration de cette protéine dans le cerveau au sein des plaques séniles;
- – et une augmentation de TAU-p, témoignant du largage vers le compartiment extracellulaire de cette protéine lors de la mort neuronale.
![]() En pratique clinique, devant une plainte mnésique, le diagnostic se fait par l’évaluation neuropsychologique, une IRM cérébrale et le bilan biologique plasmatique. L’examen du LCS et la scintigraphie de perfusion/TEP-FDG sont proposés dans les formes de diagnostic difficile (patients vus au stade débutant de TNC mineur, profil clinique atypique et/ou démence à début précoce) (fig. 22.6).
En pratique clinique, devant une plainte mnésique, le diagnostic se fait par l’évaluation neuropsychologique, une IRM cérébrale et le bilan biologique plasmatique. L’examen du LCS et la scintigraphie de perfusion/TEP-FDG sont proposés dans les formes de diagnostic difficile (patients vus au stade débutant de TNC mineur, profil clinique atypique et/ou démence à début précoce) (fig. 22.6).
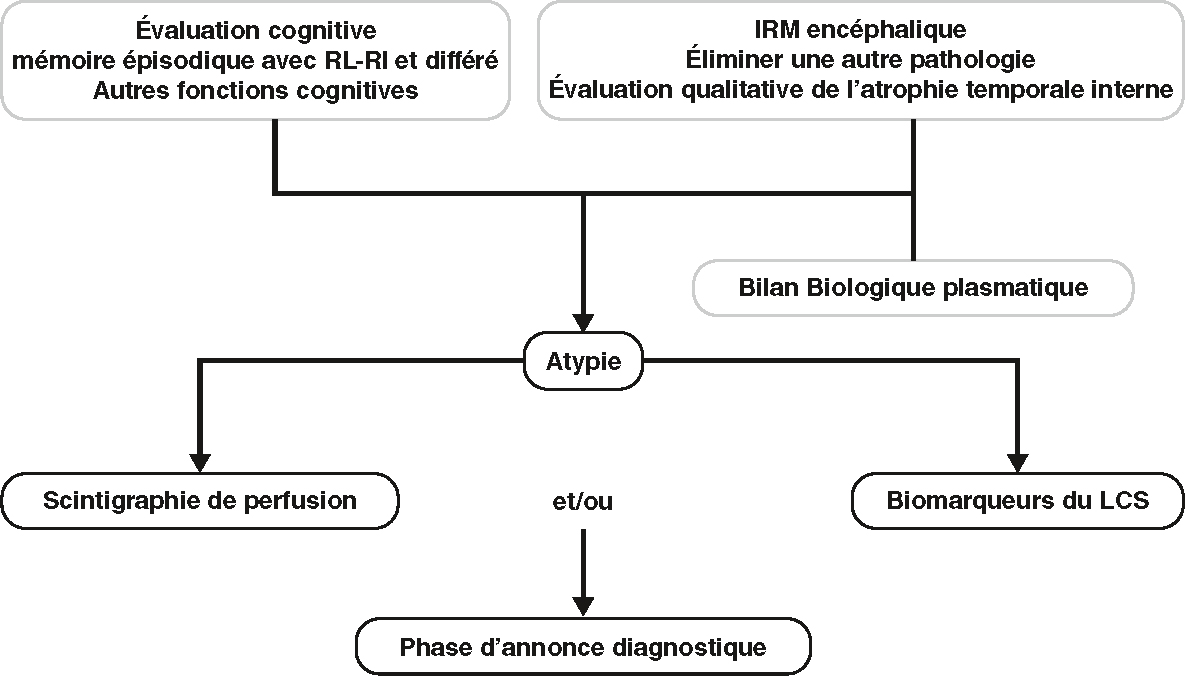
 Algorithme décisionnel devant un trouble progressif et isolé de la mémoire (ou des autres fonctions intellectuelles).
Algorithme décisionnel devant un trouble progressif et isolé de la mémoire (ou des autres fonctions intellectuelles). LCS : liquide cérébrospinal; RL-RI : rappel libre-rappel indicé.
L'image montre un algorithme décisionnel pour évaluer un trouble progressif et isolé de la mémoire ou des autres fonctions intellectuelles. Cet algorithme commence par deux évaluations principales : une évaluation cognitive et une IRM encéphalique. L'évaluation cognitive inclut la mémoire épisodique avec RL-RI et différé, ainsi que d'autres fonctions cognitives. L'IRM encéphalique vise à éliminer d'autres pathologies et à évaluer qualitativement l'atrophie temporale interne. Les résultats de ces évaluations mènent à un bilan biologique plasmatique pour détecter des signes d'atypie. Si une atypie est détectée, deux options sont envisagées : une scintigraphie de perfusion ou l'analyse des biomarqueurs du liquide céphalo-rachidien (LCS). Ces étapes permettent de progresser vers la phase d'annonce diagnostique. Cet algorithme est pertinent car il offre une approche structurée pour diagnostiquer les troubles cognitifs progressifs, en utilisant des méthodes d'évaluation et des tests biologiques pour identifier les anomalies et orienter le diagnostic.
C 404Diagnostic différentiel
1 Confusion mentale
2 Causes fonctionnelles de TNC
- • La dépression, les troubles du sommeil (insomnie et apnées du sommeil), l’anxiété chronique, la prise de psychotropes (benzodiazépines, antidépresseurs, hypnotiques, etc.) peuvent donner des troubles de l’attention et des fonctions exécutives retentissant sur le fonctionnement de la mémoire (« pseudo-amnésie »).
- • Si les troubles cognitifs apparaissent dans un contexte de dépression, proposer un traitement d’épreuve par antidépresseurs, à dose pleine, pendant une période minimale de 3 mois.
3 Causes organiques
a « Démences » secondaires et éventuellement curables
- • L’hypothyroïdie, la carence en vitamine B12 et/ou en folates, la syphilis, l’évolution d’une infection par le VIH, certaines tumeurs cérébrales (méningiomes frontaux).
- • L’hydrocéphalie à pression « normale » :
-
- –
 elle se manifeste par des troubles de la marche (à petits pas), des troubles cognitifs, surtout de type frontal avec apathie, et des troubles du contrôle urinaire;
elle se manifeste par des troubles de la marche (à petits pas), des troubles cognitifs, surtout de type frontal avec apathie, et des troubles du contrôle urinaire; - – 405les troubles cognitifs sont quelquefois suffisamment sévères pour entraîner une démence et/ou des épisodes de confusion;
- – le scanner cérébral et l’IRM du cerveau montrent une dilatation tétraventriculaire sans effet de masse et avec une suffusion de liquide dans le parenchyme périventriculaire (résorption transépendymaire) entraînant des anomalies radiologiques (hypodensité au scanner X et en IRM, hypersignal en pondération T2 de la substance blanche périventriculaire);
- – un test diagnostique et thérapeutique consiste à effectuer des ponctions lombaires évacuatrices;
- – le traitement chirurgical par dérivation ventriculo-péritonéale est proposé quand la probabilité diagnostique est forte.
- –
-
•
 L’hématome sous-dural chronique : il s’agit d’une collection extraparenchymateuse à contenu liquidien, parfois associée à un saignement récent. Il est une cause fréquente de troubles cognitifs (ralentissement psychomoteur, apathie, syndrome frontal, confusion mentale…) chez la personne âgée. Il est souvent détecté à distance d’un traumatisme crânien même léger (et passant quelquefois inaperçu). Il est aussi favorisé par la déshydratation, l’éthylisme chronique et les traitements affectant la coagulation. Le scanner X ou l’IRM du cerveau mettent en évidence une collection liquidienne dans les espaces méningés (entre la dure-mère et l’arachnoïde). Lorsqu’il est chronique, l’hématome sous-dural apparaît le plus souvent hypodense au scanner X cérébral ou associant des zones d’épanchement de sang frais (hyperdenses) et des zones hypodenses. Il est en forme de « croissant » et souvent bilatéral. L’évacuation chirurgicale ou la surveillance simple se discutent au cas par cas (fig. 22.7).
L’hématome sous-dural chronique : il s’agit d’une collection extraparenchymateuse à contenu liquidien, parfois associée à un saignement récent. Il est une cause fréquente de troubles cognitifs (ralentissement psychomoteur, apathie, syndrome frontal, confusion mentale…) chez la personne âgée. Il est souvent détecté à distance d’un traumatisme crânien même léger (et passant quelquefois inaperçu). Il est aussi favorisé par la déshydratation, l’éthylisme chronique et les traitements affectant la coagulation. Le scanner X ou l’IRM du cerveau mettent en évidence une collection liquidienne dans les espaces méningés (entre la dure-mère et l’arachnoïde). Lorsqu’il est chronique, l’hématome sous-dural apparaît le plus souvent hypodense au scanner X cérébral ou associant des zones d’épanchement de sang frais (hyperdenses) et des zones hypodenses. Il est en forme de « croissant » et souvent bilatéral. L’évacuation chirurgicale ou la surveillance simple se discutent au cas par cas (fig. 22.7).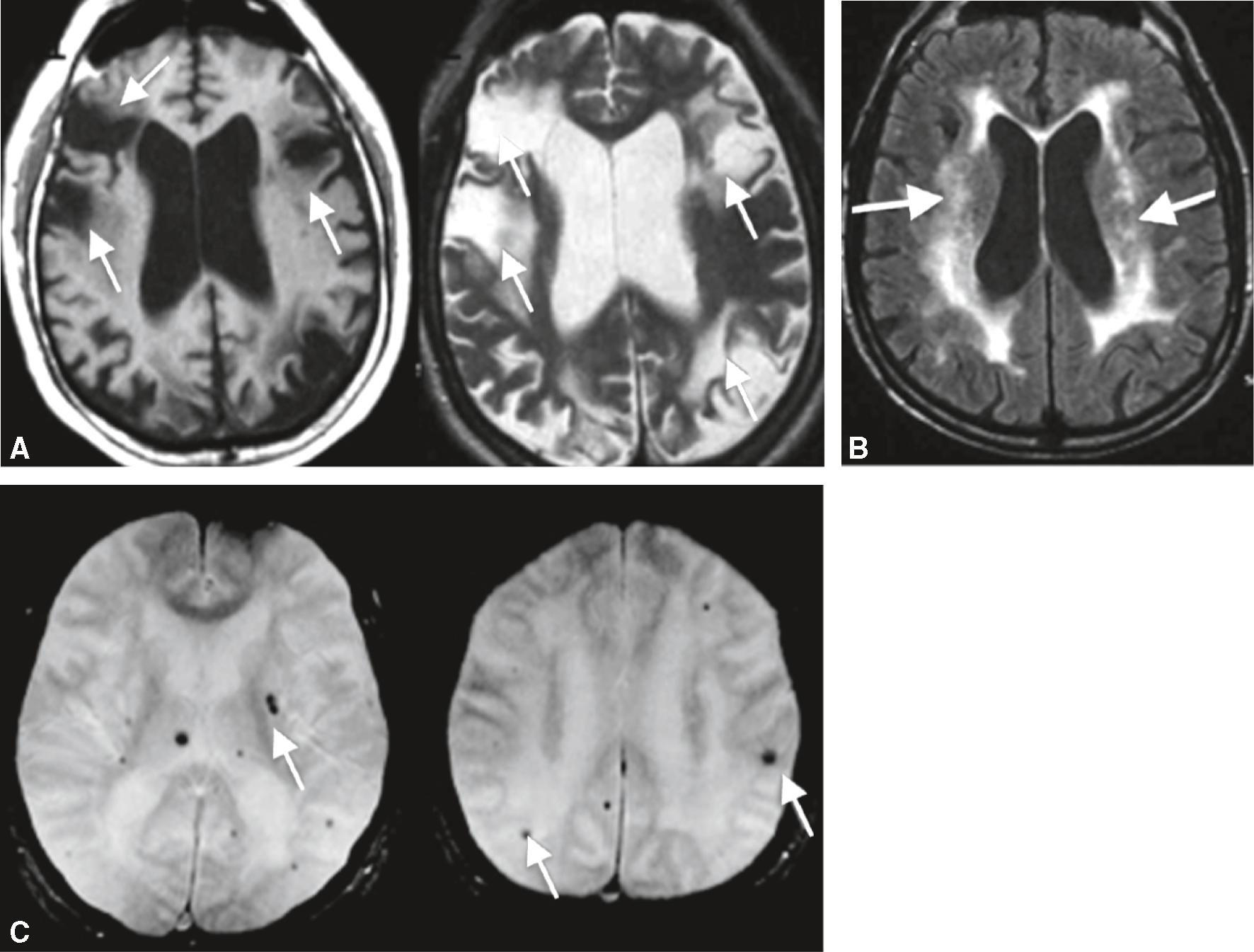
Fig. 22.7  Exemples en IRM de lésions vasculaires responsables de troubles cognitifs et de démences.
Exemples en IRM de lésions vasculaires responsables de troubles cognitifs et de démences.
A. Infarctus corticaux et sous-corticaux multiples (séquences T1 et T2). B. Hypersignaux de la substance blanche sus-tentorielle (séquence T2/FLAIR). C. Microsaignements (séquence T2, écho de gradient).L'image présente des exemples de lésions vasculaires cérébrales observées par IRM, responsables de troubles cognitifs et de démences. L'image A montre des coupes axiales du cerveau avec des flèches indiquant des zones de lésions vasculaires. Ces lésions apparaissent sous forme de zones hyperintenses, plus brillantes que le tissu cérébral environnant, souvent associées à des dommages aux petits vaisseaux sanguins, entraînant des troubles cognitifs. L'image B montre aussi une coupe axiale du cerveau avec des flèches pointant vers des lésions hyperintenses autour des ventricules cérébraux, les cavités remplies de liquide céphalorachidien. Ces lésions périventriculaires, courantes chez les personnes âgées, peuvent indiquer une leucoaraïose, liée à des troubles cognitifs et à la démence. L'image C présente deux coupes axiales du cerveau avec des flèches indiquant des microhémorragies cérébrales, des taches sombres représentant des saignements microscopiques, souvent causés par une hypertension chronique ou d'autres maladies vasculaires. Les microhémorragies peuvent contribuer aux troubles cognitifs et à la démence en endommageant le tissu cérébral. Ces images sont importantes car elles illustrent les différents types de lésions vasculaires pouvant affecter le cerveau et entraîner des troubles cognitifs et des démences. Elles montrent comment l'IRM peut être utilisée pour détecter et évaluer ces lésions, fournissant des informations cruciales pour le diagnostic et la gestion des troubles cognitifs.
- • 406Les lésions vasculaires par atteintes des petites artères (HTA, diabète) comprennent les lacunes, les hypersignaux de la substance blanche, les microsaignements et les petits infarctus sous-corticaux. Leur sommation peut aboutir à un TNC ou à une démence dite « vas-culaire » d’apparition insidieuse. La maladie des petites artères est souvent associée à une atteinte neurodégénérative de type Alzheimer, une situation appelée TNC ou démence mixte.
- • Si le syndrome démentiel évolue rapidement dans un délai inférieur à 1 an, envisager les encéphalopathies subaiguës : maladie de Creutzfeldt-Jakob, encéphalite inflammatoire ou auto-immune (incluant les syndromes paranéoplasiques).
b Autres démences dégénératives
Démence frontale (dégénérescence lobaire frontotemporale ou DLFT)
- •
 À la différence de la maladie d’Alzheimer, qui est une démence par troubles cognitifs, la DLFT est, le plus souvent, une démence par troubles comportementaux.
À la différence de la maladie d’Alzheimer, qui est une démence par troubles cognitifs, la DLFT est, le plus souvent, une démence par troubles comportementaux. - • Elle est le prototype clinique du syndrome frontal.
- • Les symptômes et signes cliniques de la DLFT sont expliqués par le dysfonctionnement du lobe frontal qui a pour principales fonctions de générer des comportements volontaires et adaptés aux besoins de l’individu ou en rapport avec les interactions sociales et de bloquer (ou réguler) les comportements automatiques, pulsionnels ou archaïques.
- • Les signes cliniques apparaissent insidieusement, le plus fréquemment entre 50 et 60 ans (en moyenne 10 ans avant ceux de la maladie d’Alzheimer).
-
• Il s’agit :
- – d’une perte des convenances sociales (familiarité excessive, impudeur, comportements en société non adaptés compte tenu de ce que l’on connaît de la personne et de son milieu social);
- – d’un trouble du contrôle des conduites personnelles (gloutonnerie, diminution de l’hygiène corporelle, baisse du contrôle urinaire, etc.);
- – d’une perte de l’intérêt pour les autres (baisse de l’empathie, indifférence affective);
- – d’une difficulté par le patient à percevoir et analyser ses symptômes (anosognosie);
- – d’une apathie (diminution spontanée de l’initiative et des comportements volontaires).
- • À l’examen : signes de désinhibition du comportement, troubles des fonctions exécutives.
- • Dans environ 25 à 30 % des cas, il s’agit d’une maladie héréditaire, transmise sur un mode autosomique dominant.
- •
 Il existe plusieurs formes cliniques. La forme la plus fréquente est la forme comportementale (due principalement à une dégénérescence des zones ventrales des lobes frontaux), mais il existe aussi des formes plus rares débutant par des troubles du langage constituant une aphasie primaire progressive.
Il existe plusieurs formes cliniques. La forme la plus fréquente est la forme comportementale (due principalement à une dégénérescence des zones ventrales des lobes frontaux), mais il existe aussi des formes plus rares débutant par des troubles du langage constituant une aphasie primaire progressive. -
• L’IRM cérébrale peut montrer une atrophie du cortex frontal et du tissu sous-cortical (entraînant un aspect « ballonisé » des cornes ventriculaires frontales), tandis que la scintigraphie de perfusion et le TEP-scan métabolique montrent une hypoperfusion ou un hypométabo-lisme des régions frontales et temporales (fig. 22.8).
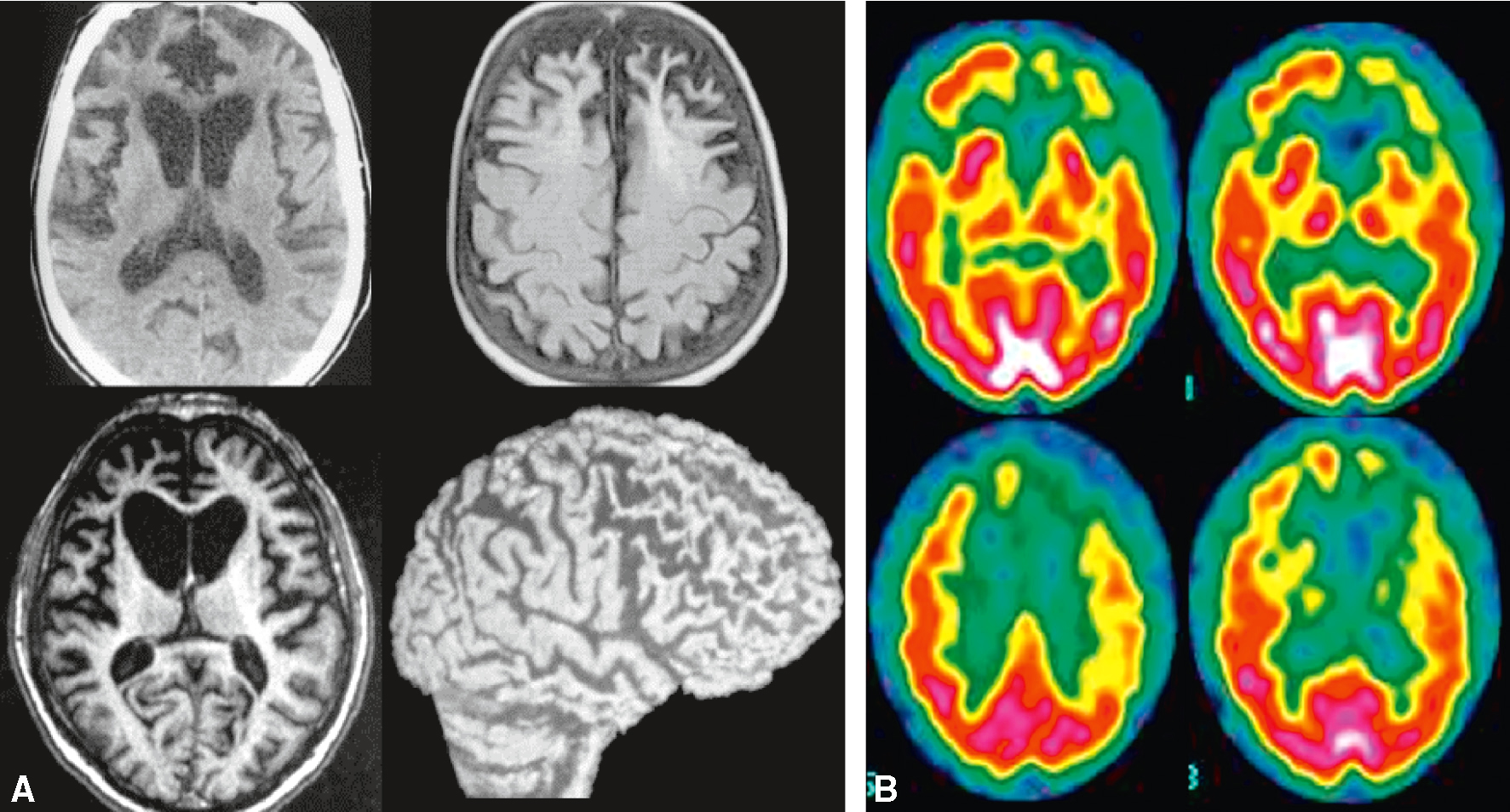
Fig. 22.8  Démence frontotemporale.
Démence frontotemporale.
A. IRM. B. Scintigraphie de perfusion. L’IRM et la scintigraphie de perfusion montrent une atrophie/hypoperfu-sion dans les régions frontales, temporales antérieures et cingulaires. Noter, en IRM, l’aspect ballonisé des cornes frontales des ventricules latéraux.La démence frontotemporale (DFT) est une forme de démence qui affecte principalement les lobes frontaux et temporaux du cerveau. L'image montre des scans cérébraux qui illustrent les changements structurels et fonctionnels associés à cette maladie. Sur la partie gauche de l'image (A), on voit des images de résonance magnétique (IRM) du cerveau. Les deux premières images en haut montrent des coupes transversales du cerveau, tandis que les deux images en bas montrent une coupe transversale et une vue latérale du cerveau. Ces images révèlent une atrophie significative des lobes frontaux et temporaux, caractéristique de la DFT. L'atrophie se manifeste par une réduction du volume cérébral et un élargissement des ventricules cérébraux. Sur la partie droite de l'image (B), on voit des images de tomographie par émission de positons (TEP) qui montrent l'activité métabolique du cerveau. Les zones colorées en rouge et jaune indiquent une activité métabolique normale, tandis que les zones en vert et bleu montrent une activité réduite. Les images montrent une diminution de l'activité métabolique dans les lobes frontaux et temporaux, ce qui est typique de la DFT. Ces images sont importantes car elles permettent de visualiser les changements cérébraux associés à la démence frontotemporale, aidant ainsi à diagnostiquer et à comprendre cette maladie.
- • Les autres examens complémentaires (ponction lombaire, bilan biologique) n’apportent pas ou peu de contributions positives, mais permettent d’éliminer une autre cause.
- • Il n’y a pas de traitement spécifique à ce jour.
407Au total, la DLFT est à évoquer devant des troubles du comportement suggérant un syndrome frontal, évoluant progressivement et isolément, après qu’une cause non dégénérative (tumeur, lésion post-traumatique…) a été écartée avec l’aide de l’imagerie cérébrale.
Maladie à corps de Lewy diffus
- • À la différence de la maladie d’Alzheimer, la maladie à corps de Lewy se manifeste le plus souvent par un syndrome parkinsonien et des hallucinations de survenue précoce.
- • Les anomalies pathologiques sont celles de la maladie de Parkinson (corps de Lewy et synucléinopathie), à la différence qu’elles siègent de façon plus importante dans les régions associatives du cortex cérébral, alors que dans la maladie de Parkinson ces lésions touchent surtout la profondeur du cerveau. Cette différence de topographie lésionnelle et l’association fréquente à des lésions de maladie d’Alzheimer expliquent la démence.
-
• L’affection peut se présenter initialement comme une maladie d’Alzheimer ou comme une maladie de Parkinson avec les différences essentielles suivantes :
- – l’existence d’hallucinations visuelles ou auditives et de troubles psychiatriques (dépression sévère, troubles psychotiques), souvent inauguraux ou précoces dans l’évolution de la maladie;
- – des fluctuations majeures des performances cognitives évoquant une confusion mentale chronique a minima ;
- – quand le mode d’entrée est celui d’une démence, il faut rechercher un syndrome parkinsonien;
- – quand le mode d’entrée est un syndrome parkinsonien, il faut rechercher un syndrome démentiel.
- • La prise en charge thérapeutique est souvent un mélange de celles des deux maladies (Alzheimer et Parkinson), en tenant compte de la très mauvaise tolérance des neuroleptiques au cours de la maladie à corps de Lewy diffus.
D 408Traitement de la maladie d’Alzheimer
![]() Le traitement de la maladie d’Alzheimer est actuellement purement symptomatique, mais les perspectives futures (essais cliniques) vont dans le sens d’un blocage le plus précoce possible de la cascade biologique conduisant à la mort cellulaire (approche de neuroprotection).
Le traitement de la maladie d’Alzheimer est actuellement purement symptomatique, mais les perspectives futures (essais cliniques) vont dans le sens d’un blocage le plus précoce possible de la cascade biologique conduisant à la mort cellulaire (approche de neuroprotection).
1 Traitement médicamenteux
-
• Quatre molécules ont reçu l’AMM en France :
- – trois d’entre elles sont des anticholinestérasiques centraux (ils augmentent la biodisponibilité de l’acétylcholine dans le cerveau) : le donépézil, la rivastigmine et la galantamine;
- – la mémantine, est un antagoniste des récepteurs NMDA du glutamate;
- – elles existent tous sous une forme générique. Ces traitements sont prescrits par voie orale. La rivastigmine existe aussi sous forme de timbres à diffusion transdermique (patch).
- • L’indication actuelle se limite aux phases démentielles de la maladie (légère à modérément sévère).
- • Les essais thérapeutiques montrent que le déclin cognitif est légèrement moins marqué chez les patients traités. Le traitement améliorerait aussi certains troubles comportementaux (apathie, agitation, hallucinations.).
- • Les effets secondaires principaux (anticholinestérasiques) sont des troubles digestifs (nausées, vomissements, diarrhées et perte de poids) et des crampes musculaires.
- • En raison de leur activité pharmacologique, les inhibiteurs de la cholinestérase peuvent avoir des effets vagotoniques sur le rythme cardiaque (par exemple, bradycardie), en particulier en cas d’anomalie supraventriculaire (maladie du sinus, bloc sino-auriculaire ou auriculoventriculaire), pouvant favoriser la survenue de syncopes et de chutes. Il est impératif de respecter les contre-indications et les précautions d’emploi. Un ECG systématique, voire, en cas de doute, un avis cardiologique, est nécessaire en cas de prescription. Un suivi attentif, notamment de la fréquence cardiaque, est à effectuer.
- • Leur initiation est faite obligatoirement par un neurologue, un psychiatre ou un gériatre.
- • Leur efficacité symptomatique, modeste, a été considérée comme insuffisante pour bénéficier de la solidarité nationale par la HAS qui, après une évaluation récente et défavorable de leur rapport efficacité/risque, a recommandé un déremboursement total pour l’ensemble de ces molécules et qui est appliqué depuis le 1er août 2018. Le traitement peut néanmoins être prescrit dans les conditions rappelées ci-dessus et sera donc à la charge du patient.
- • Les autres traitements médicamenteux ont pour but de limiter les troubles comportementaux. Il s’agit de psychotropes (à utiliser avec grande prudence +++).
- • Il faut penser à limiter (ou arrêter) les médicaments aggravant potentiellement les troubles cognitifs (psychotropes et en particulier les anticholinergiques).
2 Traitement non médicamenteux
-
•
 À visée de stabilisation ou de compensation du TNC :
À visée de stabilisation ou de compensation du TNC :- – séances de rééducation (ou remédiation) cognitive avec un orthophoniste (sur prescription);
- – 409séances de réhabilitation cognitive (visant à maintenir ou à restaurer l’autonomie pour certaines tâches) par une équipe spécialisée Alzheimer (ESA) composée de psychomo-triciens, ergothérapeutes et assistants de soins en gérontologie (sur prescription), pour le patient au stade léger à modéré;
- – stimulation cognitive en centre d’accueil de jour (médicalisé), sur inscription.
-
• Aides humaines, intervention de tiers :
- – soutien logistique des aidants : aide à domicile (auxiliaire de vie, aide-soignant);
- – en cas de perte d’autonomie, dans les cas complexes (sujet seul en refus de soins), recours possible à des dispositifs appelés maison pour l’autonomie et l’intégration des maladies d’Alzheimer (MAIA) pour l’intégration des services d’aide et de soins dans le champ de l’autonomie;
- – institutionnalisation quand le maintien au domicile est impossible : maison de retraite médicalisée (maison de retraite adaptée dite EHPAD) ou service de long séjour.
-
• Aides financières et médico-légales :
- – affection de longue durée (ALD-15) et prise en charge à 100 % (stade démentiel);
- – soutien financier : allocation personnalisée d’autonomie (APA) sous conditions de revenu et de degré de perte d’autonomie si ≥ 60 ans; prestation de compensation du handicap (PCH) si < 60 ans;
- – mesures de protection médico-légale de type sauvegarde de justice, tutelle ou habilitation familiale si nécessaire (pas systématique).
-
• Hygiène de vie et autres traitements :
- – activités physiques quotidiennes (marche à pied, par exemple);
- – sorties quotidiennes;
- – traitement des déficiences sensorielles (surdité, troubles visuels), aggravant les difficultés cognitives et d’interactions sociales;
- – traitement des facteurs aggravants curables (anémie, insuffisance cardiaque, insuffisance antéhypophysaire, déficits sensoriels, hématome sous-dural, etc.);
- – prévention de la iatrogénie (arrêt des psychotropes non indispensables);
- – dans les phases de démences sévères, une surveillance accrue de l’état nutritionnel est nécessaire (oubli fréquent des repas).
-
• Aide aux aidants :
- – plateformes d’accompagnement et de répit (soutien psychologique, formation des aidants);
- – associations de familles.
-
• La plupart de ces mesures ont pour but de :
- – éviter le retrait social et l’absence de stimulation physique et cognitive;
- – soutenir les familles, souvent épuisées par la prise en charge chronique.
III État confusionnel
A Pour comprendre
- • L’état confusionnel (ou confusion mentale) est dû à une altération modérée de la vigilance entraînant une désorganisation globale de la pensée et des fonctions cognitives.
- • Les principaux symptômes et signes cliniques de la confusion mentale résultent des troubles attentionnels, eux-mêmes secondaires à l’altération de la vigilance.
- •
 L’attention peut être considérée comme la « porte d’entrée » ouvrant vers le fonctionnement de l’ensemble des fonctions cognitives. Si la porte est « entrebâillée » ou « fermée », 410les fonctions intellectuelles qui en dépendent sont perturbées, entraînant une désorganisation majeure et globale de la pensée cohérente.
L’attention peut être considérée comme la « porte d’entrée » ouvrant vers le fonctionnement de l’ensemble des fonctions cognitives. Si la porte est « entrebâillée » ou « fermée », 410les fonctions intellectuelles qui en dépendent sont perturbées, entraînant une désorganisation majeure et globale de la pensée cohérente. - • L’état confusionnel est très fréquent, notamment chez la personne âgée de plus de 70 ans (dans cette population, sa prévalence est comprise entre 30 et 40 % chez les personnes hospitalisées, de 50 % en postopératoire et 70 % en réanimation).
B Diagnostic
-
•
 La confusion se manifeste par l’apparition brusque ou rapidement progressive (en quelques minutes, heures ou jours) de troubles neuropsychiques :
La confusion se manifeste par l’apparition brusque ou rapidement progressive (en quelques minutes, heures ou jours) de troubles neuropsychiques :-
– difficultés attentionnelles :
- – difficulté pour maintenir l’attention sur les questions de l’examinateur,
- – troubles de la mémoire à court terme : répéter une phrase longue, une suite de chiffres dans l’ordre direct ou inversé (« empan chiffré »), les mois de l’année dans l’ordre inverse, faire une opération de calcul mental, etc.,
- – caractère décousu et incohérent du langage spontané;
- – troubles de l’étape attentionnelle de l’enregistrement en mémoire à long terme (« encodage »), entraînant des difficultés à retenir une liste de mots et surtout une désorientation temporospatiale constante avec souvent un télescopage d’événements anciens avec le présent : globalement, les troubles attentionnels induisent une désorganisation de la pensée avec altération du raisonnement et du jugement;
- – troubles du comportement : perplexité anxieuse, agitation, agressivité, délire onirique (plus rarement structuré), hallucinations le plus souvent visuelles; labilité de l’humeur et de l’affect, allant de l’euphorie à la tristesse.
-
- • L’argument clinique majeur est la fluctuation des troubles cliniques ; elle est le reflet de la fluctuation de la vigilance. Les troubles décrits ci-dessus peuvent être absents ou présents (de modérément à intensément) selon le moment de la journée. Au maximum, il peut exister une inversion du cycle veille–sommeil (cycle nycthéméral), la confusion et l’agitation s’aggravant significativement en période vespérale et dans l’obscurité, tandis qu’une grande partie de la journée est occupée par la somnolence.
- • Il peut exister des signes somatiques non spécifiques d’une étiologie : un tremblement myoclonique (secousses irrégulières) des extrémités, d’attitude et d’action, un asté-rixis (ou flapping tremor : myoclonies négatives par chutes intermittentes et répétées du tonus musculaire).
- • L’EEG met en évidence un ralentissement global de l’activité électrique (non spécifique d’une étiologie).
- • Il y a une amnésie lacunaire pour toute la durée de l’épisode confusionnel.
- • Schématiquement, on peut distinguer trois formes cliniques : la forme confuso-onirique, dans laquelle le patient est agité, en proie à un délire onirique et des troubles végétatifs (hypersudation, tachycardie); la forme stuporeuse, dans laquelle la somnolence et le ralentissement psychomoteur sont au premier plan; et la forme mixte, alternant de façon irrégulière et imprévisible les états des deux premières formes.
-
•
 La Confusion Assessment Method (CAM) est un outil d’aide au diagnostic, rapide (5 à 10 minutes) et reproductible (encadré 22.4).
La Confusion Assessment Method (CAM) est un outil d’aide au diagnostic, rapide (5 à 10 minutes) et reproductible (encadré 22.4).
C 411Diagnostic différentiel
1 Aphasie de Wernicke
- •
 Elle peut mimer une confusion car les propos sont incohérents, le patient ne comprend pas son interlocuteur et il peut être agité du fait des troubles du langage.
Elle peut mimer une confusion car les propos sont incohérents, le patient ne comprend pas son interlocuteur et il peut être agité du fait des troubles du langage. - • Le patient aphasique de Wernicke ne comprend pas le sens des mots alors que le patient confus ne comprend pas le sens des phrases car il perd le fil de l’attention (ainsi, plus la consigne est longue, plus le patient confus est perdu).
- • Dans l’aphasie de Wernicke, il existe des paraphasies sémantiques (un mot dit pour un autre) et surtout des néologismes (non-mots).
- • Dans l’aphasie de Wernicke, il existe le plus souvent une amputation du champ visuel (hémi- ou quadranopsie latérale homonyme) liée à la proximité entre aire de Wernicke et radiations optiques.
- • Il n’y a ni troubles de la vigilance ni fluctuations nycthémérales de l’état neurologique, et les autres champs de la cognition sont respectés.
2 Trouble psychotique aigu
- • Si les propos sont diffluents comme au cours d’une confusion, en revanche, les éléments psychiatriques sont au premier plan.
- • Son apparition ne paraît pas liée à une atteinte somatique ou neurologique.
- • Il n’y a pas de trouble de vigilance.
- • Il faudra néanmoins se méfier d’une prise de toxiques ou de médicaments.
3 Ictus amnésique
- • Trouble aigu de l’enregistrement en mémoire épisodique.
- • Installation brusque.
- • Dure environ 6 à 8 heures.
- • Cet état est spontanément réversible.
- • Il laisse une lacune amnésique définitive.
- • 412Pendant l’épisode, le patient ne peut pas enregistrer volontairement de nouvelles informations. Le patient est perplexe sur son état et, symptôme très caractéristique, pose répétiti-vement les mêmes questions.
- • Il n’est pas, à la différence de la confusion, désorienté dans l’espace et la vigilance est conservée.
- • L’ictus amnésique peut être spontané ou post-traumatique (traumatisme crânien ou stress aigu). Sa physiopathologie n’est pas précisément connue.
- • Il peut récidiver, mais rarement (20 % des cas).
4 Syndrome démentiel
- • D’un point de vue physiopathologique, la démence (quelle que soit l’étiologie) est due aux lésions structurelles (réversibles ou non) de circuits cérébraux essentiels pour l’élaboration cognitive, tandis que la confusion mentale est liée à un trouble de la vigilance altérant de façon non spécifique les fonctions cognitives.
- • D’un point de vue clinique, le syndrome démentiel correspond à un trouble chronique (de plus de 6 mois), sans grande variation nycthémérale et constitué de troubles cognitifs spécifiques. Toutefois, une confusion mentale peut révéler ou émailler l’évolution d’un syndrome démentiel.
D Recherche étiologique
-
•
 Un très grand nombre de situations peuvent produire un état confusionnel (encadré 22.5).
Un très grand nombre de situations peuvent produire un état confusionnel (encadré 22.5). -
• L’examen clinique et le contexte orientent le diagnostic étiologique vers :
- – les causes neurologiques (principalement : traumatismes crâniens, hémorragie méningée, méningite et méningo-encéphalite, processus expansifs);
- – les causes non neurologiques (principalement : affections endocriniennes, métaboliques et insuffisances d’organe aiguës ou chroniques décompensées, intoxications volontaires ou involontaires).
- • 413Chez les patients âgés, les causes non neurologiques sont bien plus fréquentes que les causes neurologiques.
-
• Il faut insister sur l’existence de facteurs de risque de la confusion mentale :
- – chez une personne âgée, elle peut être produite par des causes générales inattendues chez les sujets jeunes (fécalome, globe vésical, troubles neurosensoriels, etc.);
- – les pathologies psychiatriques chroniques, la consommation d’alcool et de psychotropes;
- – l’immobilisation (hospitalisation, réanimation, phase de réveil postopératoire);
- – une pathologie chronique préexistante (insuffisance rénale ou hépatique, etc.);
- – elle peut être révélatrice d’un syndrome démentiel débutant. Il est justifié de réévaluer l’état cognitif des patients à distance (à 6 mois) de l’épisode confusionnel.
- • La stratégie du bilan étiologique (interrogatoire des proches, examen clinique et bilan complémentaire) rejoint celle du coma (voir chapitre 27 – item 336).
E Prise en charge d’un patient confus
La confusion mentale est une urgence médicale, diagnostique et thérapeutique, nécessitant presque toujours une hospitalisation immédiate car :
- • la cause de la confusion est souvent une pathologie grave, voire létale, rapidement (diabète décompensé, insuffisance surrénale aiguë, hémorragie méningée, etc.);
- • la confusion elle-même est potentiellement dangereuse (troubles majeurs du comportement et signes somatiques tels que la déshydratation).
La première étape de la prise en charge est d’évaluer le retentissement à court terme de l’état clinique (constantes vitales) et de traiter immédiatement les troubles vitaux (état de choc, hypothermie, etc.).
La seconde étape est de déterminer l’étiologie et de la lever.
La recherche de la cause de l’état confusionnel ne doit pas être différée même si les fonctions vitales sont assurées car seul le traitement de la cause permet la guérison.
L’étape du diagnostic étiologique et de son traitement rejoint la prise en charge d’un coma (voir chapitre 27 – item 336). Cette étape repose sur :
- • l’interrogatoire des proches ou des secouristes ayant transporté le patient aux urgences (antécédents médicaux, prise de médicaments ou de toxiques);
- • 414l’examen des documents médicaux disponibles;
- • un examen clinique approfondi général et neurologique (ne pas oublier la prise de la température, la recherche d’une morsure latérale de langue, l’examen des pupilles, la recherche de plaies, les traces d’injections, la recherche d’un globe urinaire ou d’un fécalome par toucher rectal);
- • le bilan paraclinique effectué en urgence dépendra des hypothèses formulées au décours de la phase clinique. Le bilan paraclinique minimum est :
-
- – ionogramme sanguin, calcémie, CRP, fonctions rénale (y compris calcul de la clairance de la créatinine) et hépatique, protides totaux, numération sanguine, TP-TCA, glycémie au doigt et plasmatique, bandelette urinaire, SaO2,
- – ECG,
- – radiographie thoracique,
- – si le scanner cérébral sans injection (pour éliminer l’hématome sous-dural) n’est pas recommandé de façon systématique par la HAS5, il ne faut pas hésiter à le demander en urgence devant le moindre doute de pathologie neurologique.
Le traitement de l’épisode confusionnel ne peut être envisagé indépendamment de la cause. Dans tous les cas :
- • veiller au maintien de la nutrition et réhydratation, si besoin par voie parentérale;
- • le patient est au calme, en chambre individuelle (avec lumière tamisée et porte ouverte pour la surveillance);
- • surveillance des constantes vitales et de la conscience fréquente et régulière;
- • retirer tous les médicaments non indispensables ou utiliser les plus petites doses possible. Cette démarche s’impose d’autant plus que l’ordonnance contient des psychotropes (se méfier en particulier des anticholinergiques +++) et qu’il existe un trouble de l’élimination (insuffisance rénale ou hépatique). Attention aussi à ne pas arrêter brusquement un traitement psychotrope ancien, car le sevrage brutal (par exemple aux benzodiazépines) peut être lui-même source de confusion mentale;
- • il faut éviter, dans la mesure du possible, la contention physique, qui aggrave l’agitation et l’angoisse.
Il faudra rester prudent quant à l’administration de psychotropes sédatifs car ils peuvent aggraver les troubles psychiques (troubles de la vigilance) et l’état somatique (syndrome akinéto-rigide des neuroleptiques). S’ils sont indispensables, préférer les benzodiazépines anxiolytiques à demi-vie courte aux neuroleptiques; ces derniers ne doivent être administrés qu’en cas d’agitation majeure faisant courir un risque au patient ou à l’entourage.
La confusion apparaît rapidement mais disparaît quelquefois très lentement, même quand la cause est levée (cela d’autant plus que le patient est âgé ou altéré sur le plan cognitif). Il faut donc être patient et ne pas conclure trop rapidement à l’absence d’efficacité de la prise en charge.
415
1La mise en place de trois plans nationaux « Alzheimer » (2001–2012) par le gouvernement francais, pour developper la recherche et mieux prendre en charge les patients, temoigne de l’importance societale de ce probleme.
2Les protéines β-amyloïdes et TAU hyperphosphorylées sont des protéines anormales, résultant de dysfonc-tions de voies de régulation de protéines constituantes des neurones. Par exemple, la protéine TAU (normalement phosphorylée) est une protéine nécessaire à la charpente microtubulaire des prolongements neuronaux. Elle participe aux transferts moléculaires du corps du neurone vers la synapse.
3Le diagnostic génétique moléculaire est un sixième argument. Il permet de faire un diagnostic de certitude de maladie d’Alzheimer dans les très rares formes génétiques de la maladie (moins de 1 % des patients). En effet, dans ces cas, la maladie d’Alzheimer est due à une mutation monogénique, de transmission autosomique dominante. Toutefois, ces formes génétiques se distinguent des autres par le début jeune (avant 60 ans, voire bien plus tôt) et par l’existence d’autres signes neurologiques. Elles ne doivent être évoquées que lorsqu’il existe des antécédents de démence du sujet jeune dans au moins deux générations successives.
4Dans le but de rechercher une comorbidité associée, la HAS recommande de pratiquer aussi une albuminémie et une créatininémie avec calcul de la clairance selon la formule de Cockroft et Gault (HAS, Maladie d’Alzheimer et maladies apparentées : diagnostic et prise en charge, décembre 2011).
5HAS. Recommandations de bonne pratique. Confusion aiguë chez la personne âgée : prise en charge initiale de l’agitation. Mai 2009.
