Situations de départ
 28 Coma et troubles de la conscience.
28 Coma et troubles de la conscience.
 29 Contracture musculaire localisée ou généralisée.
29 Contracture musculaire localisée ou généralisée.
 31 Perte d’autonomie progressive.
31 Perte d’autonomie progressive.
 49 Ivresse aiguë.
49 Ivresse aiguë.
 50 Malaise, perte de connaissance.
50 Malaise, perte de connaissance.
 64 Vertige et sensation vertigineuse.
64 Vertige et sensation vertigineuse.
 66 Apparition d’une difficulté à la marche.
66 Apparition d’une difficulté à la marche.
 114 Agitation.
114 Agitation.
 117 Apathie.
117 Apathie.
 119 Confusion mentale/désorientation.
119 Confusion mentale/désorientation.
 120 Convulsions.
120 Convulsions.
 122 Hallucinations.
122 Hallucinations.
 126 Mouvements anormaux.
126 Mouvements anormaux.
 128 Tremblements.
128 Tremblements.
 129 Troubles de l’attention.
129 Troubles de l’attention.
 130 Troubles de l’équilibre.
130 Troubles de l’équilibre.
 131 Troubles de la mémoire/déclin cognitif.
131 Troubles de la mémoire/déclin cognitif.
 172 Traumatisme crânien.
172 Traumatisme crânien.
 226 Découverte d’une anomalie du cerveau à l’examen d’imagerie médicale.
226 Découverte d’une anomalie du cerveau à l’examen d’imagerie médicale.
 279 Consultation de suivi d’une pathologie chronique.
279 Consultation de suivi d’une pathologie chronique.
 289 Consultation et suivi d’un patient épileptique.
289 Consultation et suivi d’un patient épileptique.
 298 Consultation et suivi d’un patient ayant des troubles cognitifs.
298 Consultation et suivi d’un patient ayant des troubles cognitifs.
 313 Prévention des risques liés à l’alcool.
313 Prévention des risques liés à l’alcool.
 327 Annonce d’un diagnostic de maladie grave au patient et/ou sa famille.
327 Annonce d’un diagnostic de maladie grave au patient et/ou sa famille.
Objectifs pédagogiques
 Repérer, diagnostiquer, évaluer le retentissement d’une addiction à l’alcool.
Repérer, diagnostiquer, évaluer le retentissement d’une addiction à l’alcool.
 Expliquer les indications et principes du sevrage thérapeutique.
Expliquer les indications et principes du sevrage thérapeutique.
 13Savoir rechercher et reconnaître les signes d’un syndrome de sevrage à l’alcool et les accidents de sevrage (convulsion et delirium tremens).
13Savoir rechercher et reconnaître les signes d’un syndrome de sevrage à l’alcool et les accidents de sevrage (convulsion et delirium tremens).
 Savoir diagnostiquer une intoxication alcoolique aiguë avec ou sans coma éthylique.
Savoir diagnostiquer une intoxication alcoolique aiguë avec ou sans coma éthylique.
 Connaître les signes de l’encéphalopathie de Gayet-Wernicke, ses mécanismes et complications.
Connaître les signes de l’encéphalopathie de Gayet-Wernicke, ses mécanismes et complications.
 Connaître les complications médicales générales principales de la consommation d’alcool.
Connaître les complications médicales générales principales de la consommation d’alcool.
 Savoir prendre en charge un accident de sevrage (crise convulsive ou delirium tremens).
Savoir prendre en charge un accident de sevrage (crise convulsive ou delirium tremens).
Hiérarchisation des connaissances
| Rang | Rubrique | Intitulé | Descriptif |
|---|---|---|---|
| Prévalence, épidémiologie | Connaître les principaux chiffres liés à la consommation d’alcool en France (source : BEH 2023) | ||
| Définition | Connaître les définitions des termes suivants : addictologie, non-usage, usage à faible risque, mésusage, usage à risque, usage nocif (CIM 11), dépendance (CIM 11)* | ||
| Définition | Comparaison dépendance (CIM 11) et trouble de l’usage de l’alcool (DSM-5)* | La dépendance (CIM 11) correspond aux troubles de l’usage d’alcool modéré à sévère (DSM-5)* | |
| Diagnostic positif | Connaître les repères de consommation d’alcool définissant l’usage à faible risque* | Repères de Santé publique France définis en 2017 et communiqués en 2019* | |
| Diagnostic positif | Savoir diagnostiquer usage nocif et dépendance selon les critères de la CIM 11* | Le diagnostic de dépendance repose sur l’association de trois critères au moins dans l’année qui précède et le diagnostic d’usage nocif requiert l’élimination du diagnostic de dépendance (ils s’excluent mutuellement) | |
| Diagnostic positif | Savoir dépister un mésusage d’alcool : verres standard, consommation déclarée, AUDIT-C* | Le dépistage du mésusage d’alcool est systématique pour tout nouveau patient, en particulier aux urgences, et repose sur l’interrogatoire, au mieux avec l’aide du questionnaire AUDIT-C* | |
| Diagnostic positif | Savoir rechercher et reconnaître les signes d’un syndrome de sevrage à l’alcool et les accidents de sevrage (convulsion et delirium tremens) | Faire le diagnostic clinique, éliminer les diagnostics différentiels | |
| Identifier une urgence | Savoir diagnostiquer une intoxication alcoolique aiguë avec ou sans coma éthylique (diagnostic différentiel) et rechercher les troubles métaboliques associés | Faire le diagnostic clinique, éliminer les diagnostics différentiels, rechercher hypoglycémie, aciodocétose, hyponatrémie | |
| Diagnostic positif | Connaître l’association fréquente du mésusage d’alcool avec d’autres pathologies addictives et psychiatriques, qu’elles soient primaires ou secondaires* | Les troubles psychiatriques associés au mésusage d’alcool peuvent être primaires (existant avant l’installation du mésusage, qui peut avoir une fonction autothérapeutique) ou secondaires (la consommation d’alcool entraîne des symptômes voire des troubles psychiatriques, anxieux ou dépressifs en particulier)* | |
| Diagnostic positif | Connaître les principales complications sociales du mésusage d’alcool et le lien avec la précarité* | ||
| Examens complémentaires | Connaître les marqueurs biologiques usuels de consommation d’alcool : alcoolémie, gamma-glutamyltransférase, volume globulaire moyen, transferrine désialysée* | Les marqueurs usuels de consommation d’alcool sont l’alcoolémie, la gamma-glutamyltransférase, le volume globulaire moyen et la transferrine désialylée* | |
| Diagnostic positif | Connaître les complications médicales générales principales de la consommation d’alcool* | ||
| Définition | Connaître les principes de base de la prévention primaire du mésusage d’alcool* | ||
| Prise en charge | Connaître le RPIB (repérage précoce et intervention brève) et son contenu* | Le RPIB comprend le dépistage systématique d’un mésusage d’alcool et une intervention brève en cas de mésusage sans dépendance* | |
| Prise en charge | Connaître les principes de la prise en charge | La prise en charge doit être globale, bio-psychosociale et pluridisciplinaire, et les objectifs généraux peuvent être : un arrêt complet des consommations ou abstinence, le retour à un usage à faible risque, voire une réduction des consommations dans un objectif de réduction des risques | |
| Prise en charge | Connaître les principes de l’entretien motivationnel* | ||
| Prise en charge | Savoir prendre en charge un sevrage encadré d’alcool* | Le sevrage de l’alcool peut être réalisé en ambulatoire, par tout médecin, ou lors d’une hospitalisation, et nécessite la prévention des signes et accidents de sevrage* | |
| Prise en charge | Savoir prendre en charge un accident de sevrage (crise convulsive ou delirium tremens) | Un accident de sevrage nécessite une hospitalisation et doit être traité par benzodiazépines demi-vie longue à forte dose, dégressive sur une à deux semaines, vitamine B1 parentérale et hydratation adaptée | |
| Prise en charge | Connaître l’existente des groupes d’entraide et des structures de soins en addictologie* | ||
| Prise en charge | Connaître l’existence de médicaments spécifiques dans la dépendance à l’alcool* | Médicaments d’aide à la diminution de la consommation (nalméfène, baclofène) et au maintien de l’abstinence après un sevrage (acamprosate, naltrexone, disulfiram, baclofène)* |
14![]() L’alcoolisme est la cause directe ou indirecte de 15 à 25 % des hospitalisations et d’environ 41 000 décès par an en France1.
L’alcoolisme est la cause directe ou indirecte de 15 à 25 % des hospitalisations et d’environ 41 000 décès par an en France1.
L’identification d’un alcoolisme chronique est le plus souvent aisée : consommation excessive reconnue, présence de plusieurs signes cliniques (faciès vultueux, couperose du visage, parfois rhinophima) et de signes biologiques (macrocytose, augmentation des gamma-glutamyltransférases [γ-GT]).
15Plusieurs mécanismes peuvent expliquer les effets de l’alcool sur le système nerveux :
- • toxicité directe : l’alcool se fixe sur les phospholipides membranaires, notamment sur les récepteurs des systèmes gabaergique et glutamatergique, entraînant une dysfonction des canaux ioniques :
- • toxicité indirecte : carences vitaminiques (dues à une mauvaise nutrition et à une gastrite chronique), conséquences de l’atteinte d’organes retentissant sur le cerveau (insuffisance hépatique, cardiomyopathie alcoolique, dépression immunitaire) ou de troubles induits (traumatismes crâniens, accidents).
Quand la symptomatologie n’est pas typique, il faut penser à une autre cause que l’alcool et ne pas facilement attribuer une symptomatologie neurologique au seul alcoolisme connu d’un patient.
L’alcoolisme chronique est habituellement associé à un tabagisme chronique et aux complications neurologiques de celui-ci (métastase cérébrale d’un cancer bronchique, encéphalopathie respiratoire due à une bronchopneumopathie chronique obstructive, etc.).
Plusieurs de ces complications doivent être prévenues en prescrivant chez tout patient alcoolique hospitalisé, quelle qu’en soit la raison, un supplément vitaminique B1, B6, B12, folates et PP.
Les complications neurologiques de l’alcoolisme chronique sont souvent associées chez un même patient.
I Complications neurologiques de l’intoxication alcoolique aiguë
A Ivresse simple
Conséquence de l’action de l’alcool notamment sur la substance réticulée du tronc cérébral, les noyaux vestibulaires, le cervelet et le cortex. L’ivresse banale associe jovialité, hypomanie (parfois tristesse), propos incohérents et dysarthrie, troubles cérébelleux et vertiges.
Le diagnostic repose sur la mesure de l’alcoolémie.
B Ivresse pathologique
L’ivresse pathologique associe des troubles du comportement (agressivité, violences, dange-rosité, actes clastiques délictueux), parfois des hallucinations et un délire. Elle est suivie d’un sommeil profond et d’une amnésie lacunaire.
C Ivresse convulsivante
Par abaissement du seuil épileptogène, il s’agit le plus souvent d’une crise généralisée unique au cours d’une intoxication aiguë chez un buveur occasionnel, ne nécessitant pas de traitement antiépileptique.
D Coma éthylique
En cas d’absorption massive d’alcool, une encéphalopathie peut s’installer sous la forme d’une phase d’obnubilation puis de stupeur, enfin de coma éthylique qui peut comporter des signes de gravité (aréactivité, mydriase, hypotonie, dépression respiratoire, hypothermie, hypotension) engageant le pronostic vital et nécessitant alors le transfert en réanimation où seront prévenues les complications.
16
Des séquelles (compressions nerveuses périphériques tronculaires et/ou plexuelles, troubles mnésiques post-anoxiques) sont possibles.
II Complications neurologiques aiguës du sevrage alcoolique
L’alcool agit comme agoniste des récepteurs GABA (fonction inhibitrice). Le sevrage entraîne une diminution de la transmission gabaergique, avec pour conséquence une hyperexcitabilité. Le sevrage correspond à un arrêt complet ou à une diminution de la consommation. Il est souvent contemporain d’une affection intercurrente (pathologie infectieuse, traumatisme) qu’il importe d’identifier et de traiter.
A Crise d’épilepsie
Elle survient surtout chez un patient encore jeune, stade où les autres complications neurologiques sont encore rares.
Il s’agit le plus souvent d’une crise généralisée tonicoclonique, unique – mais des états de mal peuvent survenir dans 5 % des cas – dans les 12 à 24 heures du sevrage.
L’EEG est le plus souvent normal, des anomalies paroxystiques à la stimulation lumineuse intermittente sont possibles. Une première crise nécessite une imagerie cérébrale, car elle peut révéler une pathologie associée.
![]() Il n’y a pas d’indication à un traitement antiépileptique, mais on peut utiliser ponctuellement des benzodiazépines, afin de diminuer les autres symptômes de sevrage.
Il n’y a pas d’indication à un traitement antiépileptique, mais on peut utiliser ponctuellement des benzodiazépines, afin de diminuer les autres symptômes de sevrage.
B Delirium tremens
![]() Les signes de début (« pré-delirium tremens ») doivent être dépistés : inversion du rythme nycthéméral, cauchemars, irritabilité, anxiété, sueurs, tremblement postural des mains. Ces signes de début nécessitent d’urgence :
Les signes de début (« pré-delirium tremens ») doivent être dépistés : inversion du rythme nycthéméral, cauchemars, irritabilité, anxiété, sueurs, tremblement postural des mains. Ces signes de début nécessitent d’urgence :
- •
 une hydratation per os avec vitaminothérapie (B1, B6 et PP);
une hydratation per os avec vitaminothérapie (B1, B6 et PP); - • les benzodiazépines per os (diazépam, clonazépam) ou par voie parentérale (diazépam) en cas d’agitation plus importante, imposant une surveillance cardiorespiratoire. Ce traitement a un double intérêt : prise en charge symptomatique de l’agitation et prévention de l’évolution vers un delirium tremens avéré.
![]() En l’absence de traitement, l’évolution se fait vers un delirium tremens : syndrome confuso-onirique avec propos incohérents, agitation, hallucinations multiples surtout visuelles avec zoopsie et scènes d’agression, causes d’agressivité et de réactions de frayeur. Le syndrome 17physique associe fièvre, sueurs, trémulations, parfois signes de déshydratation, modification de la pression artérielle, tachycardie, troubles du rythme. Des crises d’épilepsie, voire un état de mal, peuvent survenir.
En l’absence de traitement, l’évolution se fait vers un delirium tremens : syndrome confuso-onirique avec propos incohérents, agitation, hallucinations multiples surtout visuelles avec zoopsie et scènes d’agression, causes d’agressivité et de réactions de frayeur. Le syndrome 17physique associe fièvre, sueurs, trémulations, parfois signes de déshydratation, modification de la pression artérielle, tachycardie, troubles du rythme. Des crises d’épilepsie, voire un état de mal, peuvent survenir.
Le delirium tremens est une urgence médicale dont le traitement associe :
- •
 hydratation adaptée au bilan électrolytique qui doit être répété, avec surveillance de la diurèse, apport vitaminique (B1, B6, PP), correction de l’hypokaliémie;
hydratation adaptée au bilan électrolytique qui doit être répété, avec surveillance de la diurèse, apport vitaminique (B1, B6, PP), correction de l’hypokaliémie; - • benzodiazépines IV (dose de charge par diazépam 10 mg par heure). Il est souhaitable de disposer de moyens de réanimation et d’un antidote des benzodiazépines (flumazénil) : en cas d’insuffisance hépatocellulaire, on privilégiera des benzodiazépines métabolisées par conjugaison (plutôt que par oxydation), telles que le lorazépam;
- • correction de l’hyperthermie (antipyrétiques);
- • recours prudent aux neuroleptiques (surveillance, diminution rapide de la posologie, uniquement si les hallucinations persistent malgré les benzodiazépines);
- • sans oublier le traitement des facteurs favorisants ou aggravants (infection pulmonaire, traumatisme, par exemple).
C Prévention des manifestations neurologiques du sevrage alcoolique
![]() Le sevrage thérapeutique à but de prévention des complications de l’alcoolisme se réalise en ambulatoire ou en milieu institutionnel. Il associe hydratation, prescriptions vitaminiques et traitement par benzodiazépines pendant une semaine à dose dégressive.
Le sevrage thérapeutique à but de prévention des complications de l’alcoolisme se réalise en ambulatoire ou en milieu institutionnel. Il associe hydratation, prescriptions vitaminiques et traitement par benzodiazépines pendant une semaine à dose dégressive.
III Complications neurologiques de l’intoxication alcoolique chronique
A Encéphalopathies
1 Encéphalopathie de Gayet-Wernicke (ou de Wernicke-Korsakoff)
Due à une carence en vitamine B1, parfois induite par un apport glucidique, son diagnostic doit être posé au début devant un seul des signes suivants ou en présence de leur association :
- • syndrome confusionnel;
- • signes oculomoteurs : paralysie oculomotrice, paralysie de fonction, nystagmus;
- • syndrome cérébelleux statique;
- • hypertonie oppositionnelle.
![]() En dehors du dosage de la vitamine B1 (effondré), le diagnostic est fait par l’IRM cérébrale (hypersignaux FLAIR des corps mamillaires).
En dehors du dosage de la vitamine B1 (effondré), le diagnostic est fait par l’IRM cérébrale (hypersignaux FLAIR des corps mamillaires).
![]() Le traitement, urgent, repose sur la vitamine B1 IV sans attendre les résultats des dosages. Il est surtout préventif : supplémentation systématique en vitamine B1 de tout patient alcoolique chronique dénutri, prescription systématique de vitamine B1 lors d’un apport glucosé chez un patient dénutri ou éthylique.
Le traitement, urgent, repose sur la vitamine B1 IV sans attendre les résultats des dosages. Il est surtout préventif : supplémentation systématique en vitamine B1 de tout patient alcoolique chronique dénutri, prescription systématique de vitamine B1 lors d’un apport glucosé chez un patient dénutri ou éthylique.
2 Encéphalopathie pellagreuse
![]() Due à une carence en vitamine PP, elle associe confusion mentale et hypertonie extrapyramidale : troubles digestifs et signes cutanéomuqueux (glossite, desquamation) sont très 18inconstants. Le traitement repose sur la vitamine PP parentérale (500 mg par jour). Il est surtout préventif : prescription systématique de vitamine PP à tout patient alcoolique dénutri.
Due à une carence en vitamine PP, elle associe confusion mentale et hypertonie extrapyramidale : troubles digestifs et signes cutanéomuqueux (glossite, desquamation) sont très 18inconstants. Le traitement repose sur la vitamine PP parentérale (500 mg par jour). Il est surtout préventif : prescription systématique de vitamine PP à tout patient alcoolique dénutri.
3 Encéphalopathie hépatique
![]() Secondaire à l’insuffisance hépatique (cirrhose), elle comporte une confusion mentale associée à un astérixis (flapping tremor), fait de myoclonies dites négatives (correspondant à une chute transitoire du tonus responsable de mouvements de flexion brusque puis extension des poignets lors de la manœuvre de Barré) avec, parfois, des signes extrapyramidaux (par dépôts de manganèse dans les ganglions de la base : intérêt de l’IRM encéphalique) et des crises d’épilepsie.
Secondaire à l’insuffisance hépatique (cirrhose), elle comporte une confusion mentale associée à un astérixis (flapping tremor), fait de myoclonies dites négatives (correspondant à une chute transitoire du tonus responsable de mouvements de flexion brusque puis extension des poignets lors de la manœuvre de Barré) avec, parfois, des signes extrapyramidaux (par dépôts de manganèse dans les ganglions de la base : intérêt de l’IRM encéphalique) et des crises d’épilepsie.
![]() Au stade de coma, des myoclonies, des signes focaux, des mouvements de décérébration sont possibles. L’EEG montre des signes (non spécifiques) évocateurs d’une encéphalopathie : ralentissement et diffusion du rythme de base, ondes triphasiques. L’évolution dépend du stade de la maladie, du traitement des facteurs déclenchants : saignement, apport protidique trop important, prise de benzodiazépines, infection, trouble métabolique.
Au stade de coma, des myoclonies, des signes focaux, des mouvements de décérébration sont possibles. L’EEG montre des signes (non spécifiques) évocateurs d’une encéphalopathie : ralentissement et diffusion du rythme de base, ondes triphasiques. L’évolution dépend du stade de la maladie, du traitement des facteurs déclenchants : saignement, apport protidique trop important, prise de benzodiazépines, infection, trouble métabolique.
Le traitement curatif associe lactulose et néomycine (par sonde nasogastrique ou lavement). Le traitement préventif est celui des facteurs déclenchants.
B Troubles cognitifs
1 Liés à l’alcool
![]() Les troubles cognitifs liés à l’alcool mais non liés à la maladie de Marchiafava-Bignami ou au syndrome de Korsakoff (voir plus loin) font toujours l’objet d’une certaine controverse. En effet, de nombreux facteurs peuvent être impliqués : effet toxique propre, carences vitami-niques, hépatopathies, traumatismes crâniens répétés, accidents vasculaires cérébraux, effet du vieillissement, possible pathologie dégénérative associée.
Les troubles cognitifs liés à l’alcool mais non liés à la maladie de Marchiafava-Bignami ou au syndrome de Korsakoff (voir plus loin) font toujours l’objet d’une certaine controverse. En effet, de nombreux facteurs peuvent être impliqués : effet toxique propre, carences vitami-niques, hépatopathies, traumatismes crâniens répétés, accidents vasculaires cérébraux, effet du vieillissement, possible pathologie dégénérative associée.
Bien que des critères diagnostiques aient été proposés, ils reposent pour l’essentiel sur des durées de consommation et de sevrage, ainsi que sur des quantités d’alcool absorbées. Le tableau clinique reste en effet imprécis : les troubles dysexécutifs (y compris comportementaux, comme apathie et bradypsychie) sont les plus fréquents, associés aux troubles mnésiques (mémoire épisodique verbale et de travail). Les troubles du langage sont inhabituels et doivent orienter vers une autre étiologie.
L’imagerie cérébrale montre une atrophie corticale diffuse mais sans corrélation avec les signes cliniques.
2 Syndrome de Korsakoff
Il est le plus souvent la conséquence d’une encéphalopathie de Gayet-Wernicke (voir plus haut) mal ou non traitée : plus rarement, il apparaît d’emblée, sans phase encéphalopathique préalable.
![]() Il traduit l’atteinte des corps mamillaires, des noyaux dorsomédians du thalamus, du trigone, du gyrus cingulaire. Cette lésion du circuit hippocampo-mamillo-thalamique (circuit de Papez) et l’atteinte frontale associée sont responsables du syndrome amnésique combiné à des signes dysexécutifs.
Il traduit l’atteinte des corps mamillaires, des noyaux dorsomédians du thalamus, du trigone, du gyrus cingulaire. Cette lésion du circuit hippocampo-mamillo-thalamique (circuit de Papez) et l’atteinte frontale associée sont responsables du syndrome amnésique combiné à des signes dysexécutifs.
![]() L’amnésie est principalement antérograde (avec au maximum un « oubli à mesure »), classiquement associée à des fausses reconnaissances et fabulations.
L’amnésie est principalement antérograde (avec au maximum un « oubli à mesure »), classiquement associée à des fausses reconnaissances et fabulations.
![]() L’imagerie cérébrale objective parfois une atrophie des corps mamillaires (fig. 2.1).
L’imagerie cérébrale objective parfois une atrophie des corps mamillaires (fig. 2.1).
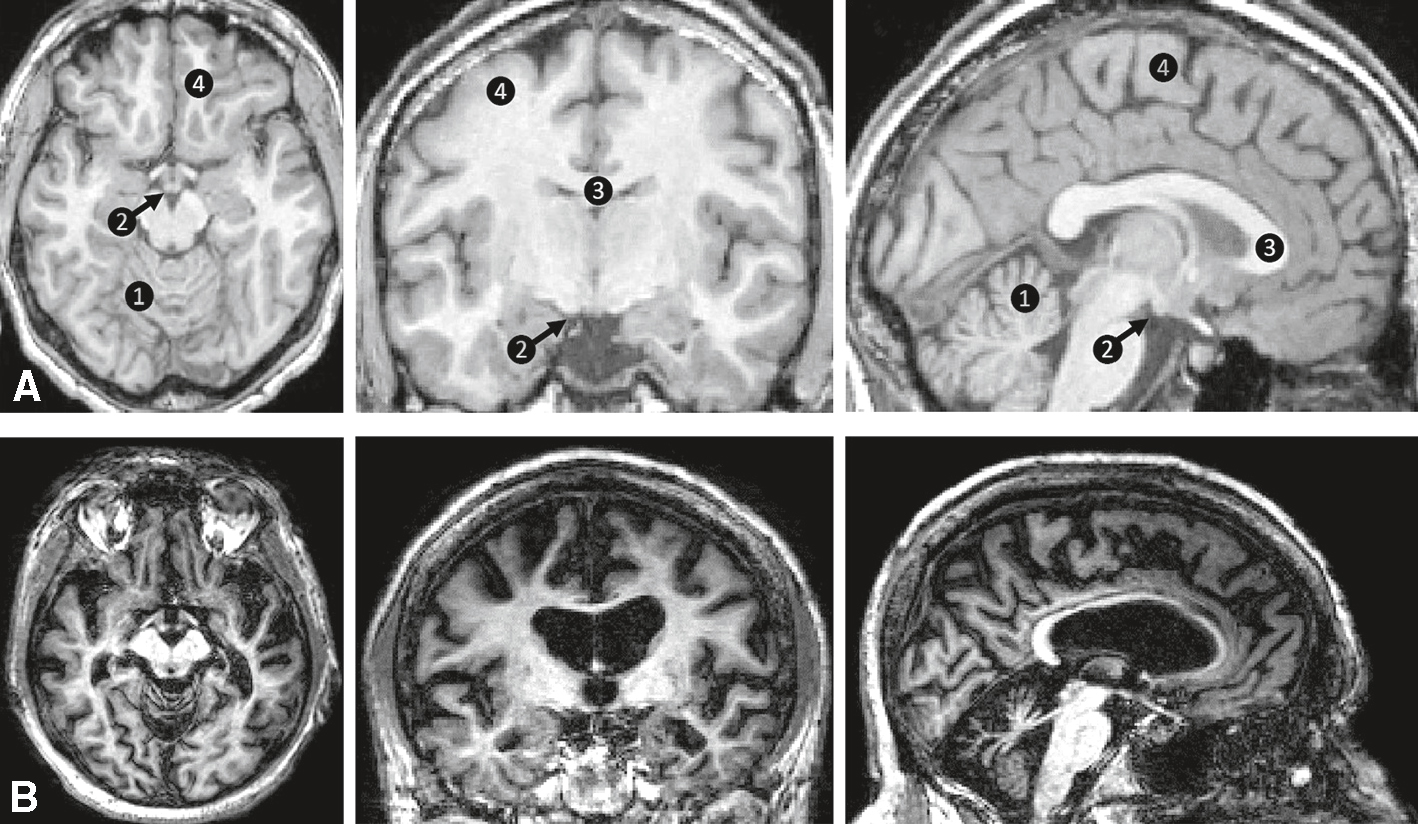
 Syndrome de Korsakoff.
Syndrome de Korsakoff. IRM T1 axiale (à gauche), coronale (au milieu), sagittale (à droite). 1. Cervelet. 2. Corps mamillaire (flèche noire). 3. Corps calleux. 4. Cortex. A. Sujet sain. B. Syndrome de Korsakoff : atrophie du cervelet, des corps mamillaires, du corps calleux et du cortex.
Sur les images en T1 pondéré, en séries axiales, coronales et sagittales (rangée A), on observe un hypersignal symétrique des corps mamillaires (repère 2) et du thalamus médian (repère 3), souvent atteint dans les encéphalopathies carentielles. L’atrophie des corps mamillaires est nette sur le plan sagittal, accompagnée d’un élargissement des sillons corticaux (repère 4), suggérant une perte de volume cortical diffuse. Le fornix (repère 1) paraît aminci, probablement secondaire à une dégénérescence transneuronale. En B, l’atrophie hippocampique est notable, avec des ventricules dilatés, caractéristiques d’un syndrome de Korsakoff chronique. Pas de rehaussement anormal ni de signe d’hémorragie active.
19Le traitement vitaminique parenteral est nécessaire, parfois partiellement efficace. Les conséquences sociales sont majeures, avec la présence constante d’une tierce personne ou la nécessité d’un placement en institution, ce qui n’est jamais aisé avec des sujets souvent jeunes.
3 Maladie de Marchiafava-Bignami
![]() La maladie de Marchiafava-Bignami se caractérise par une démyélinisation du corps calleux, parfois plus étendue latéralement.
La maladie de Marchiafava-Bignami se caractérise par une démyélinisation du corps calleux, parfois plus étendue latéralement.
La présentation clinique est aspécifique : démence avec mutisme akinétique, troubles de la marche (astasie-abasie), dysarthrie, hypertonie. Les signes de dysconnexion calleuse sont souvent mis en évidence a posteriori. Plus rarement, le tableau est celui d’une encéphalopathie avec confusion puis coma.
Le diagnostic est confirmé par l’aspect du corps calleux en imagerie : hypodense au scanner (bien visible en avant et en arrière des cavités ventriculaires sur les coupes axiales) et hyposignal T1/hypersignal T2 à l’IRM (fig. 2.2). Le pronostic à moyen terme est classiquement sombre, mais une atteinte limitée avec régression partielle des signes est possible.
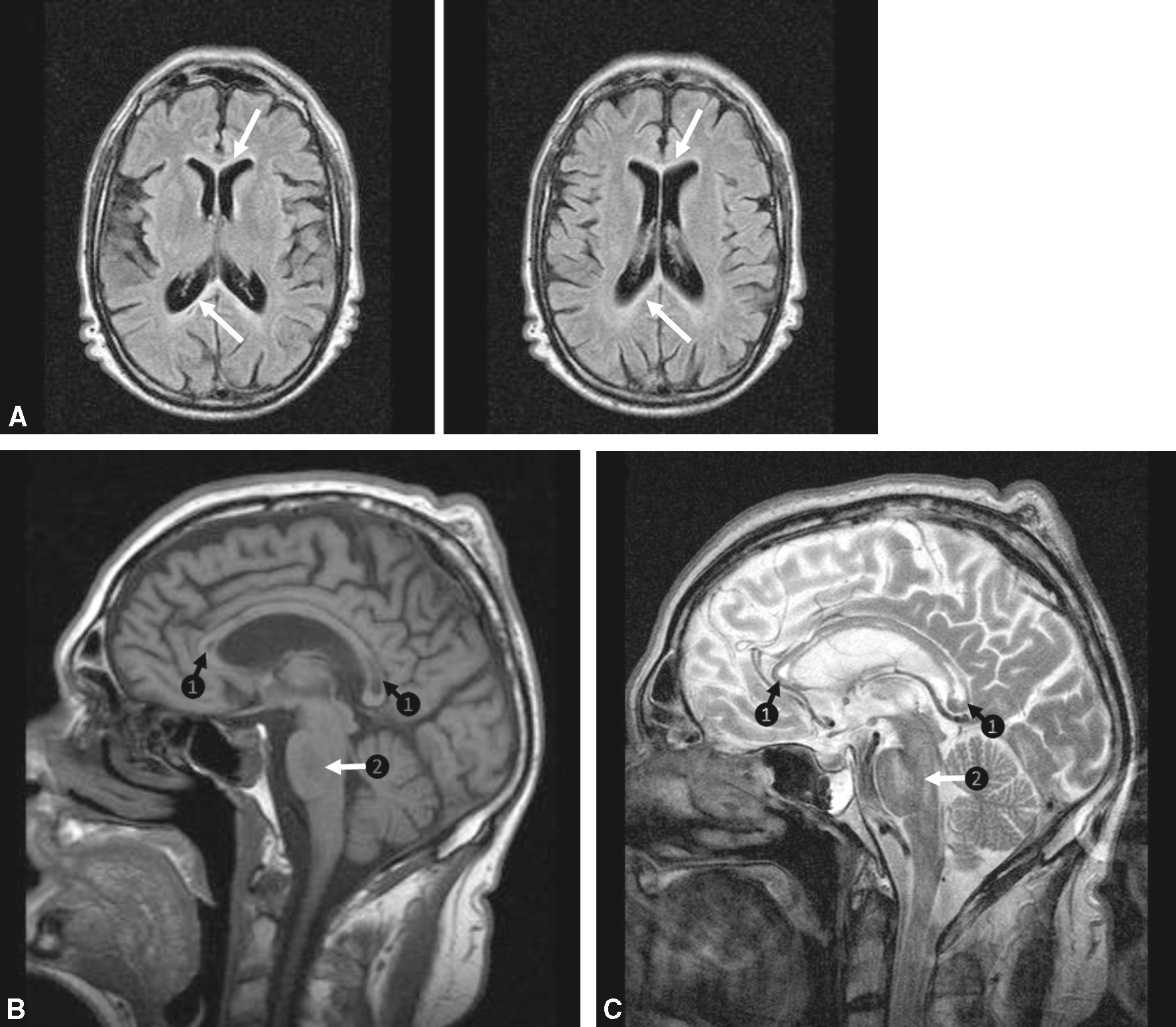
 Maladie de Marchiafava-Bignami.
Maladie de Marchiafava-Bignami. A. IRM axiale FLAIR. Hypersignaux du corps calleux (flèches blanches). B. IRM sagittale T1. 1. Hyposignaux du corps calleux (flèches noires). 2. Hyposignal du pont (ou protubérance) (flèche blanche). C. IRM sagittale T2. 1. Hypersignaux du corps calleux (flèches noires). 2. Hypersignal du pont (ou protubérance) (flèche blanche).
Sur les coupes axiales FLAIR (A), on observe un hypersignal symétrique du corps calleux, plus marqué en région moyenne et postérieure, avec des flèches blanches pointant ces lésions. En sagittal T1 (B), la flèche blanche marquée 2 montre une zone d’hyposignal localisée dans la partie moyenne du corps calleux (corpus callosum), traduisant une démyélinisation. Les flèches noires numérotées 1 désignent l’atteinte du splénium et du genu, parties postérieure et antérieure du corps calleux respectivement. En C, coupe sagittale T2, on retrouve les mêmes localisations avec un hypersignal du corps calleux (repères 1) et du pont (repère 2), caractéristique d’une démyélinisation alcoolique. Aucun effet de masse ni rehaussement n’est observé, ce qui appuie le diagnostic de maladie de Marchiafava-Bignami.
C Épilepsie
![]() L’éthylisme chronique est une des causes les plus fréquentes d’épilepsie tardive : les crises surviennent de façon aléatoire après de nombreuses années d’intoxication mais indépendamment du rythme d’ingestion.
L’éthylisme chronique est une des causes les plus fréquentes d’épilepsie tardive : les crises surviennent de façon aléatoire après de nombreuses années d’intoxication mais indépendamment du rythme d’ingestion.
L’épilepsie peut revêtir tous les types de crises, mais elle est le plus souvent généralisée, et peut continuer à se manifester après le sevrage en cas de lésions cérébrales irréversibles dues à l’alcool.
Elle ne nécessite un traitement antiépileptique au long cours que s’il y a un risque de crise avéré en dehors de toute alcoolisation, avec trois écueils : la mauvaise compliance (qui fera préférer des molécules à demi-vie longue comme le phénobarbital), le risque de dépendance, une modification du métabolisme des antiépileptiques par l’alcool (prudence vis-à-vis des antiépileptiques hépatotoxiques en cas d’hépatopathies liées à l’alcool).
20
D 21Neuropathies
1 Neuropathie optique alcoolotabagique
![]() La neuropathie optique alcoolotabagique se manifeste par une baisse bilatérale de l’acuité visuelle avec dyschromatopsie, scotome central, pâleur papillaire tardive. Favorisée par l’association à une consommation tabagique, son traitement repose principalement sur la vitamino-thérapie B et l’arrêt de l’alcoolotabagisme.
La neuropathie optique alcoolotabagique se manifeste par une baisse bilatérale de l’acuité visuelle avec dyschromatopsie, scotome central, pâleur papillaire tardive. Favorisée par l’association à une consommation tabagique, son traitement repose principalement sur la vitamino-thérapie B et l’arrêt de l’alcoolotabagisme.
2 Polyneuropathie longueur-dépendante
a Forme chronique
Due à la toxicité directe de l’alcool, la polyneuropathie longueur-dépendante s’associe aux conséquences de la carence en vitamine B1 et en folates. La neuropathie toxique alcoolique touche surtout les petites fibres sensitives (véhiculant la sensibilité thermoalgique). La neuropathie carentielle en vitamine B1 a préférentiellement des conséquences motrices, parfois aiguës (voir plus loin). Les signes de début comportent : crampes nocturnes, fatigue à la marche avec douleur à la pression des mollets, hypoesthésie douloureuse et aréflexie achil-léenne. Le traitement repose sur l’arrêt de l’intoxication éthylique. La recharge vitaminique n’est utile qu’en cas de carence associée (attention au risque d’hématomes en cas d’injection IM). Il convient de chercher une ou d’autres causes intriquées éventuelles (diabète, médicaments neurotoxiques, gammapathie monoclonale, insuffisance rénale).
À un stade évolué, il existe des douleurs (brûlure, étau, hyperesthésie au contact), une anes-thésie distale symétrique « en chaussettes », un steppage et des signes trophiques en rapport avec une neuropathie autonome distale (dépilation, troubles de la sudation, impuissance, parfois maux perforants plantaires) et cardiaque, source d’une augmentation de la mortalité.
Le traitement associe, outre le sevrage alcoolique, vitaminothérapie et renutrition en cas de carence, antalgiques (antiépileptiques et/ou tricycliques), soins locaux, rééducation, orthèses. La récupération est lente et souvent incomplète.
b Forme aiguë
Rare, essentiellement en rapport avec une carence en vitamine B1 favorisée par une dénutrition, elle évoque parfois un syndrome de Guillain-Barré. Elle s’associe souvent à une encéphalopathie de Gayet-Wernicke. Le tableau est celui d’une paraparésie douloureuse amyotrophiante, flasque et aréflexique, s’installant en 24 heures. La prise en charge impose la recharge en vitamine B1 parentérale et les mesures d’accompagnement (voir plus loin).
3 Neuropathies focales
Des neuropathies focales sont favorisées par l’amaigrissement, source de compressions nerveuses.
E 22Myopathies
1 Myopathie aiguë
![]() Rare, lors d’une ingestion massive, la myopathie aiguë associe myalgies, œdème, déficit proximal, rhabdomyolyse, myoglobinurie, créatines kinases (CK) élevées, risque d’insuffisance rénale (par nécrose tubulaire).
Rare, lors d’une ingestion massive, la myopathie aiguë associe myalgies, œdème, déficit proximal, rhabdomyolyse, myoglobinurie, créatines kinases (CK) élevées, risque d’insuffisance rénale (par nécrose tubulaire).
2 Myopathie chronique
![]() Fréquente, asymptomatique ou réduite à une faiblesse proximale, la myopathie chronique est en rapport avec une modification du calibre des fibres de type II : l’électromyogramme (EMG) montre des tracés myogènes (avec tracés neurogènes souvent associés).
Fréquente, asymptomatique ou réduite à une faiblesse proximale, la myopathie chronique est en rapport avec une modification du calibre des fibres de type II : l’électromyogramme (EMG) montre des tracés myogènes (avec tracés neurogènes souvent associés).
IV Complications neurologiques indirectes de l’alcoolisme
A Myélinolyse centropontine
![]() Rare, de physiopathologie complexe, associée à la dénutrition, la myélinolyse centropontine est favorisée par l’hyponatrémie et sa correction trop rapide. Elle comporte un trouble de la vigilance avec une tétraplégie et des signes pseudobulbaires traduisant la démyélinisation des fibres du centre du pont (ou protubérance) visible à l’IRM cérébrale (fig. 2.3 : hypersignal T2 et FLAIR), parfois étendue à la substance blanche hémisphérique. Le pronostic est péjoratif. Le traitement est préventif : correction progressive des hyponatrémies profondes.
Rare, de physiopathologie complexe, associée à la dénutrition, la myélinolyse centropontine est favorisée par l’hyponatrémie et sa correction trop rapide. Elle comporte un trouble de la vigilance avec une tétraplégie et des signes pseudobulbaires traduisant la démyélinisation des fibres du centre du pont (ou protubérance) visible à l’IRM cérébrale (fig. 2.3 : hypersignal T2 et FLAIR), parfois étendue à la substance blanche hémisphérique. Le pronostic est péjoratif. Le traitement est préventif : correction progressive des hyponatrémies profondes.
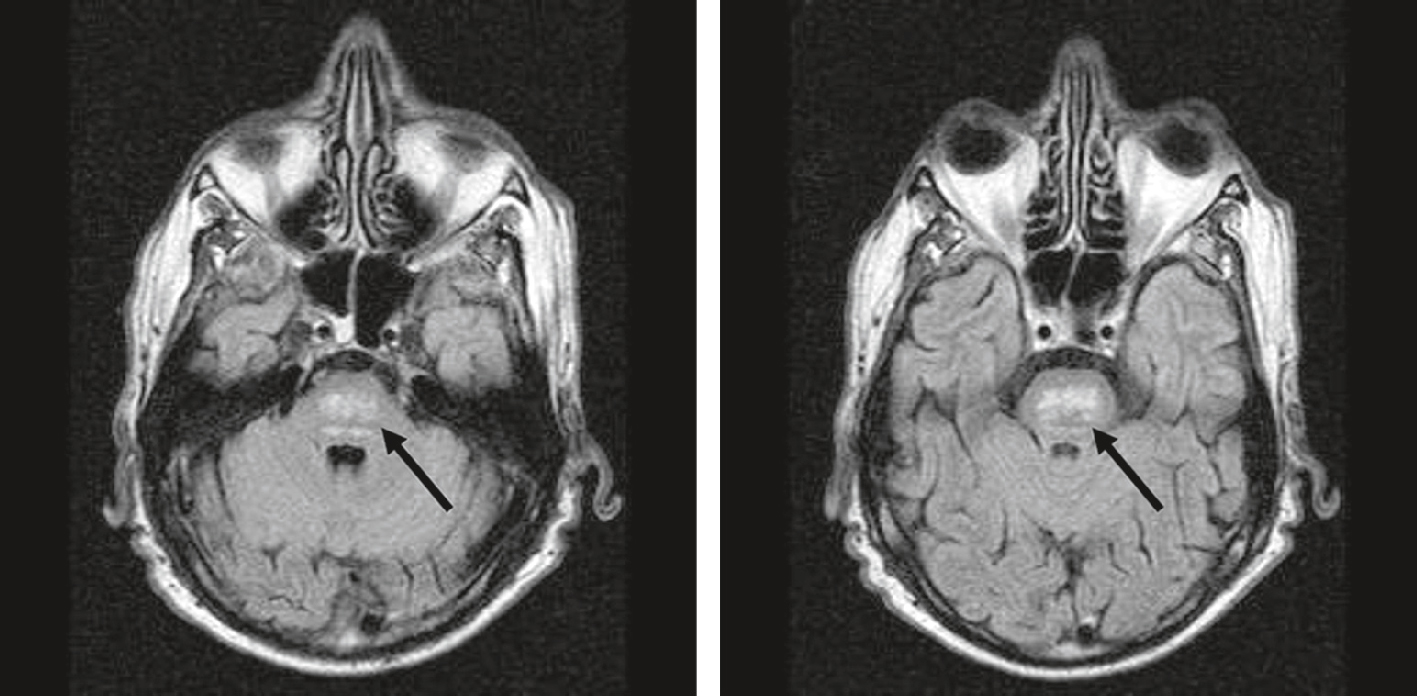
 Myélinolyse centropontine.
Myélinolyse centropontine. IRM axiale FLAIR. Hypersignaux du pont (ou protubérance) (flèches noires).
Sur ces deux coupes axiales pondérées T1, on observe au centre du pont une lésion bien circonscrite, clairement désignée par une flèche noire sur chaque image. À gauche, l’IRM montre une zone d’hyposignal, homogène, centrée dans la partie centrale du pont, sans effet de masse ni œdème périphérique. À droite, l’image met en évidence une région hyperintense anormale en T2, également localisée dans le pont. L’aspect est typique d’une atteinte de la substance blanche centrale du tronc cérébral, en accord avec une myélinolyse centropontine. Les structures environnantes telles que les pédoncules cérébelleux et les noyaux de la base semblent épargnées. Ce tableau radiologique est évocateur d’une démyélinisation osmotique, souvent liée à une correction trop rapide d’une hyponatrémie sévère.
B Accidents vasculaires cérébraux
![]() L’intoxication aiguë peut entraîner un AVC ischémique par thromboembolie d’origine cardiaque (par troubles du rythme liés à une cardiomyopathie alcoolique).
L’intoxication aiguë peut entraîner un AVC ischémique par thromboembolie d’origine cardiaque (par troubles du rythme liés à une cardiomyopathie alcoolique).
23L’intoxication alcoolique chronique est un facteur de risque d’hémorragie cérébrale et/ou méningée. Différents mécanismes sont évoqués : troubles de la coagulation (taux de prothrombine abaissé par insuffisance hépatique, thrombopénie alcoolique, thrombopathie modifiant le temps saignement), hypertension artérielle (HTA).
C Traumatismes crâniens
Du fait de chutes (lors d’ivresse aiguë, de crises d’épilepsie), l’alcoolique chronique est exposé aux traumatismes crâniens itératifs, responsables de contusions cérébrales hémorragiques, d’hématomes sous-duraux aigus ou chroniques et extraduraux.
D Neuro-infections
La dénutrition et la précarité immunitaire exposent le patient alcoolique à des pathologies infectieuses comme la méningite tuberculeuse.
E Neuropathie au disulfirame
![]() Le disulfirame est donné pour son effet antabuse (effet de flush, céphalées, nausées, vomissement) lors de la consommation d’alcool dans une démarche de prévention.
Le disulfirame est donné pour son effet antabuse (effet de flush, céphalées, nausées, vomissement) lors de la consommation d’alcool dans une démarche de prévention.
Il a une toxicité neurologique, hépatique et dermatologique à dose élevée.
Il peut induire une neuropathie axonale distale sensitive, douloureuse, qui ne doit pas être prise pour une récidive d’une neuropathie alcoolique. La neuropathie peut s’associer à une toxicité centrale (somnolence, céphalées).
F Syndrome alcoolique fœtal
![]() Les mères alcooliques et dénutries risquent d’accoucher de nourrissons souffrant d’une dysmorphie et d’un retard mental.
Les mères alcooliques et dénutries risquent d’accoucher de nourrissons souffrant d’une dysmorphie et d’un retard mental.
24
1www.santepubliquefrance.fr/determinants-de-sante/alcool; mise à jour du 06/05/2024.
