Situations de départ
 837 Incontinence fécale.
837 Incontinence fécale.
 23 Anomalie de la miction.
23 Anomalie de la miction.
 65 Déformation rachidienne.
65 Déformation rachidienne.
 66 Apparition d’une difficulté à la marche.
66 Apparition d’une difficulté à la marche.
 69 Claudication intermittente d’un membre.
69 Claudication intermittente d’un membre.
 71 Douleur d’un membre (supérieur ou inférieur).
71 Douleur d’un membre (supérieur ou inférieur).
 72 Douleur du rachis (cervical, dorsal ou lombaire).
72 Douleur du rachis (cervical, dorsal ou lombaire).
 73 Douleur, brûlure, crampes et paresthésies.
73 Douleur, brûlure, crampes et paresthésies.
 74 Faiblesse musculaire.
74 Faiblesse musculaire.
 97 Rétention aiguë d’urines.
97 Rétention aiguë d’urines.
 121 Déficit neurologique sensitif et/ou moteur.
121 Déficit neurologique sensitif et/ou moteur.
 130 Troubles de l’équilibre.
130 Troubles de l’équilibre.
 233 Identifier/reconnaître les différents examens d’imagerie (type/fenêtre/séquences/incidences/injection).
233 Identifier/reconnaître les différents examens d’imagerie (type/fenêtre/séquences/incidences/injection).
 243 Mise en place et suivi d’un appareil d’immobilisation.
243 Mise en place et suivi d’un appareil d’immobilisation.
 245 Prescription d’un appareillage simple.
245 Prescription d’un appareillage simple.
 247 Prescription d’une rééducation.
247 Prescription d’une rééducation.
 327 Annonce d’un diagnostic de maladie grave au patient et/ou à sa famille.
327 Annonce d’un diagnostic de maladie grave au patient et/ou à sa famille.
 345 Situation de handicap.
345 Situation de handicap.
Objectifs pédagogiques
 Diagnostiquer une compression médullaire non traumatique et un syndrome de la queue de cheval.
Diagnostiquer une compression médullaire non traumatique et un syndrome de la queue de cheval.
 Identifier les situations d’urgence et planifier leur prise en charge.
Identifier les situations d’urgence et planifier leur prise en charge.
 Comprendre les principaux déficits et incapacités secondaires à une compression médullaire ou un syndrome de la queue de cheval.
Comprendre les principaux déficits et incapacités secondaires à une compression médullaire ou un syndrome de la queue de cheval.
84Hiérarchisation des connaissances
| Rang | Rubrique | Intitulé | Descriptif |
|---|---|---|---|
| Éléments physiopathologiques | Connaître la physiopathologie des lésions médullaires et d’un syndrome de la queue de cheval | ||
| Diagnostic positif | Connaître les signes cliniques d’une compression médullaire | Décrire les principaux symptômes révélateurs. Diagnostiquer et décrire la sémiologie clinique du syndrome radiculaire lésionnel et le syndrome sous-lésionnel | |
| Examens complémentaires | Savoir hiérarchiser les examens complémentaires devant une suspicion de compression médullaire | Ne pas faire de PL avant d’avoir fait une imagerie de la moelle épinière | |
| Examens complémentaires | Savoir faire le diagnostic d’une compression médullaire à l’imagerie | ||
| Contenu multimédia | Exemple d’une IRM typique de compression médullaire | Savoir reconnaître sur une IRM le cordon médullaire, la queue de cheval et les structures avoisinantes | |
| Étiologies | Connaître les étiologies d’une compression médullaire | Différencier les causes extradurales, intradurales et extramédullaires, ainsi qu’intramédullaires | |
| Diagnostic positif | Connaître le diagnostic différentiel | ||
| Diagnostic positif | Connaître les formes topographiques | Savoir mettre en évidence les éléments cliniques des différents niveaux de compression médullaire dorsale, cervicale basse, cervicale haute | |
| Identifier une urgence | Savoir identifier des situations d’urgence devant une compression médullaire | ||
| Prise en charge | Connaître les principes de la prise en charge des situations d’urgence devant une compression médullaire | ||
| Diagnostic positif | Savoir faire le diagnostic clinique d’un syndrome de la queue de cheval | ||
| Examens complémentaires | Savoir hiérarchiser les examens complémentaires d’un syndrome de la queue de cheval | ||
| Examens complémentaires | Savoir faire le diagnostic radiologique d’un syndrome de la queue de cheval | ||
| Contenu multimédia | IRM typique de syndrome de la queue de cheval | ||
| Étiologies | Connaître les étiologies d’un syndrome de la queue de cheval | ||
| Diagnostic positif | Connaître le diagnostic différentiel d’un syndrome de la queue de cheval | ||
| Identifier une urgence | Savoir identifier les situations d’urgence devant un syndrome de la queue de cheval | ||
| Prise en charge | Connaître les principes de la prise en charge des situations d’urgence devant un syndrome de la queue de cheval | ||
| Suivi et/ou pronostic | Comprendre les principaux déficits et incapacités secondaires à une compression médullaire ou un syndrome de la queue de cheval | Conséquences et handicaps principaux sans les détailler | |
| Prise en charge | Connaître les principes essentiels de prise en charge des déficits, incapacités et handicaps secondaires à une compression médullaire ou un syndrome de la queue de cheval* | ||
| Contenu multimédia | Évoquer un diagnostic de compression médullaire sur un cas vidéo* |
Compression médullaire non traumatique
- I 85Rappels anatomiques
- II Clinique
- III Examens complémentaires
- IV Étiologie
- V Diagnostic différentiel
- VI Principes de la prise en charge
I Rappels anatomiques
![]() Voir le référentiel du 1er cycle « les fondamentaux de la pathologie neurologique ».
Voir le référentiel du 1er cycle « les fondamentaux de la pathologie neurologique ».
La moelle spinale chemine du trou occipital au bord supérieur de L2 dans un canal ostéoliga-mentaire inextensible. Elle est plus courte que le canal rachidien, ce qui explique un décalage entre le niveau vertébral et celui du métamère médullaire (par exemple, le métamère T12 est en regard de la vertèbre T9).
De la moelle spinale émergent les nerfs spinaux, qui sortent par les trous de conjugaison.
La moelle spinale se termine par le cône terminal au niveau des dernières vertèbres thoraciques et de L1; les dernières racines spinales (L2 à L5 et les racines sacrées) forment la queue de cheval.
La moelle spinale est entourée par la pie-mère qui y est adhérente, puis par l’arachnoïde sous laquelle circule le liquide cérébrospinal (LCS) et la dure-mère, épaisse et résistante, qui réalise un fourreau cylindrique épais. L’espace extradural est graisseux, rempli de vaisseaux, principalement veineux.
La moelle spinale est organisée transversalement en métamères et longitudinalement en fibres longues (fig. 7.1). Elles comportent des fibres sensitives et des fibres motrices :
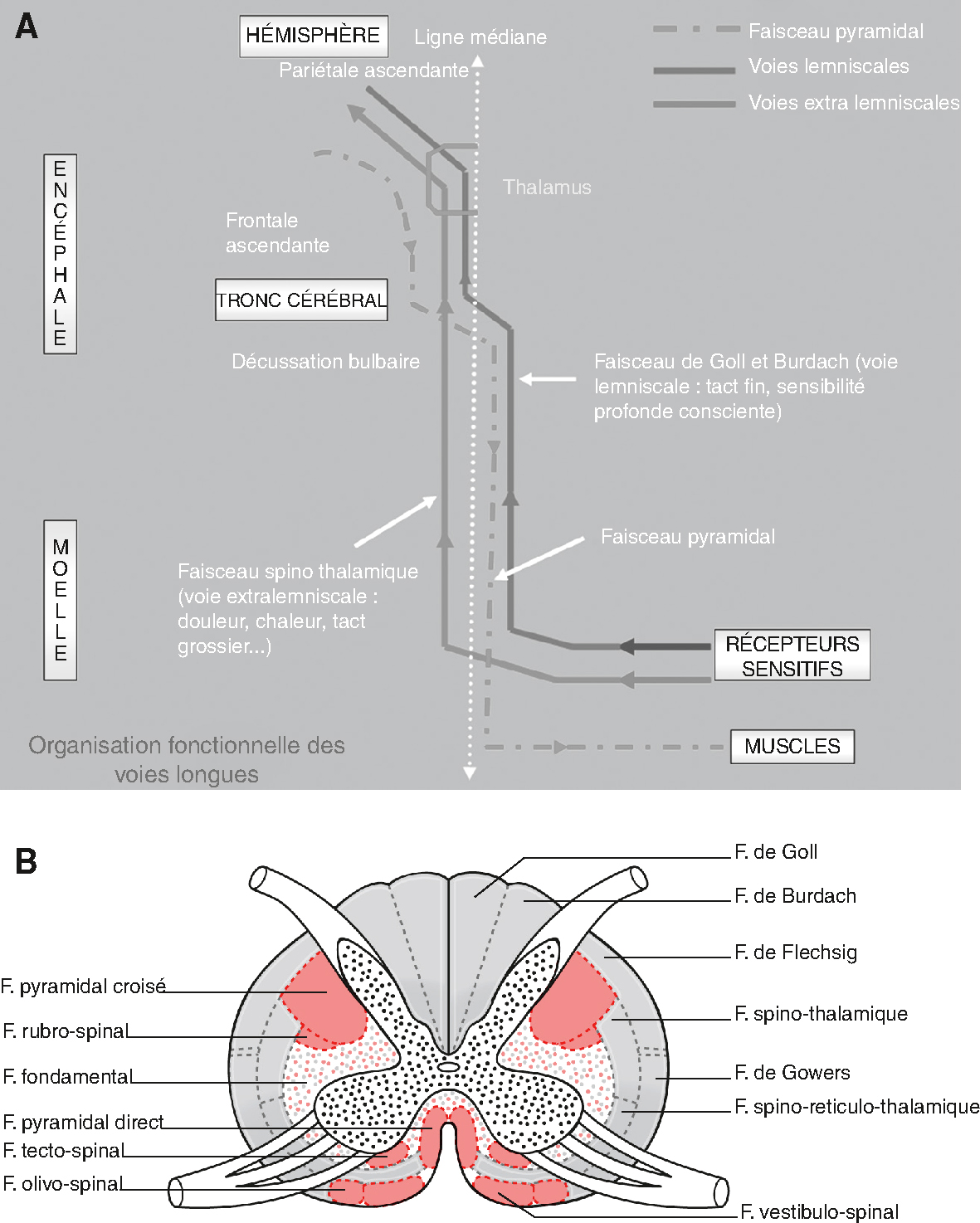
 Moelle spinale.
Moelle spinale. A. Coupe longitudinale. B. Coupe transversale.
Illustrations doctrinales représentant le tissu des longues traces de la marque de la colonne vertébrale dans la coupe longitudinale (A) et la section transversale (b). Dans A, les rayons corticospinés (ou pyramide) sont poursuivis après des descendants du cortex moteur à la marque au niveau de la décasion des pyramides et traversent la ligne centrale. La voie sensible croissante, représentée par le gris (du GOL) et en forme de coin (de Burdach), combine les tiges cérébrales et se synchronise avec le noyau sensible. La figure B explique la disposition des rayons de matériel blanc sur le marché. 4 Lumière avant et moteur extérieur et l'éclat du spinosalamic, des célibataires et du citoyen à l'arrière. Les zones roses et grises distinguent les moteurs et les rôles sensibles.
-
• les fibres sensitives se répartissent principalement :
- – en voie spinothalamique (ou extralemniscale), qui véhicule la sensibilité thermoalgique et le tact protopathique : elles croisent à chaque niveau métamérique; elles cheminent dans le cordon latéral de la moelle du côté opposé,
- – en voie lemniscale, qui véhicule le tact épicritique et la sensibilité profonde, située dans le cordon postérieur de la moelle spinal, homolatéral; elles croiseront plus haut à la partie inférieure de la moelle allongée (bulbe);
- • le faisceau pyramidal moteur, après avoir croisé dans la moelle allongée, descend dans le cordon latéral de la moelle spinale.
86Certains éléments cliniques orientant vers une compression médullaire découlent de cette organisation anatomofonctionnelle :
- • un syndrome lésionnel en regard de la compression (douleur radiculaire, déficit radiculaire);
- • l’existence d’un niveau sensitif correspondant à la limite supérieure de l’atteinte sensitive;
- • un syndrome sous-lésionnel : dysfonctionnement de la moelle sous-jacente privée du contrôle central (déficit sensitif, déficit moteur, signes d’irritation pyramidale, hypertonie pyramidale, troubles sphinctériens);
- • un syndrome douloureux rachidien.
II Clinique
La compression médullaire non traumatique doit être diagnostiquée dès les premiers signes cliniques, car elle nécessite une prise en charge urgente.
Le diagnostic de compression médullaire non traumatique est posé sur l’existence d’un syndrome lésionnel et d’un syndrome sous-lésionnel associé le plus souvent à des signes rachidiens.
A 87Syndrome radiculaire lésionnel
Il comprend :
- • des douleurs radiculaires souvent isolées au début, de topographie constante, signalant le dermatome lésionnel (névralgies cervicobrachiales, algies thoraciques en ceinture). Elles surviennent en éclairs, par salves, impulsives à la toux. Elles peuvent s’estomper dans la journée avec l’activité physique et ne se manifester qu’au repos, surtout la nuit, à heures fixes, pouvant s’atténuer à la déambulation nocturne;
- • un possible déficit radiculaire avec hypoesthésie en bande dans le territoire douloureux avec abolition, diminution ou inversion d’un réflexe, pouvant aboutir à un déficit moteur dans le même territoire radiculaire avec amyotrophie. Ces symptômes sont au début plus discrets à l’étage thoracique ou abdominal qu’au niveau cervical, où la névralgie cervico-brachiale est plus typique.
Il permet donc de déterminer le niveau lésionnel et d’orienter les explorations neuroradiologiques.
B Syndrome sous-lésionnel
Le syndrome sous-lésionnel associe des troubles moteurs, sensitifs et sphinctériens.
1 Troubles moteurs
Syndrome pyramidal d’intensité variable :
- • simple fatigabilité à la marche, difficulté à la course, maladresse en terrain accidenté, cédant à l’arrêt;
- • gêne non douloureuse correspondant à la claudication intermittente de la moelle;
- • progressivement, réduction du périmètre de marche pouvant aboutir à un confinement au fauteuil en raison d’une paraplégie ou d’une tétraplégie spastique.
Il faut noter la différence avec l’installation des signes cliniques dans un contexte de compression médullaire aiguë qui se fera initialement par un déficit moteur flasque, suivi de l’installation plus lente du syndrome pyramidal.
2 Troubles sensitifs
Ils sont retardés : picotements, fourmillements, sensations de striction, d’étau, de ruissellement d’eau glacée, de brûlures parfois exacerbées au contact. Un signe de Lhermitte est possible (décharge électrique le long du rachis et des membres à la flexion du cou).
Le patient a l’impression de marcher sur du coton ou du caoutchouc avec une gêne plus marquée lors de la fermeture des yeux (souffrance cordonale postérieure).
Le déficit sensitif n’est pas toujours complet, initialement cordonal postérieur (atteinte de la sensibilité discriminative, de la proprioception) ou spinothalamique (déficit thermoalgique).
Il existe un niveau sensitif correspondant au métamère inférieur de la compression.
3 Troubles sphinctériens
Troubles urinaires (miction impérieuse, dysurie), sexuels ou anorectaux (constipation) sont très tardifs dans les compressions médullaires, sauf si la lésion est située dans le cône terminal.
Dans les compressions médullaires évoluées, ils sont quasi constants.
C 88Syndrome rachidien
- • Les douleurs, permanentes et fixes, localisées ou plus diffuses, à type de tiraillement, de pesanteur ou d’enraidissement rachidien, augmentent à l’effort mais elles existent aussi au repos et la nuit.
- • Elles sont peu ou pas sensibles aux antalgiques usuels.
- • Une raideur segmentaire du rachis, très précoce, est à rechercher systématiquement.
- • Une déformation segmentaire (cyphose, scoliose, torticolis) est possible, avec douleurs spontanées localisées accrues lors de la percussion des épineuses ou à la palpation appuyée de la musculature paravertébrale en regard de la zone lésionnelle.
III 89Examens complémentaires
![]() Une ponction lombaire peut aussi être à l’origine d’une décompensation brutale et doit être proscrite devant un tableau de compression médullaire en l’absence d’IRM.
Une ponction lombaire peut aussi être à l’origine d’une décompensation brutale et doit être proscrite devant un tableau de compression médullaire en l’absence d’IRM.
A IRM
L’IRM est l’examen urgent de première intention (séquences T1, T2, sans puis avec injection de gadolinium) :
- •
 étude du cordon médullaire dans les deux plans de l’espace (sagittal et axial) et observation des structures avoisinantes;
étude du cordon médullaire dans les deux plans de l’espace (sagittal et axial) et observation des structures avoisinantes; - • détermination du niveau médullaire concerné et de la topographie lésionnelle, épidurale, intradurale extra- ou intramédullaire. En cas de processus compressif épidural, les anomalies squelettiques avoisinantes devront être recherchées;
- • tumeurs intradurales extramédullaires : masses arrondies ovoïdes jouxtant la moelle spinale;
- • lésions intramédullaires : élargissement du cordon médullaire (lésion médullaire dont l’aspect dépend de l’étiologie).
![]() L’IRM précise la cartographie du processus tumoral : hauteur, dimension, rapports avec les structures avoisinantes. La nature pleine ou kystique oriente l’étiologie. S’il y a rehaussement par injection de gadolinium, une origine tumorale, inflammatoire ou, plus rarement, infectieuse est évoquée.
L’IRM précise la cartographie du processus tumoral : hauteur, dimension, rapports avec les structures avoisinantes. La nature pleine ou kystique oriente l’étiologie. S’il y a rehaussement par injection de gadolinium, une origine tumorale, inflammatoire ou, plus rarement, infectieuse est évoquée.
90Elle permet également de juger du degré de rétrécissement pour évaluer le risque potentiel de souffrance médullaire suraiguë redoutée dans des compressions médullaires lentes.
B Autres examens (seulement et/ou en complément de l’IRM)
1 Scanner et myéloscanner
a Scanner en complément de l’IRM
![]() Il recherche et précise des modifications osseuses : calcifications, érosion d’un pédicule, élargissement d’un trou de conjugaison, élargissement du diamètre transversal ou antéropos-térieur du canal rachidien, aspect lytique ou condensant vertébral aboutissant à une vertèbre ivoire ou à un tassement.
Il recherche et précise des modifications osseuses : calcifications, érosion d’un pédicule, élargissement d’un trou de conjugaison, élargissement du diamètre transversal ou antéropos-térieur du canal rachidien, aspect lytique ou condensant vertébral aboutissant à une vertèbre ivoire ou à un tassement.
b Myéloscanner en cas de contre-indication à l’IRM
Coupes de scanner rachidien après injection intradurale (par ponction au niveau lombaire ou sous-occipital, selon la topographie de l’atteinte) de produit de contraste permettant de visualiser les rapports de la moelle spinale avec les structures adjacentes dont le rachis.
2 Radiographies rachidiennes simples
![]() Elles ne sont plus réalisées.
Elles ne sont plus réalisées.
![]() Elles sont remplacées par le scanner; elles sont utiles en dynamique parfois pour rechercher une instabilité (clichés en flexion et extension).
Elles sont remplacées par le scanner; elles sont utiles en dynamique parfois pour rechercher une instabilité (clichés en flexion et extension).
3 Potentiels évoqués somesthésiques et moteurs
Ils apprécient l’état fonctionnel des voies lemniscales et pyramidales.
Toutefois, ils ne constituent pas un instrument diagnostique de première intention.
IV Étiologie
A Causes extradurales
1 Métastases néoplasiques vertébrales et épidurites métastatiques
-
• Les causes extradurales sont dominées par les métastases néoplasiques vertébrales pouvant être compliquées d’une épidurite métastatique (fig. 7.3) :

Fig. 7.3  Métastase vertébrale avec épidurite.
Métastase vertébrale avec épidurite.
Lésion osseuse développée au niveau du corps de T4, massivement étendue aux pédicules et à l’arc postérieur à gauche (coupe axiale), en hyposignal T1, en hypersignal T2, fortement rehaussée après injection de gadolinium. Extension intracanalaire épidurale avec compression et engainement médullaires. Les espaces liquidiens péri-médullaires sont totalement effacés en regard de la compression. À noter, le respect des disques intervertébraux sus- et sous-jacents. A. T1 sagittal après injection. B. T2 sagittal. C. T1 sagittal. D. T1 axial après injection.Série d’images en imagerie par résonance magnétique (IRM) en coupes sagittales et axiales illustrant une métastase vertébrale compliquée d’une épidurite. Les coupes sagittales (A, B et C) montrent une infiltration pathologique d’un corps vertébral thoracique avec un hyposignal en T1 et un hypersignal en T2, traduisant un envahissement tumoral. Un effet de masse est visible, avec effacement du signal normal de la graisse épidurale postérieure et compression de la moelle épinière. L’image D en coupe axiale confirme la compression épidurale avec déformation circulaire de la moelle et envahissement des tissus périmédullaires. L’aspect évoque une épidurite secondaire à une localisation métastatique, nécessitant une prise en charge urgente pour prévenir un déficit neurologique.
- – cancers primitifs les plus fréquents retrouvés : poumon, sein, prostate, rein;
- – envahissement néoplasique vertébro-épidural fréquemment rencontré au cours d’hémo-pathies malignes : lymphomes non hodgkiniens, leucémies aiguës, myélomes.
- • Les épidurites métastatiques peuvent également survenir indépendamment d’une atteinte osseuse.
- • Les tumeurs vertébrales bénignes (hémangiome, chondrome) ou primitivement malignes (sarcome) sont rares à l’exception du myélome.
2 91Myélopathie cervicarthrosique
- • Compression médullaire lente cervicale.
- • Patients de plus de 40 ans aux antécédents de névralgies cervicobrachiales, de torticolis, de traumatismes rachidiens cervicaux.
- • Syndrome sous-lésionnel : syndrome pyramidal spastique progressif avec troubles sensitifs subjectifs (signe de Lhermitte).
- • Syndrome lésionnel : signes sensitifs et moteurs avec aréflexie, amyotrophie sur un ou les deux membres supérieurs.
-
• L’IRM confirme la cervicarthrose avec étroitesse du canal cervical et arthrose préférentiel-lement sur la partie inférieure du rachis cervical (fig. 7.4), hypersignal T2 intramédullaire fréquemment observé.
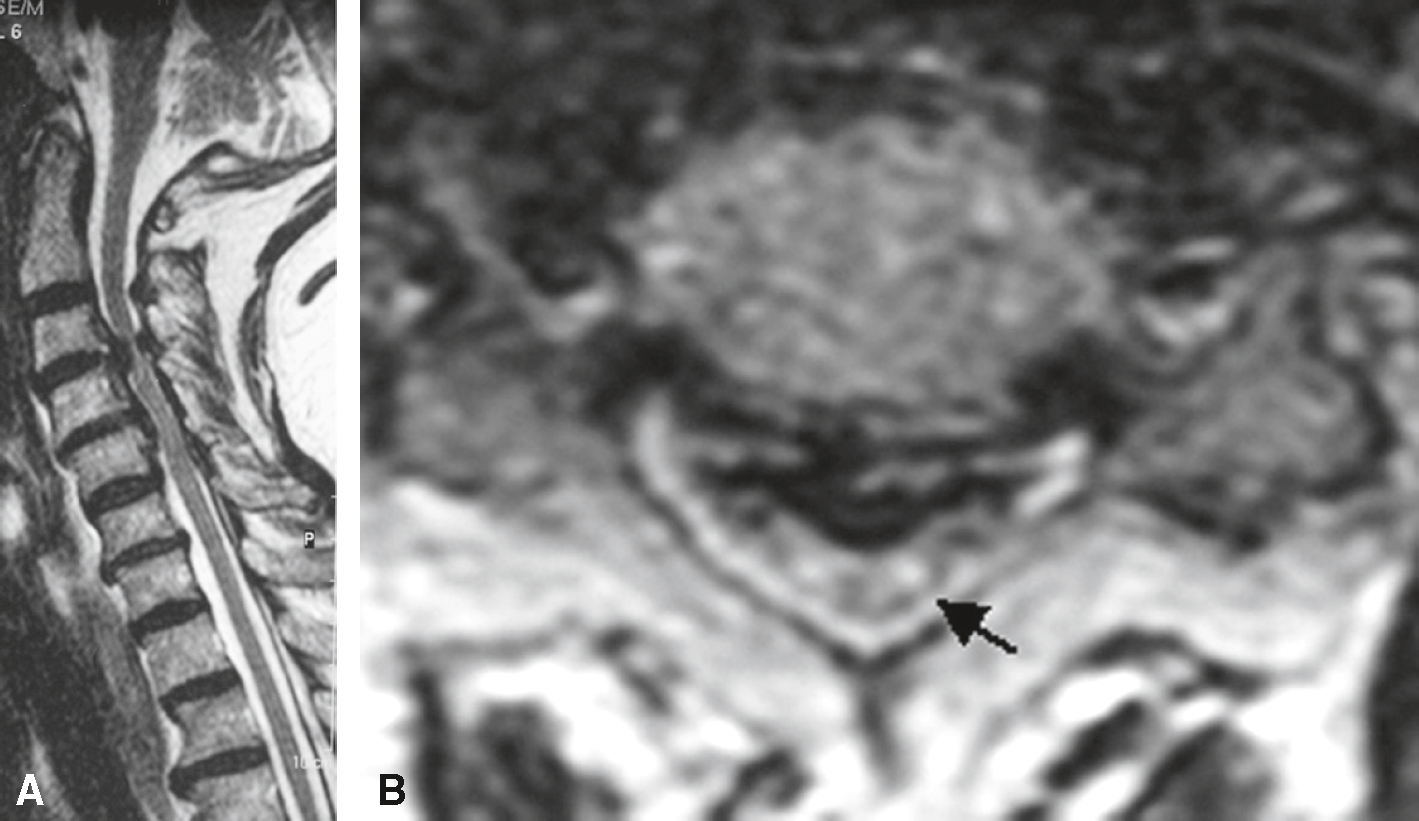
Fig. 7.4  Myélopathie cervicarthrosique.
Myélopathie cervicarthrosique.
Sténose du canal cervical en C4-C4 et en C4-C5, d’origine dégénérative avec éperons osseux antérieur et postérieur en C3-C4 en hyposignal (grande flèche). Les espaces liquidiens périmédullaires sont effacés sur deux étages et la moelle est laminée. Il existe un hypersignal intramédullaire en regard de l’interligne C3-C4 témoignant d’une souffrance ischémique liée à la compression chronique de la moelle. A. T2 sagittal. B. T2 axial.Cette image IRM en deux plans illustre une myélopathie cervicarthrosique. L’image A correspond à une coupe sagittale médullaire, montrant une réduction marquée du canal rachidien cervical avec un aplatissement de la moelle épinière au niveau de plusieurs étages cervicaux, notamment à mi-hauteur. On y observe une hyperintensité intramédullaire en hypersignal T2, suggérant une souffrance médullaire chronique par compression. L’image B, en coupe axiale, met en évidence un rétrécissement concentrique du canal rachidien et un débord discal postérieur associé à une hypertrophie des articulations zygapophysaires. La flèche noire pointe une zone de compression directe de la moelle au centre du canal cervical. Cet aspect est typique des lésions dégénératives chroniques responsables de signes cliniques tels que troubles de la marche, paresthésies ou faiblesse des membres supérieurs.
3 92Hernie discale
Préférentiellement au niveau cervical.
Elle peut être une étiologie de compression médullaire extradurale (fig. 7.5).
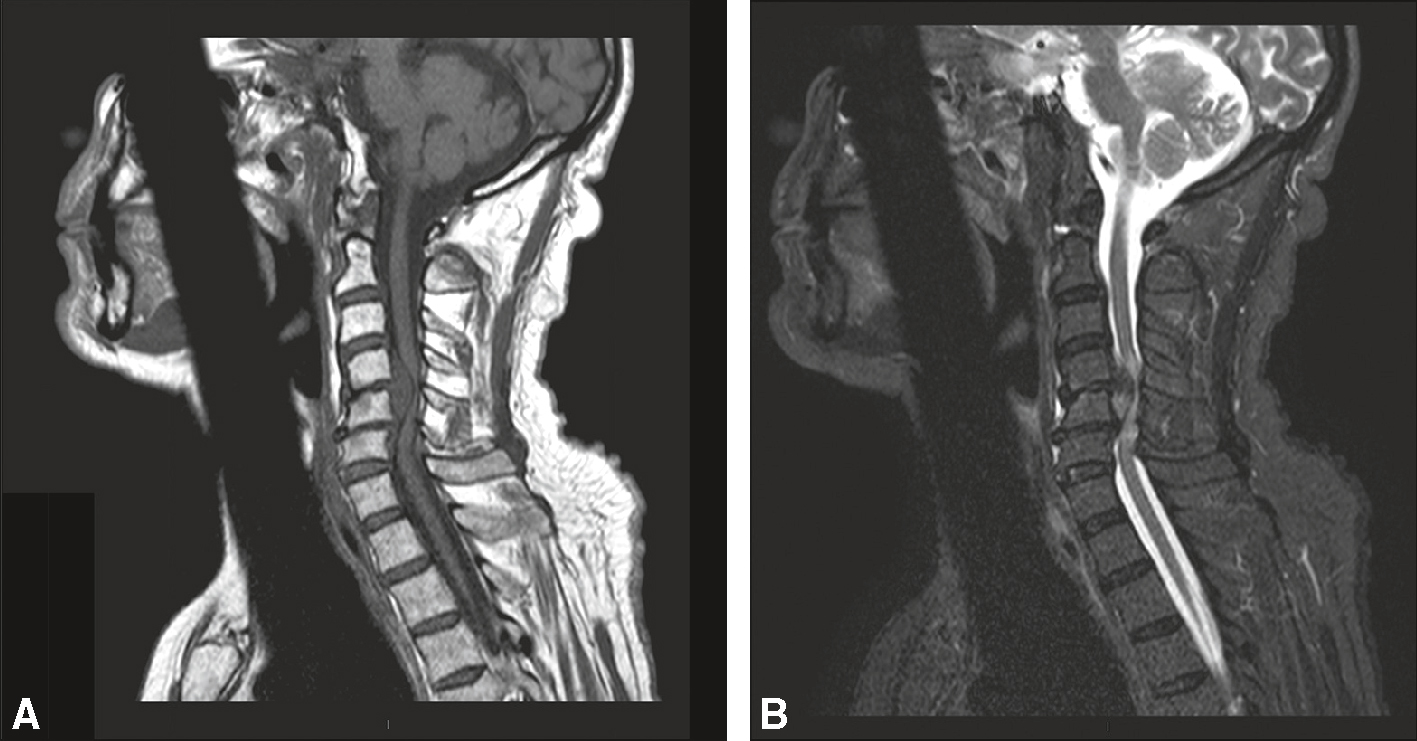
 Compression médullaire due à une hernie discale exclue en C5-C6.
Compression médullaire due à une hernie discale exclue en C5-C6. Les espaces liquidiens périmédullaires sont laminés. Compression médullaire avec hypersignal intramédullaire en regard témoignant d’une souffrance, en absence d’anomalie osseuse associée. A. Sagittal T1. B. Sagittal T2.
Image en coupes sagittales d’une IRM cervicale, présentée en deux volets A et B, montrant une compression médullaire au niveau C5-C6. La vue A, en pondération T1, met en évidence les structures anatomiques avec un bon contraste entre la moelle épinière, les disques intervertébraux et les corps vertébraux. La hernie discale postérieure en C5-C6 apparaît comme une protrusion du disque comprimant visiblement la moelle. La vue B, en pondération T2, accentue la visibilité des liquides, soulignant un hypersignal intramédullaire à ce niveau, évocateur d’un œdème ou d’une souffrance médullaire secondaire à la compression. La hernie discale exclue, bien visible par la perte de continuité avec le disque d’origine, s’insinue vers le canal rachidien, réduisant significativement l’espace périmédullaire. L’ensemble suggère une atteinte compressive aiguë ou subaiguë nécessitant une prise en charge rapide pour éviter les séquelles neurologiques. L’alignement vertébral est conservé, et aucun signe de fracture ou lésion osseuse n’est observé dans les coupes visibles.
4 93Spondylodiscites et épidurites infectieuses
À l’origine d’une compression médullaire extradurale (si bacille de Koch, il s’agit du mal de Pott) (fig. 7.6).
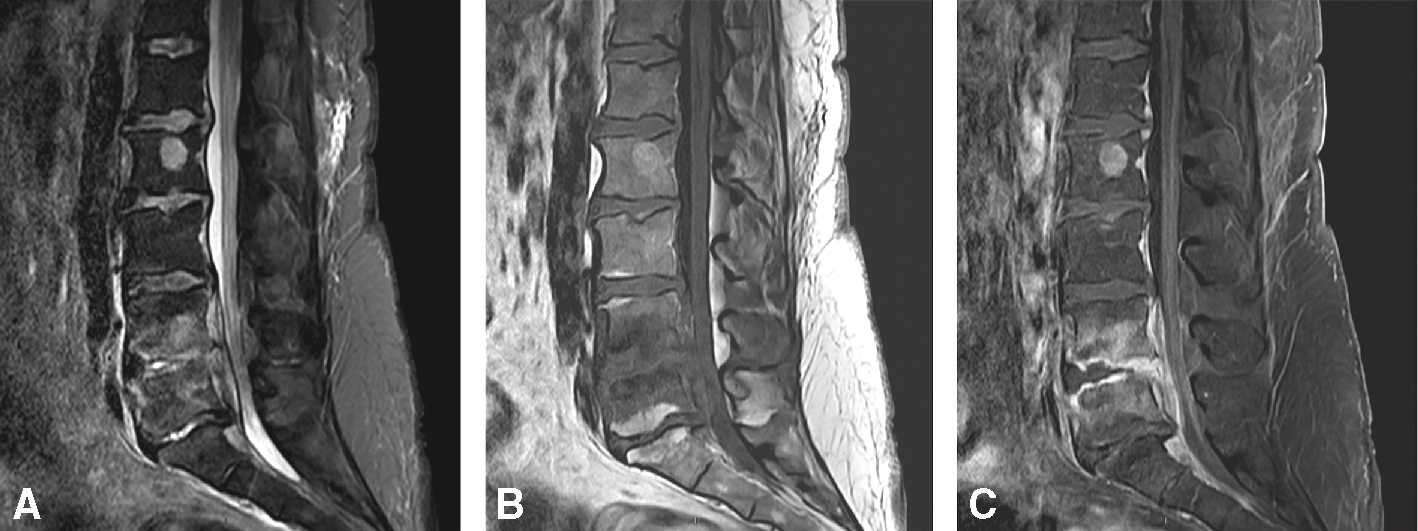
 Compression de la queue de cheval liée à une spondylodiscite infectieuse (ici à staphylocoques).
Compression de la queue de cheval liée à une spondylodiscite infectieuse (ici à staphylocoques). Hyposignal T1/hypersignal T2 des plateaux vertébraux en L4 et L5, en miroir, prenant le contraste après injection, avec spondylodiscite du disque et collection centimétrique intradiscale, atteignant l’espace épidural antérieur (épidurite comprimant la queue de cheval en regard). Intégrité des autres corps vertébraux (angiome vertébral bénin en L2). A. Sagittal T2.
 et C. Sagittal T1 sans puis avec injection de gadolinium FAT-SAT.
et C. Sagittal T1 sans puis avec injection de gadolinium FAT-SAT.Cette série d’IRM sagittales lombaires en pondérations T1, T2 et STIR (A, B, C) met en évidence une spondylodiscite infectieuse, probablement à staphylocoques. Sur l’image A, en séquence STIR, un hypersignal diffus est visible au niveau du disque intervertébral et des plateaux vertébraux adjacents, avec un œdème inflammatoire marqué. L’image B en T1 montre une perte du signal du disque et des corps vertébraux adjacents, traduisant une destruction osseuse et discale. Sur l’image C en T2, on observe une protrusion du matériel infecté dans le canal rachidien, entraînant une compression visible des racines de la queue de cheval. L’ensemble est caractéristique d’une spondylodiscite évoluée avec atteinte neurologique.
5 Hématome épidural
Lors d’un traitement avec anticoagulants ou après une ponction lombaire pouvant entraîner une compression médullaire.
B Causes intradurales extramédullaires
![]() Elles sont dominées par les tumeurs bénignes.
Elles sont dominées par les tumeurs bénignes.
1 Méningiomes
- •
 Femmes de plus de 50 ans avec compression médullaire lente typique s’exprimant par des troubles de la marche progressifs associés à un modeste syndrome lésionnel radiculaire.
Femmes de plus de 50 ans avec compression médullaire lente typique s’exprimant par des troubles de la marche progressifs associés à un modeste syndrome lésionnel radiculaire. - • Localisation tumorale thoracique dans les deux tiers des cas.
-
• L’IRM confirme la localisation intradurale extramédullaire habituellement postérieure avec une lésion à limite nette, de taille ovoïde, allongée selon le grand axe rachidien. L’implantation tumorale se fait sur la dure-mère (fig. 7.7).
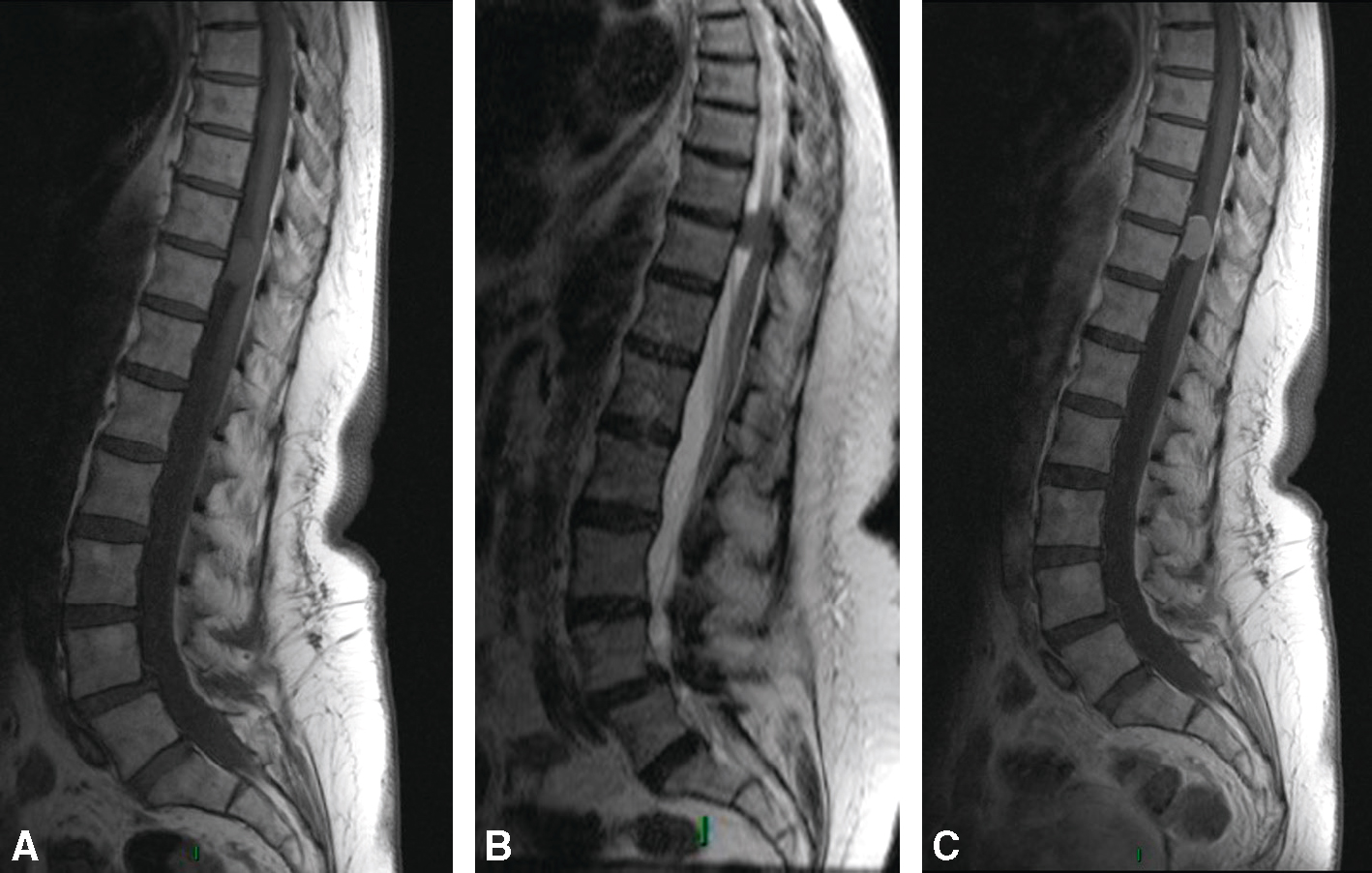
Fig. 7.7  Méningiome de niveau thoracique T10-T11.
Méningiome de niveau thoracique T10-T11.
Formation nodulaire en regard de T10-T11, épidurale antérieure, responsable d’une compression médullaire, le cordon médullaire étant refoulé et comprimé en arrière. A. En isosignal T1. B. Discret hypersignal STIR. C. Se rehaussant de façon intense et homogène avec épaississement méningé adjacent, en queue d’aronde.Cette série d’IRM sagittales thoraco-lombaires montre une lésion focale arrondie au niveau du canal rachidien, située en regard des vertèbres T10-T11. Sur l’image A (T1), la masse apparaît isointense par rapport à la moelle. Sur l’image B (T2), elle est légèrement hyperintense, bien délimitée, et refoule la moelle vers l’avant sans la détruire. L’image C (T1 avec injection de gadolinium) révèle une prise de contraste intense et homogène, caractéristique d’un méningiome intradurale extramédullaire. La moelle reste d’aspect conservé en dehors de l’effet de masse. Aucun signe de saignement, d’œdème périlésionnel ou d’atteinte osseuse adjacente n’est visible.
2 94Schwannomes
- • Ils concernent autant les hommes que les femmes de tout âge : localisation cervicale (un cas sur deux), thoracique (un cas sur quatre) et lombaire (un cas sur quatre).
- • Compression médullaire lente, mais avec un syndrome radiculaire marqué et des douleurs.
- • Radiographies rachidiennes : élargissement du trou de conjugaison.
-
• IRM : tumeur située sur une racine spinale, le plus souvent dorsale. Le neurinome apparaît en hypersignal en T2 (aspect d’un sablier) (fig. 7.8).
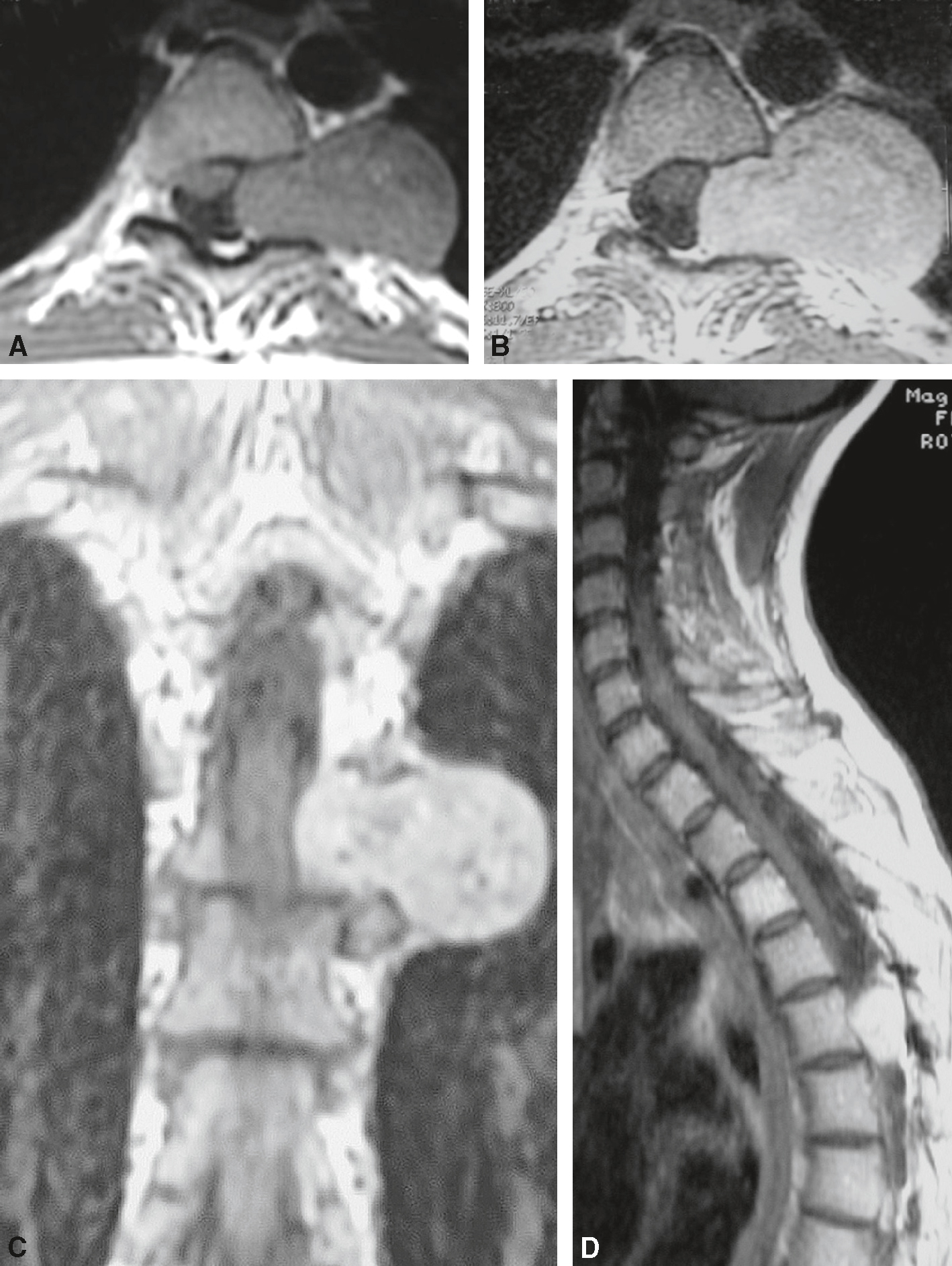
Fig. 7.8  Schwannome « en sablier » thoracique T5-T6 gauche.
Schwannome « en sablier » thoracique T5-T6 gauche.
Lésion extramédullaire extradurale, bien limitée, en forme de sablier, développée dans le foramen intervertébral T5-T6 gauche et étendue en dehors dans les espaces paravertébraux et en dedans dans le canal rachidien avec léger effet de masse sur la moelle. Le foramen est très élargi, témoignant du développement lent de la lésion. La lésion est en hyposignal T1, en hypersignal T2 et est rehaussée de manière homogène après injection. A. T1 axial. B. T1 axial après injection. C. T1 frontal après injection. D. T1 sagittal après injection.Les coupes axiales T1 et T2 (A et B) montrent une masse bien circonscrite s’étendant depuis le foramen intervertébral gauche en T5-T6. Elle présente un hyposignal modéré en T1 (A) et un hypersignal franc en T2 (B), sans signe de nécrose. L’image coronale (C) met en évidence la configuration en sablier, avec une extension intra- et extrarachidienne à travers le foramen, typique d’un schwannome foraminal. Sur la coupe sagittale (D), la masse refoule latéralement la moelle thoracique sans l’envahir, avec un effet de masse net mais sans œdème médullaire associé. Les contours sont réguliers, et l’aspect homogène après injection est en faveur d’une lésion bénigne d’origine nerveuse.
-
• Ils peuvent survenir dans le cadre d’une neurofibromatose de von Recklinghausen, surtout s’il en existe plusieurs, des signes cutanés (taches café au lait), des antécédents familiaux (fig. 7.9).
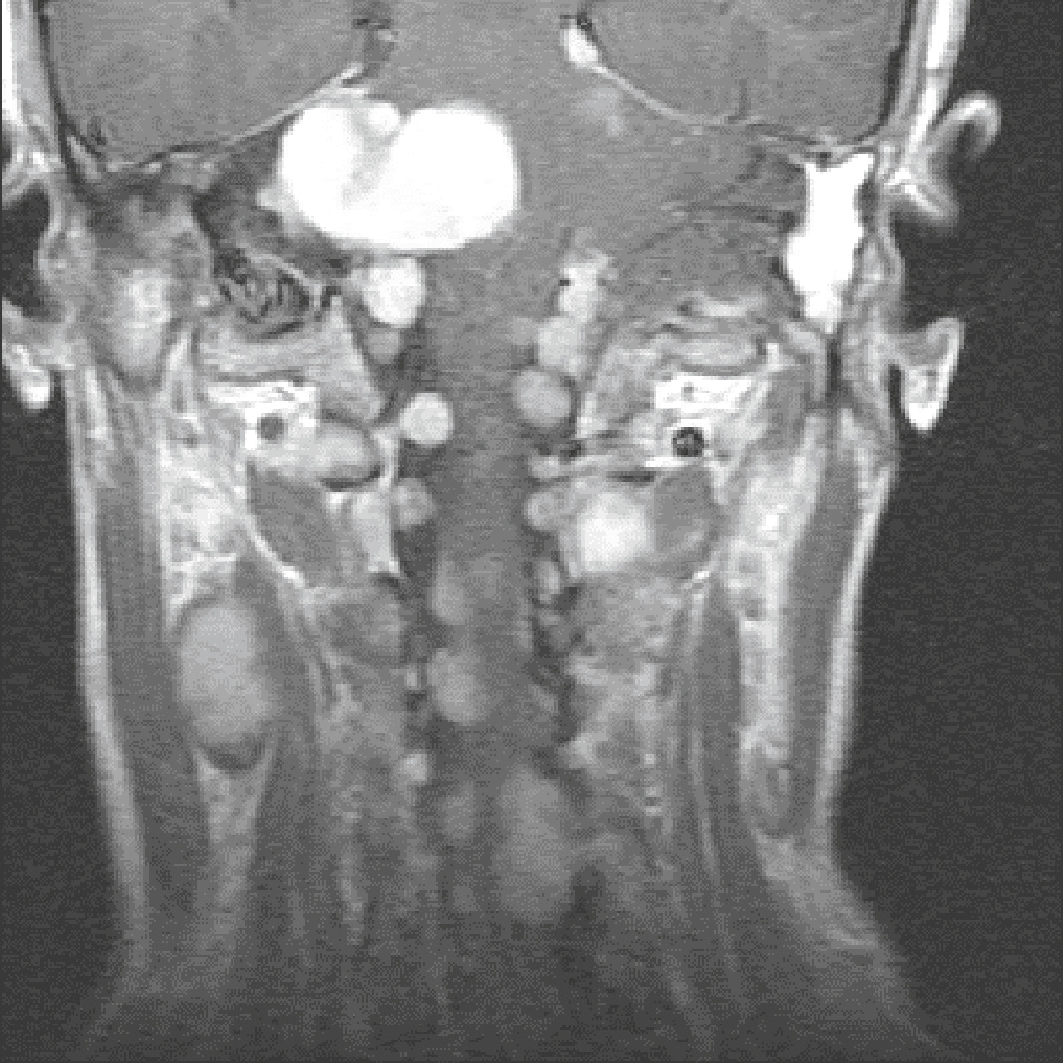
Fig. 7.9  Neurofibromes multiples responsables d’une compression médullaire dans le cadre d’une neurofibromatose de type 1 (NF1).
Neurofibromes multiples responsables d’une compression médullaire dans le cadre d’une neurofibromatose de type 1 (NF1).
La NF1, ou maladie de von Recklinghausen, est une affection autosomique dominante, à pénétrance clinique complète mais d’expression variable, de manifestation neurocutanée cliniquement hétérogène caractérisée par des taches café au lait, des nodules de Lish, des lentigos sur les aisselles et sur la région inguinale, et de multiples neurofibromes, liée à l’anomalie du gène suppresseur de tumeur NF1 (voir chapitre 26 – item 299).L’image montre une coupe coronale T1 avec injection de gadolinium centrée sur la région cervico-thoracique. On observe une multitude de lésions arrondies, bien circonscrites, réparties le long des nerfs rachidiens bilatéraux, dont certaines présentent un rehaussement intense après contraste. Ces nodules sont compatibles avec des neurofibromes plexiformes multiples. Plusieurs d’entre eux élargissent les foramens intervertébraux, notamment au niveau cervical moyen, avec un refoulement manifeste du contenu rachidien. L’effet de masse exercé sur la moelle cervicale est visible en position centrale, suggérant une compression médullaire d’origine extracanalaire. Ce tableau est typique d’une neurofibromatose de type 1 avec complications neurologiques.
3 9596Arachnoïdites
- • Réaction inflammatoire des leptoméninges engainant la moelle spinale.
- • Suites de méningite, de traumatisme ou de maladies inflammatoires (sarcoïdose).
C Causes intramédullaires
1 Tumeurs
Les causes intramédullaires sont dominées par les tumeurs qui, dans les deux tiers des cas, sont soit :
-
• des épendymomes (fig. 7.10);

Fig. 7.10  Épendymome cervical en regard de C4-C5.
Épendymome cervical en regard de C4-C5.
Masse tissulaire intramédullaire centrée sur la moelle spinale cervicale en regard de C4-C5, avec une part charnue en hypersignal T2, associée à une formation kystique adjacente, avec prise de contraste.Cette IRM cervicale en coupes sagittales montre une masse intramédullaire centrée au niveau C4-C5. Sur l’image de gauche (T2), la lésion apparaît hyperintense, bien délimitée, avec un discret élargissement de la moelle et un œdème périphérique crânialement. L’image de droite (T1 avec injection de gadolinium) montre une prise de contraste homogène, caractéristique d’un épendymome. Le canal rachidien reste élargi, sans signe d’infiltration des structures extramédullaires. L’aspect est typique d’une tumeur gliale bénigne de la moelle épinière cervicale, généralement lente à évoluer mais compressive en cas d’extension.
-
• des astrocytomes (fig. 7.11).

Fig. 7.11  Astrocytome de la moelle spinale.
Astrocytome de la moelle spinale.
Volumineux processus expansif du cône terminal étendu de T8 à L1, en hyposignal T1 et T2, avec quelques prises de contraste nodulaires au sein de la lésion après injection. Pas de prise de contraste radiculaire; intégrité des corps vertébraux. A. Sagittal T2. et C. Sagittal T1 sans puis après injection de gadolinium.
et C. Sagittal T1 sans puis après injection de gadolinium.Les coupes sagittales thoraciques en pondérations T2 (A), T1 sans injection (B) et T1 avec gadolinium (C) révèlent une lésion intramédullaire allongée, étendue sur plusieurs étages thoraciques moyens. En T2, on observe un hypersignal diffus avec une expansion de la moelle, traduisant une infiltration tumorale. En T1, la moelle apparaît élargie, avec un signal iso- à hypointense. Après injection (C), la prise de contraste est discrète, hétérogène et peu marquée, ce qui oriente vers un astrocytome, tumeur gliale souvent infiltrante, non encapsulée. L’absence de nécrose centrale ou de rehaussement net différencie cet aspect de celui d’un épendymome.
2 Malformations vasculaires (cavernome, angiome, fistule artérioveineuse durale périmédullaire)
-
• Compression médullaire lente ou hyperpression veineuse (fistule) (fig. 7.12), avec un risque hémorragique et ischémique potentiel.
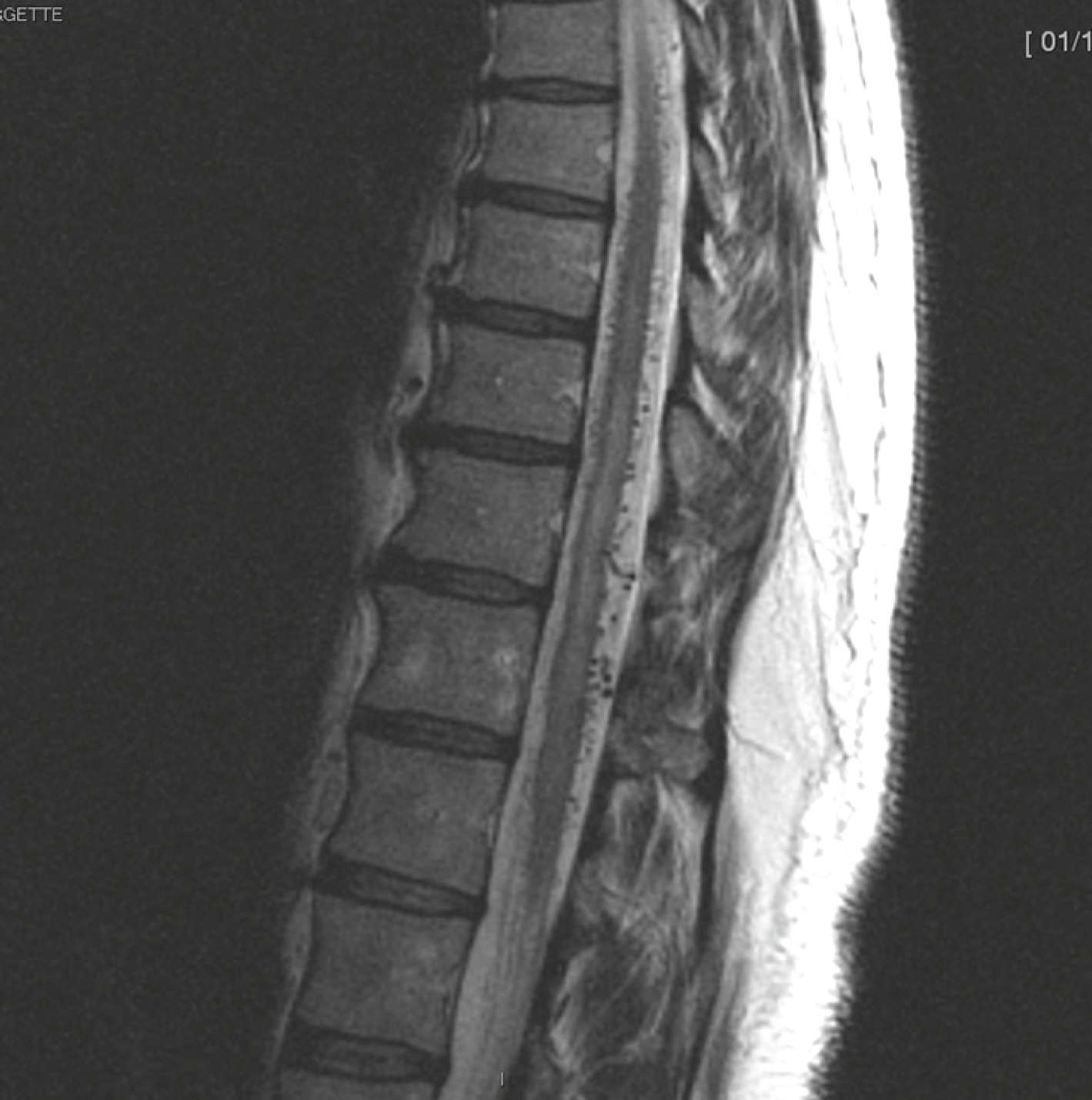
Fig. 7.12  Fistule durale médullaire.
Fistule durale médullaire.
Patient présentant un déficit des membres inférieurs avec des troubles sphinctériens d’apparition progressive. Coupe sagittale T2. Aspect de fistule durale avec un hypersignal T2 suspendu intramédullaire objectivant la souffrance médullaire chronique et le lacis vasculaire périlésionnel évoquant le drainage veineux périmédullaire.Sur cette coupe sagittale T2 de la moelle thoracique, on observe un hypersignal intramédullaire longitudinal s’étendant sur plusieurs étages, traduisant une congestion veineuse chronique. La moelle est légèrement épaissie, et l’aspect en « cordon gonflé » est typique. En arrière du cordon médullaire, on distingue de fins vaisseaux serpigineux en hyposignal, caractéristiques de la présence de veines périmédullaires dilatées. Cet aspect est hautement suggestif d’une fistule durale, pathologie vasculaire dans laquelle une communication anormale entre une artère radiculaire et le système veineux périmédullaire entraîne une hypertension veineuse et une myélopathie progressive.
- • L’IRM et, parfois, l’artériographie médullaire (fistule, angiome) visualisent la malformation vasculaire, en établissent le type précis et orientent ainsi la stratégie thérapeutique.
3 9798Syringomyélie
-
• Il s’agit d’une cavité intramédullaire (fig. 7.13).

Fig. 7.13  Syringomyélie.
Syringomyélie.Sur ces coupes sagittales thoraciques en pondération T2 (A) et T1 (B), on observe une cavité intramédullaire longitudinale bien délimitée, centrée sur la moelle épinière dorsale. Sur l’image T2 (A), la cavité apparaît en hypersignal, sans rehaussement périphérique ni signe d’œdème associé, traduisant une lésion liquidienne compatible avec une syrinx. Sur l’image T1 (B), cette même cavité est en hyposignal, confirmant la nature liquidienne pure. La moelle est élargie à ce niveau, mais les contours restent réguliers sans effet de masse extramédullaire. L’ensemble est évocateur d’une syringomyélie isolée, possiblement secondaire à une malformation de Chiari ou à un traumatisme spinal antérieur.
-
• Douleurs (névralgie cervicobrachiale, épaule et bras, à type d’étau ou de brûlures), syndrome suspendu – c’est-à-dire ne touchant qu’une fraction des métamères – au niveau des membres supérieurs le plus souvent avec déficit moteur, amyotrophie, aréflexie, hypoesthésie dissociée purement thermoalgique (fig. 7.14) suspendue, scoliose dans un tiers des cas.
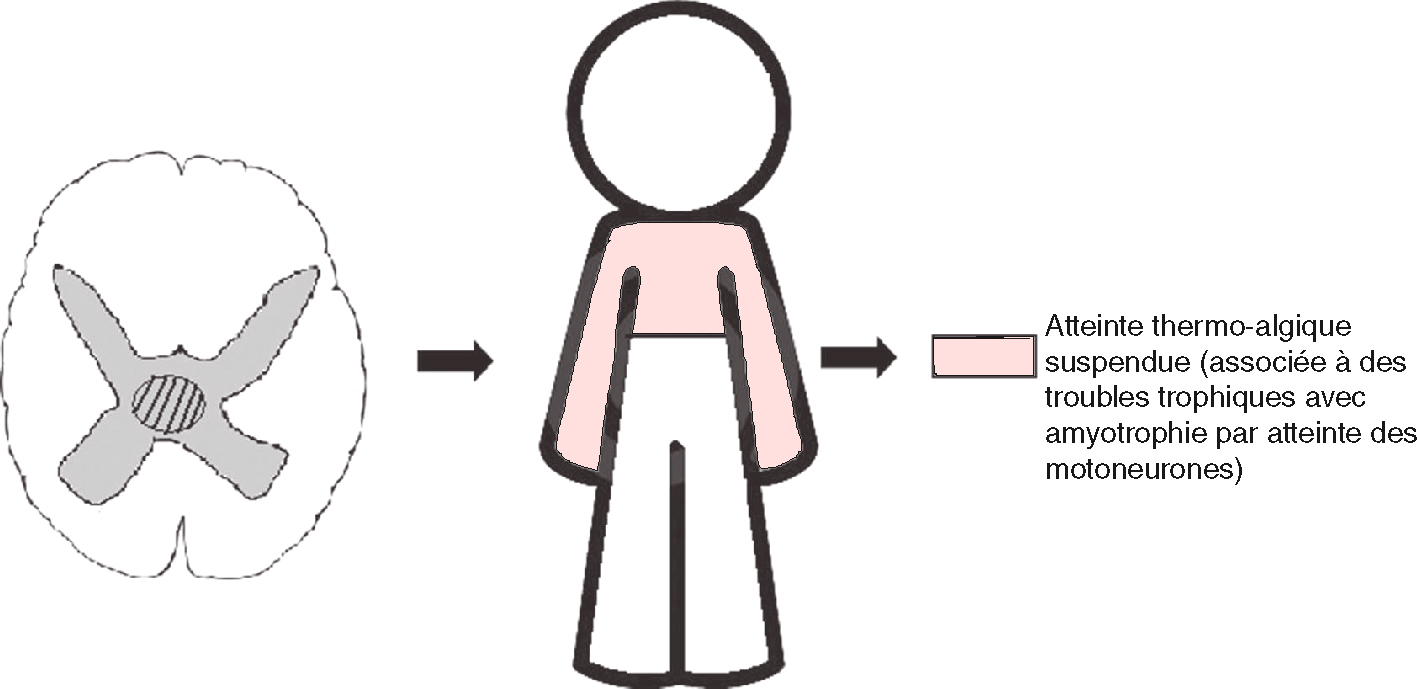
Fig. 7.14  Syringomyélie.
Syringomyélie.
Hypoesthésie « en cape » révélée par des blessures indolores à répétition. Cavitation filiforme intramédullaire, étendue de C6 à L1, dont le volume apparaît plus important en thoracique bas (avec quelques haustrations au niveau dorsal). La formation kystique apparaît centrée sur le canal épendymaire. Le cône médullaire est en place. Pas d’anomalie discovertébrale notable. A. Sagittal T2. B. Axial T2.Ce schéma illustre de manière simplifiée le déficit sensoriel typique observé dans la syringomyélie. À gauche, une section transversale de moelle montre une cavité centromédullaire, représentée en noir, localisée dans la commissure grise. Cette localisation entraîne une interruption des fibres croisées thermoalgiques. À droite, une silhouette humaine met en évidence une atteinte suspendue en rose, c’est-à-dire limitée aux dermatomes cervicaux et thoraciques supérieurs, épargnant les extrémités. Cette zone est le siège d’une perte thermo-algésique bilatérale, souvent associée à une amyotrophie segmentaire par atteinte des motoneurones. L’ensemble traduit un syndrome dissocié caractéristique.
- • L’IRM met en évidence la cavité centromédullaire pouvant remonter jusqu’à la moelle allongée (bulbe).
- • Il peut s’y associer une malformation d’Arnold-Chiari (les amygdales cérébelleuses s’engagent dans le trou occipital) ou un aspect d’arachnoïdite séquellaire d’infection ou d’hémorragie méningée.
- • Les cavités syringomyéliques peuvent survenir également dans les suites d’un traumatisme.
V 99Diagnostic différentiel
Tout tableau clinique compatible avec une souffrance médullaire nécessite une IRM pour détecter une compression médullaire lente curable dans un délai rapide, car le patient reste en permanence exposé à un risque d’accident médullaire aigu, même sur un processus d’évolution lente.
Des diagnostics trompeurs peuvent simuler la compression médullaire :
- • devant l’installation subaiguë d’une paraparésie ou paralysie flasque avec aréflexie ostéo-tendineuse des membres associée à des troubles sensitifs mais sans trouble sphinctérien, une polyradiculonévrite aiguë peut être évoquée;
- • l’apparition d’une paraparésie spastique progressive avec d’autres signes de souffrance médullaire associés peut être le premier signe d’une sclérose en plaques, surtout de forme chronique progressive d’emblée, qui nécessitera la réalisation, en plus de l’IRM médullaire, d’une IRM encéphalique et d’une ponction lombaire;
- • 100la sclérose latérale amyotrophique peut simuler une compression médullaire, mais les signes sensitifs et sphinctériens sont absents. Il existe de plus des fasciculations et une amyotrophie;
- • la sclérose combinée de la moelle spinale s’observe au cours de la maladie de Biermer. Le diagnostic est biologique : macrocytose et déficit en vitamine B12.
VI Principes de la prise en charge
![]() La compression médullaire constitue toujours une urgence diagnostique (IRM) et thérapeutique, car le tableau peut s’aggraver en quelques heures, aboutissant à une paraplégie/tétraplégie complète et définitive. Il peut s’agir d’une urgence neurochirurgicale.
La compression médullaire constitue toujours une urgence diagnostique (IRM) et thérapeutique, car le tableau peut s’aggraver en quelques heures, aboutissant à une paraplégie/tétraplégie complète et définitive. Il peut s’agir d’une urgence neurochirurgicale.
Selon l’étiologie, il peut être nécessaire de recourir à une décompression chirurgicale en urgence (laminectomie décompressive, chirurgie d’exérèse, tumorectomie, etc.), plus ou moins associée à une prise en charge complémentaire spécifique (corticothérapie, radiothérapie, antibio-thérapie, etc.). Des mesures thérapeutiques associées sont souvent nécessaires (prévention des facteurs d’aggravation notamment immobilisation si instabilité, prévention des complications du décubitus, cathétérisme vésical, etc.).
![]() Les conséquences à long terme d’une compression médullaire peuvent nécessiter une prise en charge du déficit sensitivo-moteur et des séquelles spastiques (molécules antispastiques, rééducation fonctionnelle, cathétérisme vésical, etc.).
Les conséquences à long terme d’une compression médullaire peuvent nécessiter une prise en charge du déficit sensitivo-moteur et des séquelles spastiques (molécules antispastiques, rééducation fonctionnelle, cathétérisme vésical, etc.).
Syndrome de la queue de cheval
- I 101Rappels anatomiques
- II Clinique
- III Examens complémentaires
- IV Étiologie
- V Diagnostic différentiel
- VI Principes de la prise en charge
I Rappels anatomiques
Le syndrome de la queue de cheval correspond à la souffrance des racines de la queue de cheval en dessous du cône terminal de la moelle spinale, entre les corps vertébraux de L2 et le sacrum. Il constitue un syndrome neurogène périphérique pluriradiculaire s’exprimant par des signes au niveau des membres inférieurs et du périnée, dominé par l’importance des troubles sphinctériens.
II Clinique
Le diagnostic est clinique, correspondant à une atteinte pluriradiculaire lombosacrée.
A Troubles sensitifs
Douleurs fréquentes à type de radiculalgie (cruralgie, sciatalgie) ou de douleurs pluriradicu-laires d’un ou des deux membres inférieurs. Des douleurs sacrées périnéales et génitales sont souvent associées, favorisées par les efforts à glotte fermée (toux, défécation). Des paresthé-sies ou anesthésies dans les membres inférieurs sont fréquentes, de topographie radiculaire L2 à S1. Une hypoesthésie périnéale, des organes génitaux externes et de l’anus est retrouvée, constituant une anesthésie en selle.
B Troubles moteurs
Ils sont de topographie monoradiculaire ou pluriradiculaire uni- ou bilatérale, le plus souvent asymétriques. Le déficit moteur peut se résumer à une impossibilité de marcher sur les pointes (atteinte de la racine S1) ou sur les talons (L5) ou à une impossibilité d’étendre la jambe sur la cuisse (L3, L4) ou de fléchir la cuisse sur le bassin (L1, L2). À l’extrême, l’atteinte motrice peut aboutir à une paraplégie flasque avec amyotrophie.
C Réflexes
L’abolition d’un ou plusieurs réflexes tendineux aux membres inférieurs est habituellement constatée; les réflexes périnéaux, anaux, bulbocaverneux, clitorido-anaux sont abolis.
D 102Troubles génitosphinctériens
Ils apparaissent précocement : retard à la miction ou nécessité de pousser pour uriner (dysu-rie) à laquelle s’associe une pollakiurie en rapport avec une vidange de vessie incomplète. Habituellement, ces troubles sphinctériens sont accompagnés d’une insensibilité du passage urinaire. Sur le plan anal, la constipation est plus fréquente que l’incontinence fécale. Sur le plan génital, il existe une impuissance ou une anesthésie vaginale.
III Examens complémentaires
![]() L’IRM est l’examen de choix pour visualiser la compression de la queue de cheval. Le myé-loscanner peut jouer un rôle diagnostique en cas de contre-indication à l’IRM.
L’IRM est l’examen de choix pour visualiser la compression de la queue de cheval. Le myé-loscanner peut jouer un rôle diagnostique en cas de contre-indication à l’IRM.
L’électromyogramme mettra en évidence des signes neurogènes dans le territoire de la queue de cheval.
IV Étiologie
-
•
 Les hernies discales et les épendymomes représentent les causes les plus fréquentes d’un syndrome de la queue de cheval :
Les hernies discales et les épendymomes représentent les causes les plus fréquentes d’un syndrome de la queue de cheval :- – les hernies discales s’expriment habituellement par un début brutal douloureux, déclenché par un effort faisant suite à des épisodes lombosciatalgiques; l’IRM révèle une hernie exclue, latérale ou médiane, pouvant être associée à des lésions arthrosiques;
- – les épendymomes du filum terminal sont d’évolution plus lente, mais peuvent s’accompagner d’hémorragies méningées brutales s’exprimant par une violente douleur lombaire.
- • Les neurinomes, les méningiomes, les métastases, les processus infectieux sont plus rares.
- • Le syndrome du canal lombaire étroit peut être congénital ou acquis avec des hernies discales étagées ou arthrose visualisée à l’IRM. Il s’exprime par une claudication radiculaire intermittente douloureuse, progressive à l’effort, cédant à l’arrêt de celui-ci. Il s’y associe des pares-thésies et des troubles sphinctériens pouvant aboutir à un syndrome de la queue de cheval.
V Diagnostic différentiel
- •
 Il est constitué par l’atteinte du cône terminal de la moelle spinale, qui aboutit à une sémiologie assez proche, mais complétée d’un signe de Babinski (souvent retardé), d’une abolition des réflexes abdominaux inférieurs et de troubles sensitifs remontant jusqu’à un niveau T12-L1. Les réflexes tendineux ne sont pas abolis (et peuvent devenir, hors contexte aigu, pyramidaux).
Il est constitué par l’atteinte du cône terminal de la moelle spinale, qui aboutit à une sémiologie assez proche, mais complétée d’un signe de Babinski (souvent retardé), d’une abolition des réflexes abdominaux inférieurs et de troubles sensitifs remontant jusqu’à un niveau T12-L1. Les réflexes tendineux ne sont pas abolis (et peuvent devenir, hors contexte aigu, pyramidaux). - • 103Les polyradiculonévrites aiguës ne présentent habituellement pas de troubles sphinctériens.
- • Les syndromes plexiques lombaires par envahissement néoplasique sont visualisés par l’imagerie pelvienne.
VI Principes de la prise en charge
Il s’agit d’une urgence neurochirurgicale et sa reconnaissance impose une IRM en urgence et une prise en charge neurochirurgicale immédiate. Le pronostic fonctionnel, et surtout celui des troubles sphinctériens, dépend étroitement de la durée et de l’intensité de la compression des racines lombosacrées.
Le traitement est chirurgical : son objectif est de décomprimer les racines lombosacrées par une laminectomie lombaire avec exérèse de la lésion compressive.
Des mesures thérapeutiques associées sont souvent nécessaires (prévention des complications du décubitus, cathétérisme vésical, etc.).
