Situations de départ
Symptômes et signes cliniques
 12 Nausées.
12 Nausées.
 13 Vomissements.
13 Vomissements.
 28 Coma et troubles de conscience.
28 Coma et troubles de conscience.
 50 Malaise/perte de connaissance.
50 Malaise/perte de connaissance.
 118 Céphalée.
118 Céphalée.
 119 Confusion mentale/désorientation.
119 Confusion mentale/désorientation.
 120 Convulsions.
120 Convulsions.
 121 Déficit neurologique sensitif et/ou moteur.
121 Déficit neurologique sensitif et/ou moteur.
 126 Mouvements anormaux.
126 Mouvements anormaux.
 134 Troubles du langage et/ou phonation.
134 Troubles du langage et/ou phonation.
 138 Anomalie de la vision.
138 Anomalie de la vision.
 143 Diplopie.
143 Diplopie.
 183 Analyse du liquide cérébrospinal (LCS).
183 Analyse du liquide cérébrospinal (LCS).
 226 Découverte d’une anomalie du cerveau à l’examen d’imagerie médicale.
226 Découverte d’une anomalie du cerveau à l’examen d’imagerie médicale.
 231 Demande d’un examen d’imagerie.
231 Demande d’un examen d’imagerie.
Prise en charge aiguë et chronique
 250 Prescrire des antalgiques.
250 Prescrire des antalgiques.
 259 Évaluation et prise en charge de la douleur aiguë.
259 Évaluation et prise en charge de la douleur aiguë.
Situations diverses
 345 Situation de handicap.
345 Situation de handicap.
 352 Expliquer un traitement au patient (adulte/enfant/adolescent).
352 Expliquer un traitement au patient (adulte/enfant/adolescent).
Objectifs pédagogiques
 Diagnostiquer une hémorragie méningée.
Diagnostiquer une hémorragie méningée.
 Identifier les situations d’urgence et planifier leur prise en charge.
Identifier les situations d’urgence et planifier leur prise en charge.
Hiérarchisation des connaissances
| Rang | Rubrique | Intitulé | Descriptif |
|---|---|---|---|
| Définition | Définition de l”hémorragle méningée dite sous-arachnoïdienne, spontanée et traumatique | ||
| Étiologies | Connaître les principales causes d’hémorragie méningée et les facteurs favorisants | ||
| Diagnostic positif | Connaître les présentations cliniques et le diagnostic d’hémorragie méningée | Évoquer le diagnostic devant une céphalée évocatrice chez un patient sans autre argument pour une cause de céphalée urgente avec signes d’irritation pyramidale | |
| Diagnostic positif | Connaître la stratégie d’exploration complémentaire devant un tableau clinique évocateur d’hémorragie méningée | Indication = scanner cérébral sans injection en urgence. Reconnaître la présence de sang dans les espaces sous-arachnoïdiens sur un scanner PUIS ponction lombaire (savoir quand et comment réaliser une ponction lombaire. Connaître les caractéristiques du LCS en cas d’hémorragie méningée) | |
| Examens complémentaires | Connaître les signes évocateurs d’hémorragies méningées au scanner cérébral sans injection | ||
| Examens complémentaires | Connaître les caractéristiques du liquide céphalorachidien dans l’hémorragie méningée | ||
| Contenu multimédia | Exemple d’HSA sur TDM |
1. Hémorragie sous-arachnoïdienne;
|
|
| Examens complémentaires | Connaître la stratégie d’exploration complémentaire à visée étiologique | Indication = scanner cérébral avec injection. Reconnaître un anévrisme artériel (= image d’addition artérielle) ou une autre origine vasculaire | |
| Identifier une urgence | Connaître l’urgence d’une hémorragie méningée | Identifier l’urgence diagnostic et la nécessité de référer en urgence à un service spécialisé : neurochirurgie, neuroradiologie interventionnelle | |
| Prise en charge | Connaître le traitement symptomatique initial | Savoir prévenir les complications avec un isolement neurosensoriel au lit, antalgique IV, contrôle de la pression artérielle et appel d’un réanimateur | |
| Prise en charge | Connaître les principes du traitement étiologique | Connaître les grands principes du traitement étiologiques (neurochirurgical et neuro-radio-interventionnel) | |
| Suivi et/ou pronostic | Connaître les complications évolutives d’une hémorragie méningée | Hypertension intracrânienne, hydrocéphalie aiguë précoce et retardée, récidive hémorragique, vasospasme cérébral |

I 550Pour comprendre
- •
 L’hémorragie méningée, ou hémorragie sous-arachnoïdienne (HSA) non traumatique, est définie par l’irruption de sang artériel dans les espaces sous-arachnoïdiens.
L’hémorragie méningée, ou hémorragie sous-arachnoïdienne (HSA) non traumatique, est définie par l’irruption de sang artériel dans les espaces sous-arachnoïdiens. - • L’anévrisme cérébral rompu en est la cause la plus fréquente et représente environ 85 % des HSA.
- • Les HSA anévrismales représentent environ 5 % des accidents vasculaires cérébraux.
- • L’HSA est une urgence diagnostique et thérapeutique qui impose une admission immédiate en milieu spécialisé et pluridisciplinaire pour une prise en charge diagnostique et thérapeutique optimale.
II 551Diagnostiquer une hémorragie méningée
A Symptômes et signes cliniques d’une hémorragie sous-arachnoïdienne
1 Céphalées
- • Il s’agit de céphalées « explosives », d’emblée maximales.
- •
 Des vomissements en jet ou des nausées, une photophobie et une phonophobie peuvent être associés, mais sont inconstants.
Des vomissements en jet ou des nausées, une photophobie et une phonophobie peuvent être associés, mais sont inconstants.
2 Signes neurologiques
- •
 Raideur méningée.
Raideur méningée. - • Signes pyramidaux, paralysie du VI : ils n’ont pas de valeur localisatrice.
-
• Troubles de la vigilance :
- –
 coma d’emblée ou mort subite par inondation massive des espaces sous-arachnoïdiens peuvent survenir;
coma d’emblée ou mort subite par inondation massive des espaces sous-arachnoïdiens peuvent survenir; - – syndrome confusionnel d’installation aiguë;
- – crise épileptique généralisée.
- –
-
• Anomalies du fond d’œil :
- – hémorragies rétiniennes ou vitréennes (syndrome de Terson) qui peuvent être responsables d’une baisse d’acuité visuelle uni- ou bilatérale;
- – œdème papillaire lié à une augmentation brutale de la pression intracrânienne.
- •
 Paralysie du III intrinsèque et extrinsèque (mécanisme compressif par un anévrisme de l’artère carotide interne intracrânienne).
Paralysie du III intrinsèque et extrinsèque (mécanisme compressif par un anévrisme de l’artère carotide interne intracrânienne). -
• Les autres signes de localisation témoignent d’un hématome intraparenchymateux associé. Par exemple :
- – une hémiparésie, une hémianopsie, une aphasie en cas d’hématome temporal (touchant l’hémisphère dominant) compliquant un anévrisme de l’artère cérébrale moyenne;
- – une paraparésie, un mutisme, un syndrome frontal en cas d’hématome fronto-basal compliquant un anévrisme de l’artère communicante antérieure ou de l’artère péricalleuse.
3 Signes extraneurologiques
Signes végétatifs :
- •
 bradycardie ou tachycardie;
bradycardie ou tachycardie; - • choc avec œdème pulmonaire et insuffisance cardiaque aiguë (consécutif à l’orage caté-cholaminergique provoqué par l’HSA);
- • modifications de la repolarisation à l’ECG;
- • instabilité tensionnelle (hypertension artérielle sévère consécutive à l’hypertension intracrânienne);
- • hyperthermie retardée (38–38,5 °C).
B Explorations complémentaires à visée diagnostique
![]() L’imagerie cérébrale est indispensable pour :
L’imagerie cérébrale est indispensable pour :
- • faire le diagnostic d’HSA (une imagerie cérébrale normale n’élimine pas le diagnostic d’HSA);
- • établir le diagnostic étiologique de la cause sous-jacente (anévrisme le plus souvent).
1 552Scanner cérébral
-
•
 Affirme le diagnostic lorsqu’il montre une hyperdensité spontanée dans les espaces sous-arachnoïdiens : citernes de la base, vallées sylviennes et scissure interhémisphérique essentiellement (fig. 29.1). Les anévrismes étant situés à la base du cerveau, les HSA corticales doivent faire évoquer une étiologie autre qu’anévrismale (syndrome de vasoconstriction cérébrale réversible, thrombose veineuse cérébrale…).
Affirme le diagnostic lorsqu’il montre une hyperdensité spontanée dans les espaces sous-arachnoïdiens : citernes de la base, vallées sylviennes et scissure interhémisphérique essentiellement (fig. 29.1). Les anévrismes étant situés à la base du cerveau, les HSA corticales doivent faire évoquer une étiologie autre qu’anévrismale (syndrome de vasoconstriction cérébrale réversible, thrombose veineuse cérébrale…).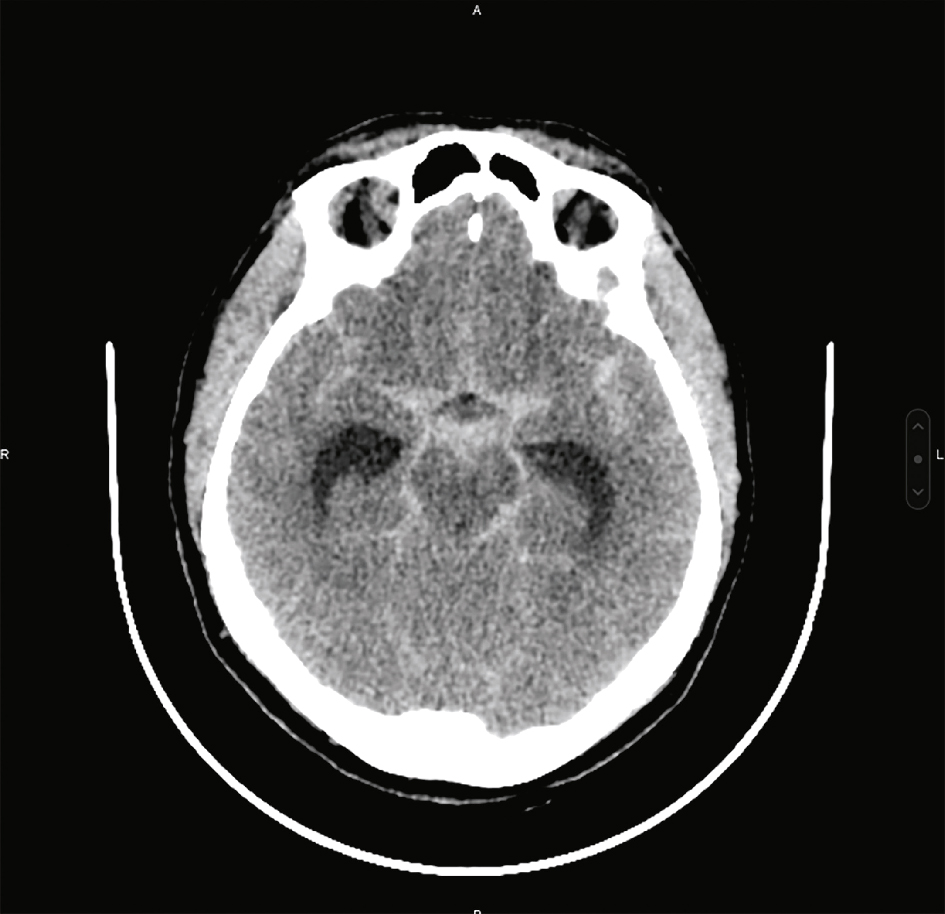
Fig. 29.1  Scanner cérébral sans injection (coupe axiale) montrant une hyperdensité spontanée des citernes de la base, des deux vallées sylviennes.
Scanner cérébral sans injection (coupe axiale) montrant une hyperdensité spontanée des citernes de la base, des deux vallées sylviennes.Image de scanner cérébral en coupe axiale, réalisée sans injection de produit de contraste, révélant une hyperdensité spontanée localisée dans les citernes de la base ainsi que dans les deux vallées sylviennes. Cette hyperdensité, visible sous forme de zones blanches au sein des espaces sous-arachnoïdiens, évoque fortement la présence de sang, suggérant une hémorragie méningée aiguë, très probablement d’origine anévrismale. La symétrie des structures cérébrales profondes est globalement respectée, mais la densité accrue dans ces régions clés impose une prise en charge rapide, car elle témoigne d’un saignement actif dans les espaces cérébro-méningés.
-
•
 Recherche des complications précoces :
Recherche des complications précoces : - – hématome intraparenchymateux associé;
- – hémorragie intraventriculaire;
- – ischémie cérébrale;
- – hydrocéphalie aiguë;
- – œdème cérébral.
2 IRM cérébrale
- •
 A une sensibilité comparable au scanner dans les premières 24 heures pour faire le diagnostic.
A une sensibilité comparable au scanner dans les premières 24 heures pour faire le diagnostic. -
• A meilleure une sensibilité que le scanner dans les jours qui suivent l’HSA avec les séquences FLAIR et T2* (fig. 29.2).
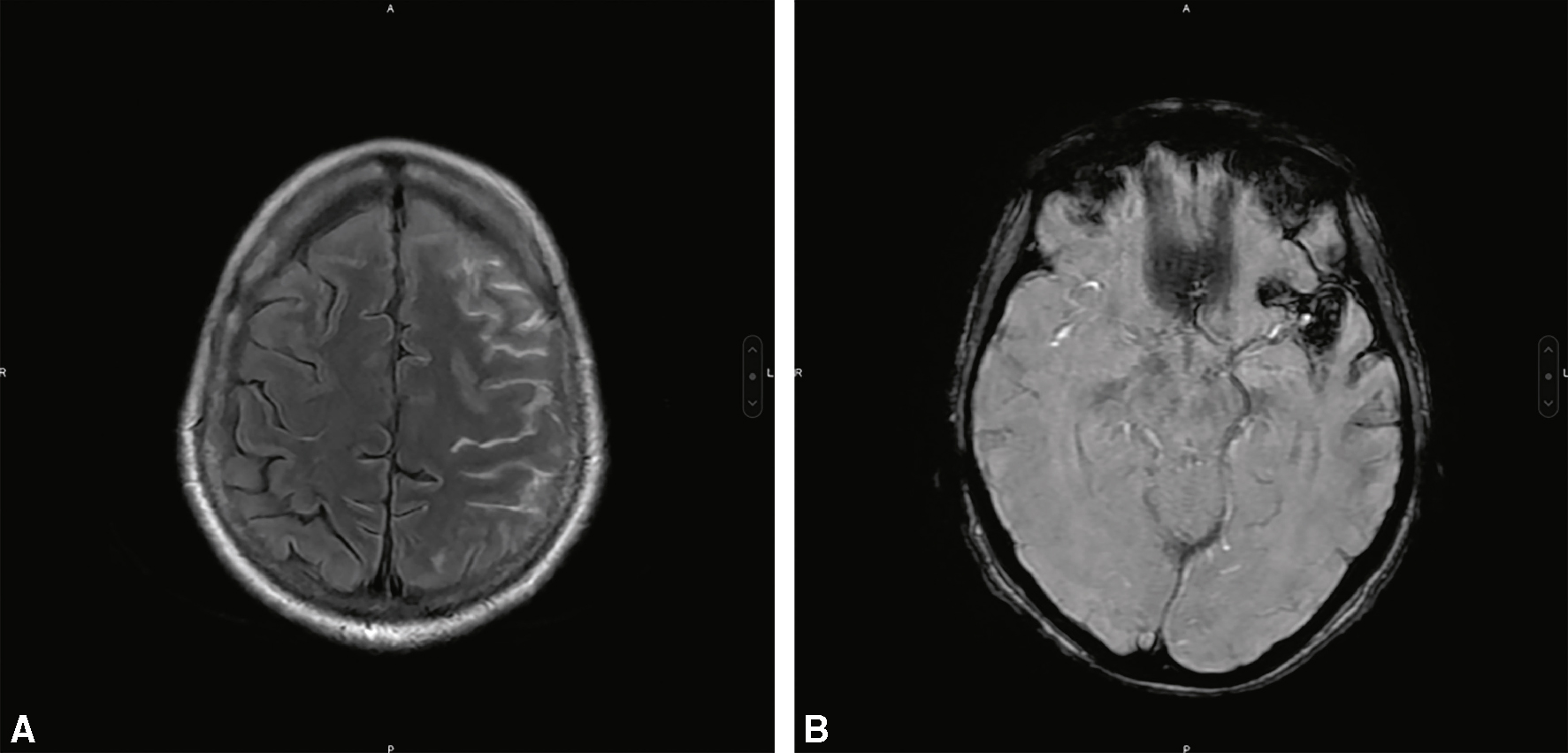
Fig. 29.2  IRM cérébrale montrant une HSA corticale frontale gauche (A : coupe axiale, séquence FLAIR) et de la vallée sylvienne gauche (B : coupe axiale, séquence de susceptibilité magnétique).
IRM cérébrale montrant une HSA corticale frontale gauche (A : coupe axiale, séquence FLAIR) et de la vallée sylvienne gauche (B : coupe axiale, séquence de susceptibilité magnétique).Ces deux coupes axiales d’IRM cérébrale illustrent une hémorragie sous-arachnoïdienne (HSA) localisée à la convexité. L’image A, en séquence FLAIR, montre un hypersignal diffus au niveau des sillons frontaux gauches, indiquant la présence de sang dans l’espace sous-arachnoïdien cortical. L’image B, obtenue en séquence de susceptibilité magnétique (SWI), révèle plusieurs foyers d’hypo-intensité dans la vallée sylvienne gauche, caractéristiques de dépôts hématiques. L’aspect combiné sur les deux séquences confirme une HSA corticale gauche, probablement d’origine veineuse ou traumatique, en dehors du contexte habituel de rupture anévrismale. Ces images soulignent l’importance des séquences FLAIR et SWI dans la détection précoce et précise des hémorragies corticales.
- • Détecte un certain nombre d’autres causes (tumeurs, thrombose veineuse cérébrale, syndrome de vasoconstriction cérébrale réversible).
3 553Ponction lombaire
- •
 N’est jamais faite d’emblée.
N’est jamais faite d’emblée. - • Est indiquée lorsque l’imagerie cérébrale ne montre pas l’HSA.
- • Est contre-indiquée en cas d’hémorragie responsable d’un effet de masse.
Résultats de la ponction lombaire
Les anomalies caractéristiques du liquide cérébrospinal (LCS) en cas HSA sont les suivantes :
- •
 pression du LCS élevée (> 25 cm d’H2O), témoignant de l’augmentation de la pression intracrânienne;
pression du LCS élevée (> 25 cm d’H2O), témoignant de l’augmentation de la pression intracrânienne; -
• aspect visuel :
- – examen des tubes du LCS : liquide uniformément rosé, incoagulable, dans les trois tubes,
-
– teinte rosé jaunâtre du fait de la présence de pigments sanguins (bilirubine et oxyhémo-globine à partir de la 12e heure de l’hémorragie) (tableau 29.1),
 Tableau comparatif du liquide cérébrospinal (LCS) dans l’hémorragie sous-arachnoïdienne (HSA) et ponction lombaire (PL) traumatique.
Tableau comparatif du liquide cérébrospinal (LCS) dans l’hémorragie sous-arachnoïdienne (HSA) et ponction lombaire (PL) traumatique.LCS dans l’HSA LCS en cas de PL traumatique Liquide uniformément rosé, incoagulable, dans les trois tubes Liquide coagulable et de moins en moins sanglant au fur et à mesure du recueil Surnageant xanthochromique après centrifugation et présence de chromoprotéines Surnageant clair après centrifugation avec absence de pigments sanguins Rapport érythrocytes/leucocytes supérieur à celui du sang (103) Rapport érythrocytes/leucocytes superposable à celui du sang Présence de chromoprotéines Pression du LCS élevée Pression d’ouverture normale - –
 analyse par spectrophotométrie avec recherche des chromoprotéines : oxyhémoglo-bine, bilirubine, méthémoglobine, ferritine.
analyse par spectrophotométrie avec recherche des chromoprotéines : oxyhémoglo-bine, bilirubine, méthémoglobine, ferritine.
554
C Explorations complémentaires à visée étiologique
1 Imagerie vasculaire
-
•
 L’angioscanner ou l’ARM permettent de visualiser dans la majorité des cas la présence de l’anévrisme artériel (image d’addition, fig. 29.3).
L’angioscanner ou l’ARM permettent de visualiser dans la majorité des cas la présence de l’anévrisme artériel (image d’addition, fig. 29.3).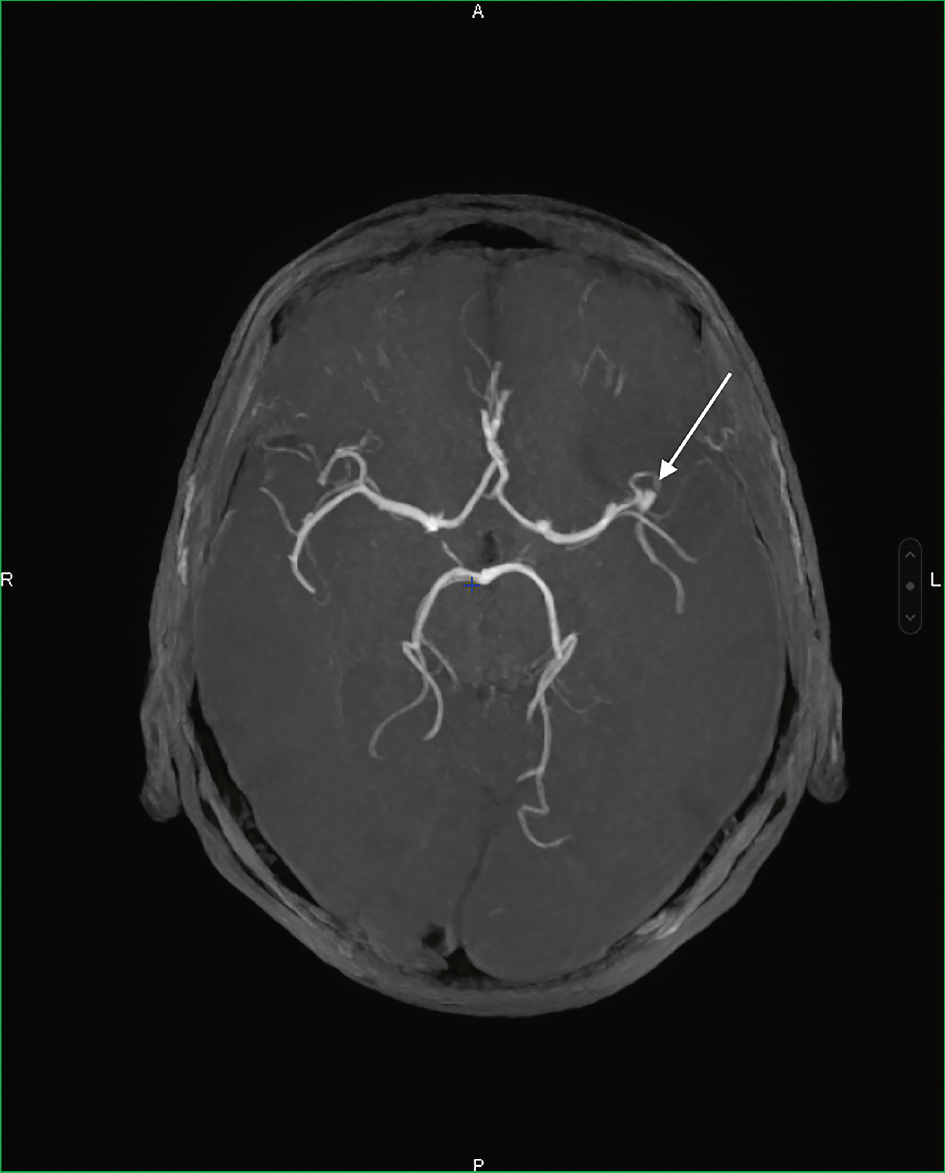
Fig. 29.3  Angiographie par résonance magnétique cérébrale montrant un anévrisme de l’artère cérébrale moyenne gauche (flèche).
Angiographie par résonance magnétique cérébrale montrant un anévrisme de l’artère cérébrale moyenne gauche (flèche).Image d’angiographie par résonance magnétique cérébrale en vue axiale, centrée sur le polygone de Willis. Les principales artères intracrâniennes sont bien visibles en hypersignal, permettant une analyse fine de leur morphologie. Une flèche blanche pointe une dilatation focale localisée sur le segment bifurcationnel de l’artère cérébrale moyenne gauche, compatible avec un anévrisme. Cette image met en évidence la capacité de l’ARM à détecter les anomalies vasculaires intracrâniennes sans injection de produit de contraste iodé, en visualisant nettement les structures artérielles cérébrales dans leur continuité et leur calibre.
- • L’angiographie conventionnelle, ou artériographie cérébrale par cathéterisme artériel, est réalisée lors du traitement de l’anévrisme ou à visée diagnostique dans certains cas où l’étiologie reste incertaine.
555Les objectifs du traitement sont de :
- • lutter contre la douleur du syndrome méningé aigu;
- • traiter la cause du saignement;
- • prévenir et traiter les complications éventuelles.
2 Prise en charge thérapeutique
- • Hospitalisation en urgence dans une unité de soins intensifs ou de réanimation d’un centre spécialisé assurant une surveillance continue (pouls, pression artérielle, conscience toutes les heures, température toutes les 8 heures, examen neurologique plusieurs fois par jour) et une prise en charge pluridisciplinaire.
-
• Le traitement comporte plusieurs axes résumés dans la figure 29.4.
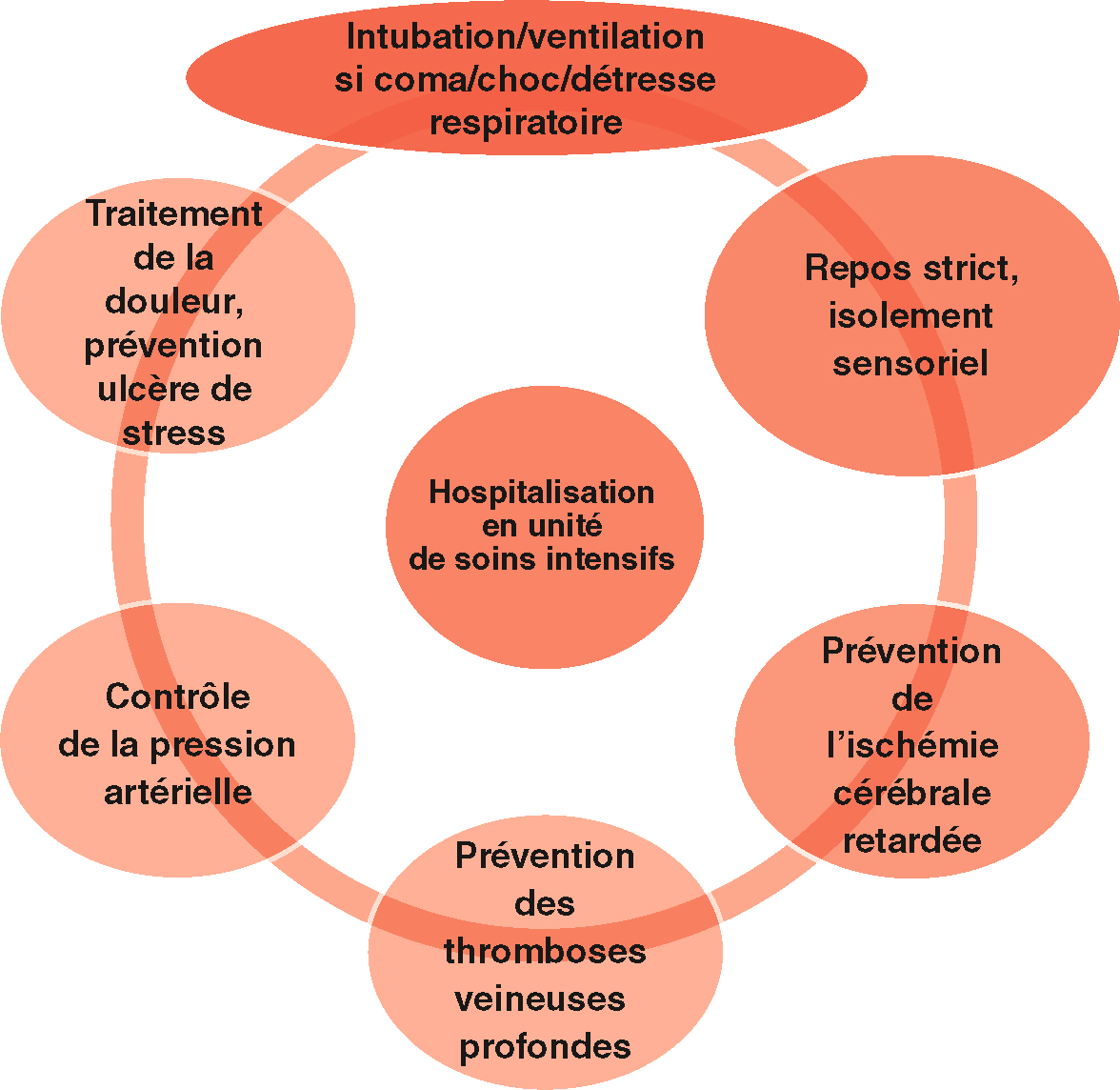
Fig. 29.4  Axes de la prise en charge thérapeutique de l’HSA.
Axes de la prise en charge thérapeutique de l’HSA.1 est une vue circulaire montrant l'axe essentiel du traitement thérapeutique de l'hémorragie sous-arachnoïdienne dans une unité de soins intensifs. Le centre possède des hospitalisations en soins intensifs d'un cadre critique pour une surveillance étroite et une intervention rapide. Les priorités incluent l'intubation et la ventilation en cas de coma, de choc ou d'essoufflement, et un calme strict dans la séparation sensorielle qui limite les stimuli qui peuvent exacerber les conditions neurologiques. La prévention des clochards cérébraux retardés est une étape importante pour éviter les complications de la colonne vertébrale vasculaire. Il est également important de contrôler strictement la pression artérielle pour prévenir la thrombose veineuse profonde, de réduire la récupération, d'assurer un soulagement de la douleur et en même temps prévenir les ulcères de stress. Cette approche intensive coordonnée à l'échelle mondiale nous permet de limiter les résultats neurologiques et d'optimiser le potentiel de reconstruction.
3 Prévention du resaignement
- • Exclusion précoce de l’anévrisme intracrânien dans les 24 à 48 heures qui suivent l’hospitalisation (et le plus précocement par rapport à la rupture). En cas de resaignement, la mortalité peut atteindre 60 %.
-
• Traitement de l’anévrisme : deux types de traitement :
- – le traitement chirurgical;
- –
 le traitement endovasculaire (ou embolisation) : il est le traitement de première intention des anévrismes rompus.
le traitement endovasculaire (ou embolisation) : il est le traitement de première intention des anévrismes rompus.
556
4 Hydrocéphalie
-
•
 Elle est liée à l’obstruction des voies de circulation du LCS (fig. 29.5A).
Elle est liée à l’obstruction des voies de circulation du LCS (fig. 29.5A).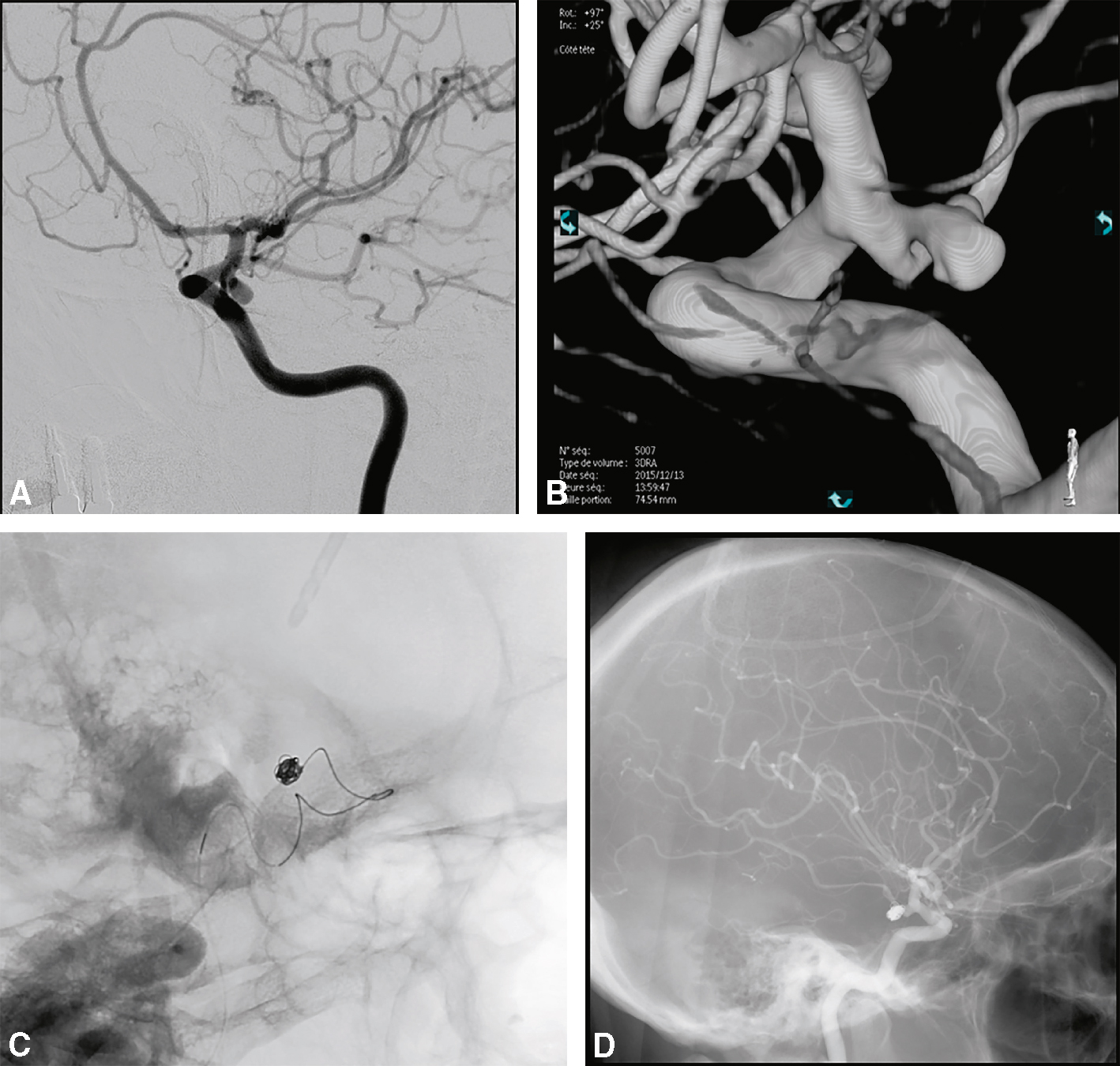
Fig. 29.5  Angiographie conventionnelle (temps artériel) : anévrisme de la communicante postérieure gauche (A), image 3D (B), pendant (C) et après l’embolisation (les clichés montrant l’exclusion de l’anévrisme : D).
Angiographie conventionnelle (temps artériel) : anévrisme de la communicante postérieure gauche (A), image 3D (B), pendant (C) et après l’embolisation (les clichés montrant l’exclusion de l’anévrisme : D).Cette série d'images montre des étapes différentes de traitement des anévrismes intracrâniens dans le communicateur postérieur gauche. Cette photographie est une dilatation d'anévrisme bien définie dans la partie proximale du communicateur postérieur gauche, conservée par l'angiographie conventionnelle de l'âge artériel. Dans la reconstruction 3D, avec une reconstruction très précise, la figure B montre la morphologie complexe de l'anévrisme, le collier et la relation avec les branches artérielles adjacentes. La figure C illustre les étapes d'embolisation procédurale dans lesquelles la mise en œuvre en spirale (spirale) se distingue sous le contrôle scortique du rayonnement du sac d'anévrisme. Enfin, les images des résultats finaux après embolisation sont présentées avec l'exclusion complète des anévrismes dans la rivière circulatoire, indiquant le succès du traitement endovasculaire. Ce processus démontre la précision et l'efficacité de la neuroradiologie interventionnelle dans la prévention de la destruction de l'anévrisme.
- • Elle peut être précoce (3–72 heures) ou retardée (3e jour–3e semaine).
-
• Son traitement consiste en la mise en place d’un cathéter de dérivation ventriculaire externe (fig. 29.6).
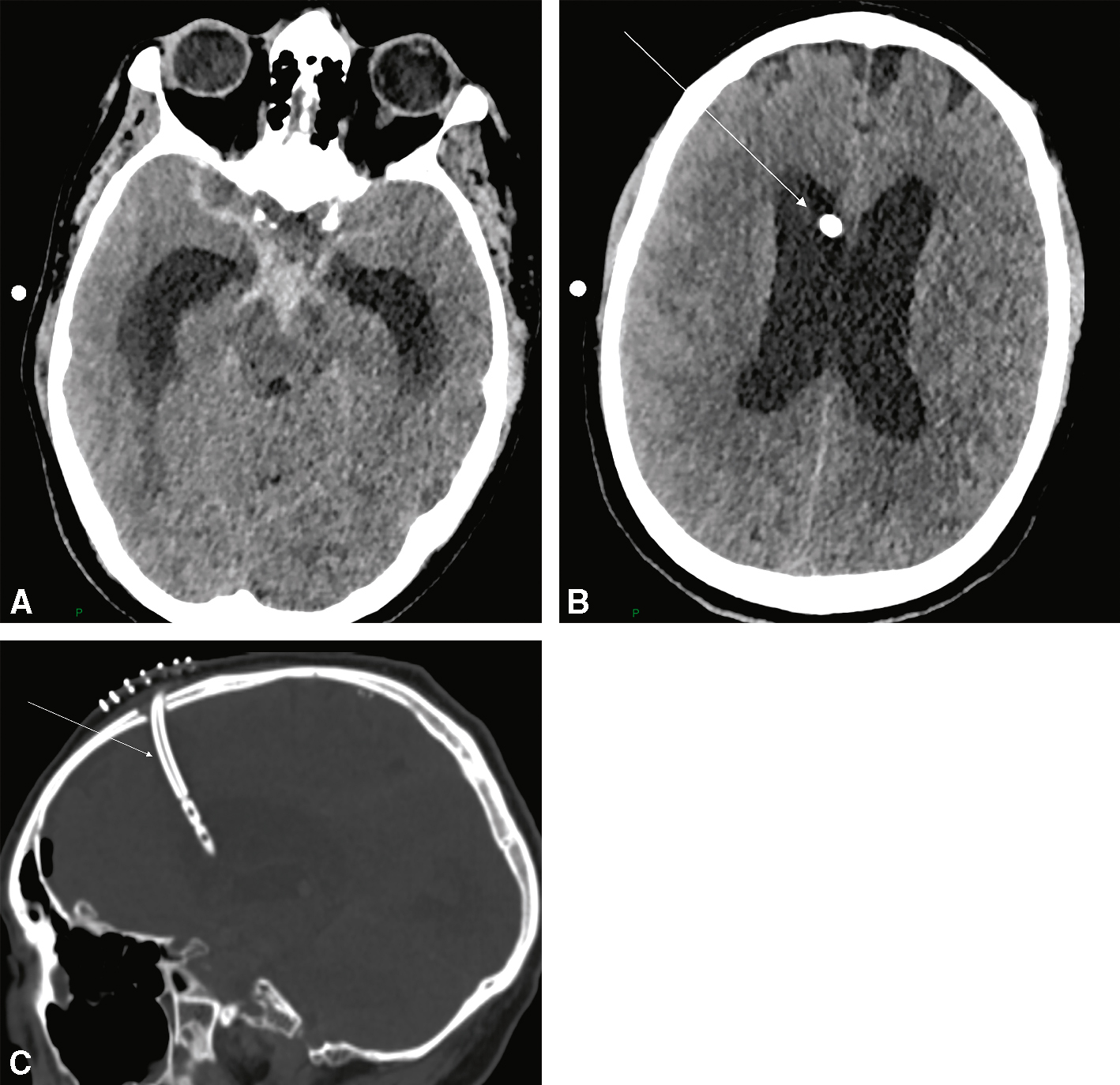
Fig. 29.6  Scanner cérébral montrant la pose d’un cathéter de dérivation ventriculaire externe (DVE).
Scanner cérébral montrant la pose d’un cathéter de dérivation ventriculaire externe (DVE).
A. Scanner cérébral en coupe axial montrant une HSA des citernes de la base avec dilatation des cornes temporales des ventricules latéraux. B. Scanner cérébral en coupe axial montrant une DVE (flèche) positionnée dans la corne frontale du ventricule latéral droit. C. Scanner cérébral en coupe sagittale montrant la trajectoire de la DVE (flèche).Les trois coupes tomodensitométriques (axiales et sagittale) montrent l’emplacement d’un cathéter de dérivation ventriculaire externe. Sur les vues axiales, la première image montre une dilatation des ventricules latéraux, en particulier des cornes frontales, suggérant une hydrocéphalie active. La seconde image met en évidence le cathéter placé dans le ventricule droit, bien centré sans déviation, avec son extrémité visible au sein du liquide cérébrospinal. La coupe sagittale confirme le trajet du cathéter depuis le scalp jusqu’à la cavité ventriculaire. Aucun signe d’hémorragie, de malposition ou de complication immédiate n’est visible.
5 557Ischémie cérébrale retardée (ICR)
- •
 Complique l’occlusion et/ou le vasospasme des artères distales. Elle s’associe, ou pas, avec un vasospasme de la portion proximale des artères cérébrales.
Complique l’occlusion et/ou le vasospasme des artères distales. Elle s’associe, ou pas, avec un vasospasme de la portion proximale des artères cérébrales. - •
 La sévérité de l’HSA, l’étendue du saignement et les troubles de la vigilance initiaux sont des facteurs de risque d’ICR.
La sévérité de l’HSA, l’étendue du saignement et les troubles de la vigilance initiaux sont des facteurs de risque d’ICR. - •
 L’ICR est évoquée devant la survenue d’une confusion, de troubles de la vigilance et/ou de déficits neurologiques focaux et parfois fluctuants en rapport avec de nouvelles lésions ischémiques sur l’imagerie cérébrale.
L’ICR est évoquée devant la survenue d’une confusion, de troubles de la vigilance et/ou de déficits neurologiques focaux et parfois fluctuants en rapport avec de nouvelles lésions ischémiques sur l’imagerie cérébrale. - •
 Le vasospasme survient habituellement entre le 4e jour et la fin de la 2e semaine avec un pic vers le 7e–8e jour.
Le vasospasme survient habituellement entre le 4e jour et la fin de la 2e semaine avec un pic vers le 7e–8e jour. - •
 La prévention de l’ICR repose sur le maintien d’une euvolémie, la lutte contre l’hypo-natrémie et l’hypotension, ainsi qu’un traitement par nimodipine.
La prévention de l’ICR repose sur le maintien d’une euvolémie, la lutte contre l’hypo-natrémie et l’hypotension, ainsi qu’un traitement par nimodipine.
6 Autres complications
- • Hyponatrémie par syndrome de perte en sel en rapport avec sécrétion inappropriée notamment de brain natriureticpeptide (BNP).
- • Cardiopathie catécholaminergique (tako tsubo).
- • 558Complications de réanimation (pneumopathie, ulcère, etc.).
- • Anosmie pour les anévrismes de la communicante antérieure.
- • Crises comitiales (HSA abondantes, hémorragie intraparenchymateuse, ischémie).
- • Troubles cognitifs.
